


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
| A、25℃时,0.1mol/L的醋酸中,c(H+)=0.1mol/L | ||
| B、在稀醋酸溶液中加入少量醋酸钠固体,会促进醋酸的电离 | ||
| C、在稀氨水中通入氨气,所得溶液的pH减小 | ||
D、向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
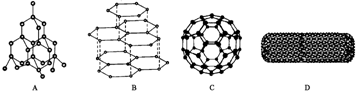
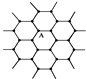 可推算在石墨晶体中,每个正六边形平均所占有的C 原子数与C-C键数之比为
可推算在石墨晶体中,每个正六边形平均所占有的C 原子数与C-C键数之比为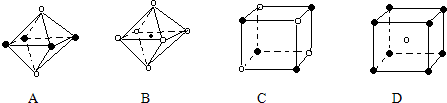
查看答案和解析>>
科目:高中化学 来源: 题型:
| 结晶 |
| 精制 |
| 电解 |
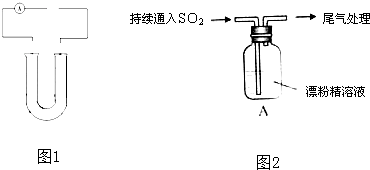
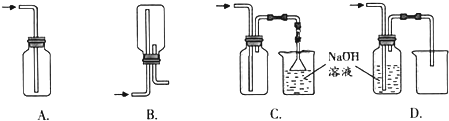
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
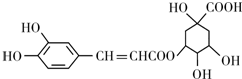
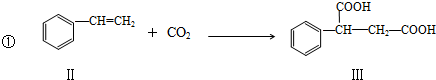
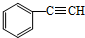 和H2三者发生反应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应,Ⅵ和Ⅶ的结构简式分别为
和H2三者发生反应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应,Ⅵ和Ⅶ的结构简式分别为查看答案和解析>>
科目:高中化学 来源: 题型:
A、C
| ||||||
B、Cu
| ||||||
C、CaO
| ||||||
D、Fe
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com