
【题目】下列对化学反应的认识正确的是( )
A.化学反应过程中,断键吸热,成键放热
B.如果某化学反应的△H和△S均小于0,则反应一定能自发进行
C.对于同一个化学反应,一步完成和分几步完成,其反应的焓变不相同
D.反应物的总焓大于反应产物的总焓时,△H>0
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】室温下,将 0.10 mol·L-1 盐酸滴入 20.00 mL 0.10 mol·L-1 氨水中,溶液中 pH 和 pOH 随加入盐酸体积变化曲线如图所示。已知:pOH=-lg c(OH-),下列正确的是

A. M 点所示溶液中可能存在c(Cl-)> c(NH4+)
B. N 点所示溶液中可能存在:c (NH4+)+ c(NH3﹒H2O)= c(Cl-)
C. Q 点盐酸与氨水恰好中和
D. M 点到Q点所示溶液中水的电离程度先变大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮可以形成多种离子和分子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于 NH4+的性质。
(1)写出N2H62+中共价键的类型除极性键,非极性键外再写出一种__________。
(2)下列关于NH2-的说法合理的是____________________(填字母)。
A.H-N-H夹角109.5° B. H-N-H夹角180° C. H-N-H夹角大约105°
D.中心原子的杂化轨道为四面体形 E. 该离子为V形 F.易与H+结合
(3)写出N3-的等电子体且是中性分子的化学式___________________(一种)。
(4)N2H4名称是肼,也叫联氨,通常为无色油状发烟液体,有吸湿性,有氨的臭味。可作为火箭的燃料。其沸点比氨气高的主要原因是________________________。
利用含N的铜萃取剂M可通过如下反应实现铜离子的富集:
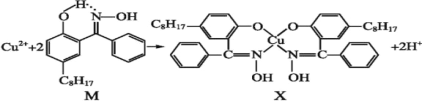
(5)X难溶于水、易溶于有机溶剂,X中配位原子是______。
(6)M中氮原子以_______杂化轨道与氧原子形成σ键。
(7)M与W(如图)是同分异构体,则在水中溶解度较大的物质是___(填字母M或W)。
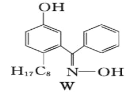
(8)常用![]() 表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为
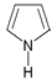
表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为![]() 。吡咯(如图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,已知氮原子有一对未参与杂化的电子占据p轨道,吡咯分子中的大π键应表示为________。
。吡咯(如图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,已知氮原子有一对未参与杂化的电子占据p轨道,吡咯分子中的大π键应表示为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】称取4.00g氧化铜和氧化铁固体混合物,加入50.0mL2.00mol·L-1的硫酸充分溶解,往所得溶液中加入5.60g铁粉,充分反应后,得固体的质量为3.04g。请计算:
(1)加入铁粉充分反应后,溶液中溶质的物质的量_________________。
(2)固体混合物中氧化铜的质量_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.加入正催化剂,活化分子百分数增大,化学反应速率一定增大
B.熵增加且放热的反应一定是自发反应
C.任何条件下,化学反应的焓变都等于化学反应的反应热
D.常温下硝酸铵能够溶于水,因为其溶于水是一个熵增大过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.有下列微粒:①11H、②21H、③31H、④16O2、⑤16O3。回答下列问题(填序号):
(1)以上5种微粒中共含有___种元素,__互为同素异形体;
(2)___互称为同位素。
Ⅱ.根据下列提供的一组物质回答问题:
①HCl ②CaCl2 ③MgO ④Cl2 ⑤NaOH ⑥NH4Cl
(1)仅含共价键的是___;离子化合物有___;(用序号表示)
(2)既有离子键又有共价键的是___;含有非极性键的是__;(用序号表示)
(3)HCl的电子式:____;NaOH的电子式:____;MgO的电子式:____。
用电子式表示CaCl2的形成过程:____________
用电子式表示Cl2的形成过程:______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种物质分子式都是C7H8O,若滴入FeCl3 溶液,只有C呈紫色;若投入金属钠,只有B没有变化。在A、B中分别加入溴水,溴水不褪色。
(1)写出A、B、C的结构简式: A:__________________; B:___________________;C:____________________。
(2)C的另外两种同分异构体的结构简式是: ①__________________;②______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物说法正确的是( )
A. 可用高锰酸钾溶液鉴别甲苯、环己烯与溴苯
B. ![]() 是由单体CH2=CH—CH3和CH2=CH2发生加聚反应的产物
是由单体CH2=CH—CH3和CH2=CH2发生加聚反应的产物
C. 石油裂解和油脂皂化都是由高分子化合物生成小分子物质的过程
D. 淀粉与纤维素互为同分异构体,二者水解的最终产物相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某化学兴趣小组探究化学能转变为电能的装置。

(1)当电极a为Zn、电极b为Fe、电解质溶液为稀硫酸时,SO42-向_____极(填a或b)移动,正极的电极反应式为:_____________
(2)若依据氧化还原反应:Cu+2Fe3+=Cu2++2Fe2+设计原电池,电极a为石墨、则电极b为电池的_______极,发生的电极反应式为:_______,电极a上发生的电极反应为______(填“氧化”或“还原”)反应。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用酸性溶液为电解液;则氢气应通入_____极(填a或b)。a极发生电极反应式为:________。当电路中通过2mol电子时,理论上消耗标况下氧气_____L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com