
【题目】下图是某化学兴趣小组探究化学能转变为电能的装置。

(1)当电极a为Zn、电极b为Fe、电解质溶液为稀硫酸时,SO42-向_____极(填a或b)移动,正极的电极反应式为:_____________
(2)若依据氧化还原反应:Cu+2Fe3+=Cu2++2Fe2+设计原电池,电极a为石墨、则电极b为电池的_______极,发生的电极反应式为:_______,电极a上发生的电极反应为______(填“氧化”或“还原”)反应。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用酸性溶液为电解液;则氢气应通入_____极(填a或b)。a极发生电极反应式为:________。当电路中通过2mol电子时,理论上消耗标况下氧气_____L。
【答案】a 2H++2e-=H2↑ 负 Cu-2e-=Cu2+ 还原 b O2+4e-+4H+=2H2O 11.2
【解析】
(1)根据原电池的工作原理来回答;
(2)原电池中失电子的物质作负极,根据方程式知,铜失电子,发生氧化反应,作负极,导电的非金属碳棒作正极,正极上溶液中的Fe3+获得电子,发生还原反应;
(3)在燃料电池中,通燃料的电极为负极,通入氧气的电极是正极,正极是氧气得电子,电子从负极流向正极,根据电子转移数目作计算。
(1) Zn、Fe、稀硫酸构成的原电池,金属Zn作负极,金属Fe为正极,SO42-向正电荷较多的负极a电极方向移动;正极上溶液中的H+获得电子,发生还原反应,电极反应为:2H++2e-=H2↑;
(2)在原电池中失电子的物质作负极,根据方程式知,铜失电子,发生氧化反应,作负极;由于电极a为石墨,是惰性电极,则电极b为Cu,是电池的负极,负极的电极反应式为Cu-2e-=Cu2+;在导电的非金属碳棒作正极,正极上溶液中的Fe3+获得电子,发生还原反应;
(3)在氢氧燃料电池中,燃料氢气在负极通入,氧气在正极通入,在正极上氧气得电子,电子从负极流向正极。若以电极a为正极,电极b为负极,氢气为燃料,采用酸性溶液为电解液;则氢气应通入b极,在正极a极上O2获得电子,与溶液中 H+结合形成水,所以a电极发生电极反应式为:O2+4e-+4H+=2H2O,根据电极反应式可知:每有1molO2发生反应,转移4mol电子,则当电路中通过2mol电子时,理论上消耗标况下氧气的物质的量是0.5mol,其在标准状况下的体积V(O2)= 0.5mol ×22.4L/mol=11.2L。


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】下列对化学反应的认识正确的是( )
A.化学反应过程中,断键吸热,成键放热
B.如果某化学反应的△H和△S均小于0,则反应一定能自发进行
C.对于同一个化学反应,一步完成和分几步完成,其反应的焓变不相同
D.反应物的总焓大于反应产物的总焓时,△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(化学组成为FeC2O4·2H2O)是一种淡黄色晶体粉末,是生产锂电池的原材料。已知FeC2O4·2H2O在300 ℃左右完全分解生成FeO、CO2、CO、H2O四种氧化物。某学习小组欲验证草酸亚铁晶体的分解产物。
I.甲组同学设计了如下实验装置:

(1)实验开始前,鼓入氮气排出空气的目的是_____________________________。
(2)检验水和二氧化碳的装置分别是_______和_______。
(3)设计实验验证装置A中黑色残留物不含有Fe3O4_______________________________________________________________(简要说明实验操作,现象和结论)。
II.乙组同学选用甲组实验中的装置A(接口用x表示)和下图所示的装置(可以重复选用)验证分解产物CO。
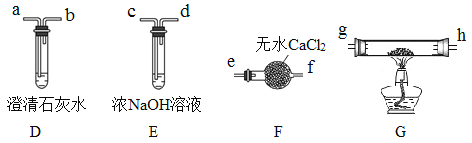
(4)乙组同学的实验装置中,依次连接的合理顺序为x→______g→h→a(用接口字母和“→”表示)。装置G反应管中盛有的物质是氧化铜。能证明草酸晶体分解产物中有CO的现象是___________。
(5)按照题目提供的装置和要求设计的实验明显存在的一个不足是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的短周期主族元素,A元素的一种单质是自然界最硬的物质,B为最活泼的非金属元素,C元素的原子的电子层数是最外层电子数的3倍,D元素最高化合价为+6价。
(1)D在周期表中的位置是 _____________,E的离子结构示意图_____________;
(2)C与D 形成化合物的电子式为_____________;
(3)A、D、E三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是______;
(4)由B、C、D形成的简单离子半径由大到小的顺序是________________;
(5)B形成的氢化物沸点比E形成的氢化物沸点_______(填“高”或“低”),原因是___________;
(6)DBn做制冷剂替代氟利昂,对臭氧层完全没有破坏作用,是一种很有发展潜力的制冷剂.该物质的摩尔质量为146g/mol,该物质的化学式为____。已知DBn在温度高于45°时为气态,DBn属于____晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究人员从木耳菜中提取过氧化物酶(POD),分别与四种不同酚类物质及H2O2进行催化反应,结果如图所示。下列相关说法正确的是
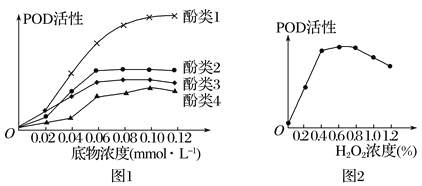
A. 图1所示的实验目的是探究不同酚类物质的浓度对POD活性的影响
B. 当底物浓度为0.08 mmolL-1时,POD催化酚类2的反应速率一定大于酚类3
C. 由图2可知,H2O2浓度过高会抑制POD的活性,降低浓度后POD的活性一定会恢复
D. H2O2对POD活性的影响与温度和pH对POD活性的影响相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数为x的元素E在周期表中位于A、B、C、D四种元素中间(如图所示),则A、B、C、D四种元素的原子序数之和不可能是(镧系、锕系、0族元素除外)( )
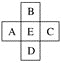
A. 4xB. 4x+14
C. 4x+10D. 4x+6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体,经历了下列过程(已知 Fe3+在 pH=5时沉淀完全).其中分析错误的是( )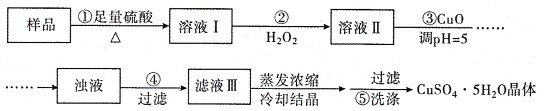
A. 步骤②发生的主要反应为:2Fe2++H2O2+2H+=2Fe3++2H2O
B. 步骤②不能用氯水、硝酸等强氧化剂代替H2O2
C. 步骤③用 CuCO3代替CuO也可调节溶液的pH
D. 滤液Ⅲ中无Fe3+,在后面的结晶过程中不会析出Fe2(SO4)3造成产品不纯,因此可直接用蒸发结晶的方法得到胆矾晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤代烃在碱性醇溶液中能发生消去反应。例如,

该反应式也可表示为

下面是几种有机化合物的转化关系:

(1)根据系统命名法,化合物A的名称是_____________。
(2)上述框图中,①_________是反应,③___________是反应。
(3)化合物E是重要的工业原料,写出由D生成E的化学方程式:_________。
(4)C2的结构简式是,F1的结构简式是______________,F1与F2互为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①CH3CH=CHCH3、② ![]() 、③
、③![]() 、④CH3CH2CH(C2H5)2、⑤35Cl、⑥O2、⑦-CH3、⑧CH2=CH-CH=CH2、⑨37Cl、⑩O3
、④CH3CH2CH(C2H5)2、⑤35Cl、⑥O2、⑦-CH3、⑧CH2=CH-CH=CH2、⑨37Cl、⑩O3
(1)互为同系物的有___________________(用序号表示)。
(2)互为同位素的有___________________(用序号表示)。
(3)③的系统名称_____________________,②的系统名称_____________________。
(4)写出⑧与Br2 按照1:1发生加成反应所得产物的结构简式______________________________。
(5)等物质的量的⑦和⑩的电子数之比为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com