
【题目】草酸亚铁晶体(化学组成为FeC2O4·2H2O)是一种淡黄色晶体粉末,是生产锂电池的原材料。已知FeC2O4·2H2O在300 ℃左右完全分解生成FeO、CO2、CO、H2O四种氧化物。某学习小组欲验证草酸亚铁晶体的分解产物。
I.甲组同学设计了如下实验装置:

(1)实验开始前,鼓入氮气排出空气的目的是_____________________________。
(2)检验水和二氧化碳的装置分别是_______和_______。
(3)设计实验验证装置A中黑色残留物不含有Fe3O4_______________________________________________________________(简要说明实验操作,现象和结论)。
II.乙组同学选用甲组实验中的装置A(接口用x表示)和下图所示的装置(可以重复选用)验证分解产物CO。
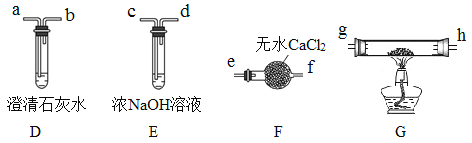
(4)乙组同学的实验装置中,依次连接的合理顺序为x→______g→h→a(用接口字母和“→”表示)。装置G反应管中盛有的物质是氧化铜。能证明草酸晶体分解产物中有CO的现象是___________。
(5)按照题目提供的装置和要求设计的实验明显存在的一个不足是________________________。
【答案】避免生成的FeO被氧化 B C 取少量装置A中固体残留物于试管中,加入稀硫酸溶解,然后滴加KSCN溶液,溶液不显红色,说明固体残留物中不含有Fe3O4 c→d→a→b→e→f G中的粉末由黑色变为红色,其后的D中的石灰水变浑浊 未对尾气进行处理,可造成环境污染
【解析】
本题主要考查验证草酸亚铁晶体的分解产物的探究实验。
I.(1)实验开始前,鼓入氮气排出空气的目的是避免生成的FeO被氧化。
(2)检验水和二氧化碳的装置分别是B和C。
(3)设计实验验证装置A中黑色残留物不含有Fe3O4,因为Fe3O4+8H+![]() 2Fe3++ Fe2++4H2O,所以可以检验Fe3+:取少量装置A中固体残留物于试管中,加入稀硫酸溶解,然后滴加KSCN溶液,溶液不显红色,说明固体残留物中不含有Fe3O4。
2Fe3++ Fe2++4H2O,所以可以检验Fe3+:取少量装置A中固体残留物于试管中,加入稀硫酸溶解,然后滴加KSCN溶液,溶液不显红色,说明固体残留物中不含有Fe3O4。
II.(4)乙组同学的实验装置中,通过E除去CO2,再通过D确认,最后通过F干燥气体,所以依次连接的合理顺序为x→c→d→a→b→e→f →g→h→a。装置G反应管中盛有的物质是氧化铜。能证明草酸晶体分解产物中有CO的现象是G中的粉末由黑色变为红色,其后的D中的石灰水变浑浊。
(5)按照题目提供的装置和要求设计的实验明显存在的一个不足是未对尾气进行处理,可造成环境污染


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
【题目】氮可以形成多种离子和分子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于 NH4+的性质。
(1)写出N2H62+中共价键的类型除极性键,非极性键外再写出一种__________。
(2)下列关于NH2-的说法合理的是____________________(填字母)。
A.H-N-H夹角109.5° B. H-N-H夹角180° C. H-N-H夹角大约105°
D.中心原子的杂化轨道为四面体形 E. 该离子为V形 F.易与H+结合
(3)写出N3-的等电子体且是中性分子的化学式___________________(一种)。
(4)N2H4名称是肼,也叫联氨,通常为无色油状发烟液体,有吸湿性,有氨的臭味。可作为火箭的燃料。其沸点比氨气高的主要原因是________________________。
利用含N的铜萃取剂M可通过如下反应实现铜离子的富集:
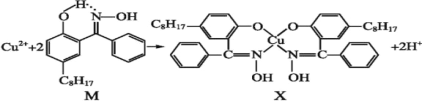
(5)X难溶于水、易溶于有机溶剂,X中配位原子是______。
(6)M中氮原子以_______杂化轨道与氧原子形成σ键。
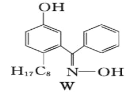
(7)M与W(如图)是同分异构体,则在水中溶解度较大的物质是___(填字母M或W)。
(8)常用![]() 表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为
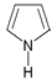
表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为![]() 。吡咯(如图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,已知氮原子有一对未参与杂化的电子占据p轨道,吡咯分子中的大π键应表示为________。
。吡咯(如图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,已知氮原子有一对未参与杂化的电子占据p轨道,吡咯分子中的大π键应表示为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种物质分子式都是C7H8O,若滴入FeCl3 溶液,只有C呈紫色;若投入金属钠,只有B没有变化。在A、B中分别加入溴水,溴水不褪色。
(1)写出A、B、C的结构简式: A:__________________; B:___________________;C:____________________。
(2)C的另外两种同分异构体的结构简式是: ①__________________;②______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物说法正确的是( )
A. 可用高锰酸钾溶液鉴别甲苯、环己烯与溴苯
B. ![]() 是由单体CH2=CH—CH3和CH2=CH2发生加聚反应的产物
是由单体CH2=CH—CH3和CH2=CH2发生加聚反应的产物
C. 石油裂解和油脂皂化都是由高分子化合物生成小分子物质的过程
D. 淀粉与纤维素互为同分异构体,二者水解的最终产物相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成。其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子。下列说法错误的是( )
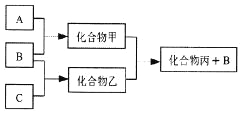
A. Z元素位于第二周期第VIA族
B. 可用排水法收集化合物乙
C. 元素X、Y、Z的原子半径大小关系为X<Z<Y
D. 化合物甲溶于化合物丙中,存在的微粒有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应2A(g)![]() B(g) ΔH>0,在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够长时间后反应再次达到平衡状态,此时c(A)/c(B=b,下列叙述正确的是( )
B(g) ΔH>0,在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够长时间后反应再次达到平衡状态,此时c(A)/c(B=b,下列叙述正确的是( )
A. 在该温度下,保持容积固定不变,向容器内补充了B气体,则a<b
B. 若a=b,则容器中可能使用了催化剂
C. 若其他条件不变,升高温度,则a<b
D. 若保持温度、压强不变,充入惰性气体,则a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某化学兴趣小组探究化学能转变为电能的装置。

(1)当电极a为Zn、电极b为Fe、电解质溶液为稀硫酸时,SO42-向_____极(填a或b)移动,正极的电极反应式为:_____________
(2)若依据氧化还原反应:Cu+2Fe3+=Cu2++2Fe2+设计原电池,电极a为石墨、则电极b为电池的_______极,发生的电极反应式为:_______,电极a上发生的电极反应为______(填“氧化”或“还原”)反应。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用酸性溶液为电解液;则氢气应通入_____极(填a或b)。a极发生电极反应式为:________。当电路中通过2mol电子时,理论上消耗标况下氧气_____L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为解决日益加剧的温室效应等问题,科学家正在研究建立如下图所示的二氧化碳新循环体系:
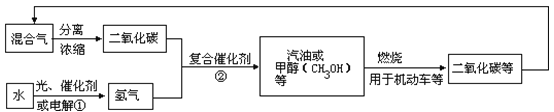
上述关系图能反映的化学观点或化学思想有 ( )
①化学变化中元素种类是守恒的;②燃烧时化学能可以转化为热能和光能;③光能或电能可以转化为化学能;④无机物和有机物可以相互转化;⑤二氧化碳也是一种重要的资源。
A. ①②③ B. ①②④⑤ C. ①④⑤ D. ①②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com