
【题目】甘油(丙三醇)在纺织、医药、化妆品工业及日常生活中用途很广,可以通过以下方法合成:
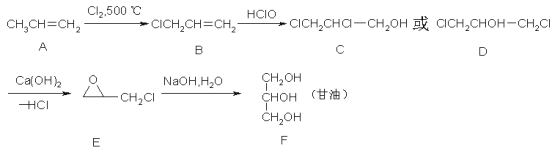
完成下列填空:
(1)A中官能团的名称是____________,A→B的反应类型是__________;
(2)写出A发生加聚反应后产物的结构简式__________________;
(3)B→C的反应类型是______________,C与D互为______________;
(4)写出A→B的化学方程式:__________________________________;
【答案】碳碳双键 取代反应 ![]() 加成反应 同分异构体 CH3CH=CH2+Cl2
加成反应 同分异构体 CH3CH=CH2+Cl2![]() ClCH2CH=CH2+HCl
ClCH2CH=CH2+HCl
【解析】
有怎样的基团就有怎样的化学性质。认真比较在某反应发生后,有机物哪部分基团或价键发生了变化,从而判断发生了怎样的反应。从题给的合成路径来看,丙烯首先发生了一氯代反应,然后与HClO发生加成反应,后脱去一分子HCl成三元环,最后在碱性条件下发生水解。
(1)A中官能团的名称是碳碳双键,注意不要说双键;A→B是在加热的条件下发生甲基上氢的卤代反应,所以该反应类型是取代反应;
(2)A是丙烯,其发生加聚反应后生成聚丙烯:![]() ;
;
(3)分析比较B(![]() )和C(
)和C(![]() )的结构,可以发现原有碳碳双键消失,其两个碳原子上分别连上了Cl和OH,应是加成反应;C与D分子式相同,结构不同,应互称为同分异构体;
)的结构,可以发现原有碳碳双键消失,其两个碳原子上分别连上了Cl和OH,应是加成反应;C与D分子式相同,结构不同,应互称为同分异构体;
(4)写出A→B的化学方程式:CH3CH=CH2+Cl2![]() ClCH2CH=CH2+HCl。
ClCH2CH=CH2+HCl。


科目:高中化学 来源: 题型:
【题目】部分中学化学常见元素原子结构及性质如表所示
元素 | 结构及性质 |
A | A在第三周期中简单离子半径最小 |
B | B原子最外层电子数是内层电子数的 |
C | 使用最广泛的金属元素C能形成两种氯化物,其相对分子质量之差为35.5 |
D | D与B同主族,且通常状况下D没有正化合价 |
E | E在周期表中位于IA族,有人认为将其排在VIIA族也有一定道理 |
F | F与B同周期,其最高价氧化物的水化物与A或B的最高价氧化物的水化物均能反应 |
(1)C元素在周期表中的位置_____________;E形成的一种简单离子能支持“将E排在VIIA族”这一观点,该离子的结构示意图为_______________________。
(2)E与D可以按原子个数比2:1、1:1形成两种化合物X、Y,区别X、Y这两种物质的实验方法为________________________________。
E与B形成的一种化合物Z与X、Y中的一种电子总数相同且能发生化学反应,写出该反应的化学方程式__________________________(用相应化学式表示)
(3)请画出化合物F2B2的电子式__________,该化合物中含有的化学键类型是_______。
(4)将A、C的单质用导线连接后插入F的最高价氧化物的水化物溶液中可形成原电池,该原电池中阴离子移向_________(填“A”或“C”),写出该原电池总反应的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)选择下列实验方法分离物质,将分离方法的序号填在横线上:a、萃取分液法;b、加热分解; c、结晶法; d、分液法; e、蒸馏法; f、过滤法; g、渗析法
①_____从硝酸钾和氯化钠的混合溶液中获得硝酸钾
②______分离水和苯的混合物
③_____除去氢氧化铁胶体中混有的NaCl
④______分离碘和四氯化碳
(2)实验室用4.0 mol/L NaCl溶液配制100mL 0.50 mol/L NaCl溶液。
①实验需要玻璃棒、胶头滴管、烧杯、量筒外,还需要的玻璃仪器是____________。
②配制上述溶液,需要4.0 mol/L NaCl溶液_________mL。
③配制过程中出现以下情况,使所配溶液浓度偏低_____________。
A.溶液转移后没有洗涤烧杯和玻璃棒。 B.定容时仰视容量瓶的刻度线。
C. 未冷却即进行转移、定容操作。 D.容量瓶中原有少量蒸馏水
E.如果加水超过了刻度线,取出溶液使液面恰好到刻度线。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用SCR技术可有效降低柴油发动机NOx排放。SCR工作原理为尿素[CO(NH2)2]水溶液热分解为NH3和CO2,再利用NH3转化NOx,装置如图所示,下列说法不正确的是( )

A.转化NO2过程的化学方程式为:8NH3+6NO2![]() 7N2+12H2O
7N2+12H2O
B.转化器工作过程中,当转移0.6mol电子时,会消耗4.48LNH3
C.尿素水溶液热分解反应不属于氧化还原反应
D.该装置转化NO时,还原剂与氧化剂物质的量之比为2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的含有Al3+、Mg2+、Ba2+的混合溶液中逐滴加入NaOH和Na2SO4的混合溶液(除上述离子外,其他离子不与所加试剂反应,假设Al3+、Mg2+结合OH-的能力相同),产生沉淀的物质的量与所加溶液的体积的关系如图所示。下列说法正确的是:
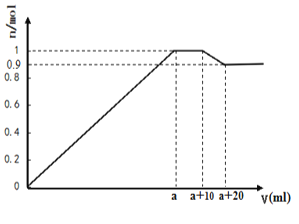
A. 当a<V<a+10时,不再生成难溶物
B. 上述含Al3+、Mg2+、Ba2+的混合溶液中3c(Al3+)+2c(Mg2+)=c(Ba2+)
C. 上述含Al3+、Mg2+、Ba2+的混合溶液中n(Al3+) = 0.2mol
D. NaOH和Na2SO4的混合溶液中c(NaOH)>c(Na2SO4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O是一种氧气吸收剂,为红棕色晶体,易被氧化,难溶于冷水,易溶于酸。其制备装置及步骤如下:
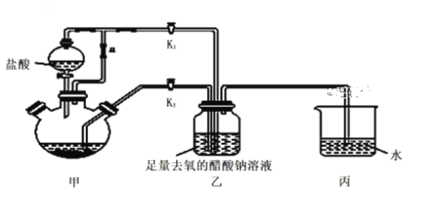
①检查装置气密性后,往三颈烧瓶中依次加入过量锌粒、适量CrCl3溶液。
②关闭K2,打开K1,旋开分液漏斗的旋塞并控制好滴速。
③待三颈烧瓶内的溶液由深绿色(Cr3+)变为亮蓝色(Cr2+)时,将溶液转移至装置乙中,当出现大量红棕色晶体时,关闭分液漏斗的旋塞。
④将装置乙中混合物快速过滤、洗涤和干燥,称量得到3.76 g [Cr(CH3COO)2]2·2H2O
(1)三颈烧瓶中的Zn与盐酸生成H2的作用____________,还发生的另一个反应的离子方程式为______________。
(2)实现步骤③中溶液自动转移至装置乙中的实验操作为______________,当乙中析出红棕色沉淀,为使沉淀充分析出并分离,需采用的操作是___________ 、_________、洗涤、干燥。
(3)装置丙中导管口水封的目的是______________。
(4)若实验所取用的CrCl3溶液中含溶质6.34 g,则[Cr(CH3COO)2]2·2H2O (相对分子质量为376)的产率是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.12 g铁粉加入25 mL 2 mol·L-1的氯化铁溶液中,充分反应后,其结果是
A. 铁粉有剩余,溶液呈浅绿色,Cl-基本保持不变B. Fe2+和Fe3+物质的量之比为5∶1
C. 往溶液中滴入无色KSCN溶液,显红色D. 氧化产物和还原产物的物质的量之比为2∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有BaCl2和NaCl的混合溶液aL,将它均分成两份,一份滴加稀硫酸,使Ba2+完全沉淀,另一份滴加AgNO3,使Cl-完全沉淀,反应中消耗xmol H2SO4、ymol AgNO3。据此得知原溶液中c(Na+)/mol·L -1为( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐不仅是日常生活的必需品,也是重要的化工原料。工业上通过海水硒盐得到粗产品再进行精制以获得纯NaCl,精制过程如图所示:

提供的试剂:Na2CO3溶液,NaOH溶液,BaCl2溶液。
粗盐产品中含有的杂质主要有硫酸盐和MgCl2、CaCl2。
(1)欲除去溶液Ⅰ中的Ca2+、Mg2+、SO42-离子,“一系列操作”中滴加试剂的先后顺序为___、NaOH、____。(填化学式)
(2)加入碳酸钠可以除去溶液中的___(填化学式,下同)和过量的___。写出Na2CO3发生反应的两个化学方程式:___,___。
(3)加入过量盐酸的作用是___。
(4)写出盐酸参与反应的化学方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com