
【题目】下列装置或操作能达到实验目的的是

A.①②B.③④C.②③④D.①②③④
【答案】B
【解析】
①从碘水中分离碘单质,应该使用萃取的方法,并选用CCl4或苯作萃取剂,故①错误;
②铜与稀硝酸反应生成NO,NO与空气中的氧气反应生成NO2,且NO与空气密度相差较小,所以不能用排空气法收集NO,故②错误;
③铁生锈要有空气和一定的湿度才行,在水里和盐溶液里面除了满足上述两个条件以外,还有加速铁生锈的另一个重要因素电解质,由于电解质的存在会大大加快生锈的速度,含量越高就越快,食盐水是电解质,电解质加速铁生锈的速度,根据右面红墨水液面的变化可证明铁生锈空气参与反应,能达到目的,故③正确;
④检查装置气密性可以采取“注水法”:首先关闭排气导管,从顶部漏斗口注水,当漏斗下端被水封闭后再注水,水面不下降,表明装置气密性好;如果水面下降,表明装置气密性差,能达到目的,故④正确;
能达到实验目的的是③④,答案选B。


 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,其中的编号代表对应的元素。
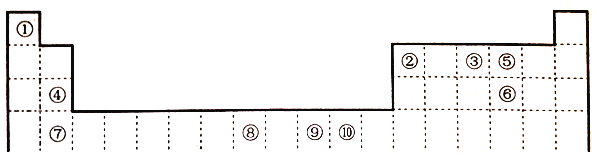
请回答:
(1)在周期表给出的10种元素中,电负性最小的元素基态原子的电子排布式为_____。
(2)在周期表给出的10种元素中,最外层未成对电子数与最外层成对电子数的个数比为3:2的元素与短周期最外层没有未成对电子数的元素形成的化合物是______(填化学式),所含化学键类型是_________。
(3)关于元素①与元素⑤形成的1:1的化合物,下列说法正确的是_____(填字母序号)。
A.该化合物中的所有原子都满足最外层8电子稳定结构
B.该化合物分子中σ键和π键数目比为1:1
C.该化合物是由极性键和非极性键形成的极性分子
D.该化合物分子的空间构型为直线形
(4)在①与③形成的相对分子质量最小的化合物A中,元素③的杂化类型是_____,写出与化合物A互为等电子体的一种阳离子_______(填离子符号)。
(5)元素⑧的+3价化合物MCl3·6H2O有三种不同颜色的异构体,为探究MCl3溶液析出的暗绿色晶体的化学式,取0.010molMCl3·6H2O配成溶液,滴加足量AgNO3溶液,得到沉淀2.870g,该晶体的化学式为_______(填字母序号)。
A.[M(H2O)6]Cl3 B.[M(H2O)5Cl]Cl2·H2O C.[M(H2O)4Cl2]Cl·2H2O
(6)元素⑩与元素⑤形成一种化合物其晶胞结构如下图所示,该化合物的化学式为____,若该晶体密度为dg/cm3,晶胞参数为apm,则阿伏加德罗常数的值NA为______。
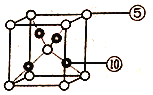
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是无机物A到M在一定条件下的转化关系(部分产物及反应条件未列出)。其中, I 是由第三周期元素组成的单质中,熔点最高的金属。K是一种红棕色气体。
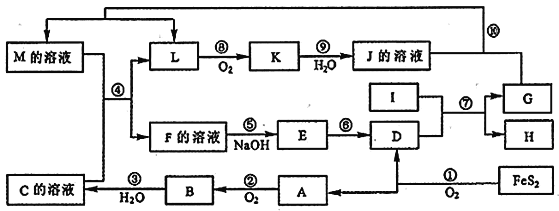
请回答下列问题
(1)M、F、E、G 四种物质中所含同一种元素,其名称是_____________。
(2)写出反应⑩(溶液 J + G)的离子反应方程式__________________________________。
(3)反应④中被还原的离子和被氧化的离子的物质的量之比是___________。
(4)向M的溶液中直接滴加 NaOH 溶液,现象是______________________,写出相应的化学方程式_____________________________,_______________________________。
(5)将化合物 D 与 KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂 K2FeO4(高铁酸钾),同时还生成 KNO2 和 H2O 。该反应的的化学方程式是___________________________。
(6)共有120 t 硫铁矿(FeS2)参与反应①冶炼化合物D,最终得到化合物D共16 t,则冶炼D的转化率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2,一元弱酸)和氟硼酸(HBF4)均可用于植物杀菌。常温时,有1 mol L-1的H3PO2溶液和1 mol˙L-1的HBF4溶液,两者起始时的体积均为V0,分别向两溶液中加水,稀释后溶液的体积均为V,两溶液的pH变化曲线如图所示.下列说法错误的是:
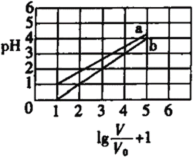
A.常温下,该HBF4溶液满足pH=![]()
B.常温下,H3PO2的电离平衡常数约为1.1![]() 10-2
10-2
C.常温下,NaBF4溶液的pH=7
D.NaH2PO2溶液中:c(OH-)-c(H+) =c(H3PO2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的各图中,表示2A(g)+B(g)2C(g)(△H<0)这个可逆反应的正确图象为(注:(C)表示C的质量分数,P表示气体压强,C表示浓度)
A.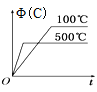 B.
B.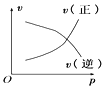 C.
C.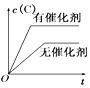 D.
D.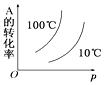
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯和乙烷的混合气体共amol,与bmol氧气共存于一密闭容器中,点燃后乙烯和乙烷充分燃烧,得到一氧化碳和二氧化碳的混合气体和45g水。
(1)一氧化碳和二氧化碳的混合气体总物质的量是_____,生成水的物质的量是____。
(2)当a=1时,乙烯和乙烷的物质的量之比是________。
(3)当a=1,且反应后一氧化碳和二氧化碳混合气体的物质的量是反应前氧气的2/3时,则b等于______,得到的一氧化碳和二氧化碳的物质的量之比是_____。
(4)a的取值范围是________,b的取值范围是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。

下列说法不正确的是
A. 电流从右侧电极经过负载后流向左侧电极
B. 为使电池持续放电,离子交换膜需选用阴离子交换膜
C. 电极A极反应式为:2NH3-6e-=N2+6H+
D. 当有4.48LNO2(标准状况) 被处理时,转移电子为0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃下,部分弱酸的电离常数如表。下列有关说法正确的是
弱酸 | HCOOH | HClO | H2S |
电离平衡 常数(Ka) | Ka=1.0×10-4 | Ka=2.0×10-8 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
A.相同浓度的HCOOH和HClO溶液的pH后者小
B.若HCOONa和HCOOH的混合溶液的pH=3,则![]() =10
=10
C.任何浓度NaHS溶液中总存在:c(Na+)+c(H+)=c(OH-)+c(HS-)
D.向NaClO溶液中通入H2S发生的反应为2ClO-+H2S===S2-+2HClO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com