
【题目】25 ℃下,部分弱酸的电离常数如表。下列有关说法正确的是
弱酸 | HCOOH | HClO | H2S |
电离平衡 常数(Ka) | Ka=1.0×10-4 | Ka=2.0×10-8 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
A.相同浓度的HCOOH和HClO溶液的pH后者小
B.若HCOONa和HCOOH的混合溶液的pH=3,则![]() =10
=10
C.任何浓度NaHS溶液中总存在:c(Na+)+c(H+)=c(OH-)+c(HS-)
D.向NaClO溶液中通入H2S发生的反应为2ClO-+H2S===S2-+2HClO
科目:高中化学 来源: 题型:
【题目】在1 L恒容密闭容器中投入足量Mg(NO3)2,在一定温度下发生下列反应:2Mg(NO3)2(s)![]() 2MgO(s)+4NO2(g)+O2(g)。能说明该反应达到平衡状态的是
2MgO(s)+4NO2(g)+O2(g)。能说明该反应达到平衡状态的是
A.NO2消耗速率与O2生成速率之比为4∶1B.NO2体积分数不再变化
C.混合气体的平均相对分子质量不再变化D.MgO的浓度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 2SiHCl3(g)![]() SiH2Cl2(g) + SiCl4(g)在催化剂作用下,于 323 K 和 343 K 时充分反应,SiHCl3 的转化率随时间变化的结果如图所示:
SiH2Cl2(g) + SiCl4(g)在催化剂作用下,于 323 K 和 343 K 时充分反应,SiHCl3 的转化率随时间变化的结果如图所示:
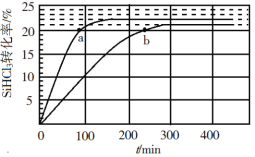
下列说法不正确的是
A.343 K 时反应物的平衡转化率为 22%
B.a、b 处反应速率大小:va>vb
C.要提高 SiHCl3 转化率,可采取的措施是降温和及时移去反应产物
D.已知反应速率![]() ,k正、k逆分别为正、逆反应速率常数,x为物质的量分数,则 343 K 时
,k正、k逆分别为正、逆反应速率常数,x为物质的量分数,则 343 K 时 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某研学小组的兴趣。“修旧如旧”是文物保护的主旨。
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有Cu和_______。
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈和有害锈,结构如图所示:
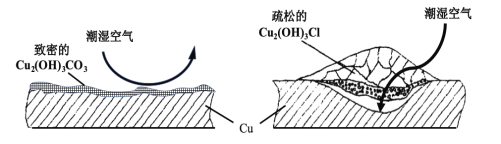
Cu2(OH)2CO3和Cu2(OH)3Cl分别属于无害锈和有害锈,请解释原因_____________。
(3)文献显示有害锈的形成过程中会产生CuCl(白色不溶于水的固体),请结合下图回答:
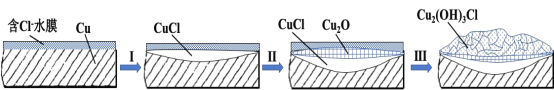
① 过程Ⅰ的正极反应物是___________。
② 过程Ⅰ负极的电极反应式是_____________。
(4)青铜器的修复有以下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法:
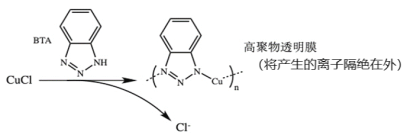
请回答下列问题:
①写出碳酸钠法的离子方程式___________________。
②三种方法中,BTA保护法应用最为普遍,分析其可能的优点有___________。
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的Cl-,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是极易溶于水的气体,常温常压下,1体积水大约能溶解700体积的氨气。
(1)实验室可在浓氨水中加入固体NaOH快速制取氨气,请用化学平衡移动原理简述原因_______________________________________________________________。
(2)甲、乙两瓶氨水的浓度分别为1mol·L-1和0.1mol·L-1,则甲、乙两瓶氨水中c(OH-)之比________(填“>”、“<”或“=”)10。
(3)向10mL0.1 mol/L的氨水中逐滴加入20mL 0.1 mol/L的醋酸,溶液导电性的变化是__________________(填“增大”、“减小”或“不变”)。写出二者反应的离子方程式:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取100.0 mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到16.84g沉淀,用过量稀硝酸处理后沉淀质量减少至6.99g,同时溶液中有气泡产生。试求:
(1)原混合液中Na2SO4的物质的量浓度为_____;
(2)产生的气体在标准状况下的体积为多少__________?(要求写出计算过程,只写结果不给分)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温25℃时,下列溶液里微粒间物质的量浓度的关系中正确的是( ):
A. 浓度0.1mol/L的NH4HSO3溶液:c(NH4+)+ c(H+)= c(OH-)+ c(HSO3-)+ c(SO32-)
B. 等体积等浓度Na2S和NaHS混合液:c(Na+)>c(S2-)>c(HS-)>c(OH-)>c(H+)
C. 将0.2mol/LNH3·H2O与0.1mol/LHCl等体积混合:c(Cl-)>c(NH4+)>c(NH3·H2O)>c(OH-)>c(H+)
D. 在0.1mol/L的Na2CO3溶液中:c (OH-)=c(H+)+ c(HCO3-)+2c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】托特罗定M合成路径如下(反应条件已略去):

已知信息:① (不稳定)
(不稳定)
②
③G遇![]() 溶液显紫色,H中含有3个六元环
溶液显紫色,H中含有3个六元环
请回答:
(1)M的分子式是__________,化合物K的结构简式是______________。
(2)下列说法正确的是__________
A.化合物B转化为C是消去反应,F转化为G是取代反应
B.化合物C转化为D的反应及F转化为G的反应都只需加入强碱后水解即可
C.![]() 化合物I与
化合物I与![]() 反应,最多消耗
反应,最多消耗![]()
D.等物质的量的A和D完全燃烧消耗的氧气量相等
(3)写出![]() 的化学方程式:__________________.
的化学方程式:__________________.
(4)M的同系物![]() 有多种同分异构体,同时符合下列条件的同分异构体的结构简式如
有多种同分异构体,同时符合下列条件的同分异构体的结构简式如 ,请再写出3种:____________________。
,请再写出3种:____________________。
①分子中含有2个独立的苯环;
②![]() 谱和
谱和![]() 谱检测显示分子中有5种化学环境不同的氢原子,有
谱检测显示分子中有5种化学环境不同的氢原子,有![]() 键,无
键,无![]() 键和
键和![]() 键。
键。
(5)设计以甲苯和乙酸酐( )为原料制备D肉桂酸(
)为原料制备D肉桂酸( )的合成路线(无机试剂任选,合成中须用到上述已知信息①②.用流程图表示):__________________________________________________________
)的合成路线(无机试剂任选,合成中须用到上述已知信息①②.用流程图表示):__________________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com