
【题目】硫元素的几种化合物存在下列转化关系:
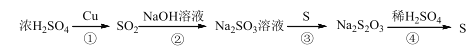
下列判断正确的是
A.反应①中生成的SO2具有还原性,故可作漂白剂
B.反应④中当消耗1mol稀硫酸时,电子转移为6mol
C.可以用CS2清洗做过实验③后附着在试管壁上的硫
D.反应④生成S的原子利用率是100%
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】如下图所示,向A、B中均充入1mol X、l mol Y,起始时A、B的体积都等于1L。在同温、同压和催化剂存在的条件下,关闭活塞K,使两容器中都发生下述反应:X(g)+Y(g) ![]() 2Z(g)+W(g) ΔH <0,达平衡时,A的体积为1.4L。下列说法错误的是( )
2Z(g)+W(g) ΔH <0,达平衡时,A的体积为1.4L。下列说法错误的是( )

A. 两容器中的反应分别达到平衡时,反应物X的速率:v(B)>v(A)
B. A容器中X的转化率为80%
C. 平衡时两容器的压强:PA<PB
D. 平衡时Y的体积分数:A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知汽车尾气无害化处理反应为2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)。下列说法正确的是
N2(g)+2CO2(g)。下列说法正确的是
A.升高温度可使该反应的逆反应速率降低
B.达到化学平衡时,化学反应已经停止
C.v正(NO)=v正(CO2)时,说明达到了化学平衡
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,用0.0200mol/L稀盐酸滴定20.00mL0.0200mol/LNaY溶液,溶液中水的电离程度随所加稀盐酸的体积变化如图所示(忽略滴定过程中溶液的体积变化),则下列有关说法正确的是
已知:K(HY)=5.0×10-11

A. 可选取酚酞作为滴定指示剂 B. M点溶液的pH>7
C. 图中Q点水的电离程度最小,Kw<10-14 D. M点,c(Na+)=c(HY)+c(Y-)+c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NiCl2是化工合成中最重要的镍源,在实验室中模拟工业上以金属镍废料(含Fe、Al等杂质)为原料生产NiCl2的工艺流程如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Ni(OH)2 |
开始沉淀的pH | 2.1 | 6.5 | 3.7 | 7.1 |
沉淀完全的pH | 3.3 | 9.7 | 4.7 | 9.2 |
(1)为了提高镍元素的浸出率,在“酸浸”时可采取的措施有__________(写一条即可)。
(2)加入H2O2时发生主要反应的离子方程式为__________。
(3)“调pH”时,控制溶液pH的范围为__________。
(4)“沉镍”过程中,若滤液A中c(Ni2+)=1.0mol/L,欲使100mL该滤液中的Ni2+沉淀完全[即溶液中c(Ni2+)≤1.0×10-5],则需用托盘天平称取Na2CO3固体的质量至少为_____g。(已知Ksp(NiCO3)=6.5×10-6,忽略溶液体积的变化)
(5)流程中由溶液得到NiCl2·6H2O的实验操作步骤依次为______、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,反应2HI(g)![]() H2(g)+ I2(g)(正反应吸热)达到平衡时,要使混合气体的颜色加深,可采取的措施是: ①增大氢气的浓度 ②升高温度 ③降低温度 ④缩小体积 ⑤增大HI的浓度 ⑥减小压强
H2(g)+ I2(g)(正反应吸热)达到平衡时,要使混合气体的颜色加深,可采取的措施是: ①增大氢气的浓度 ②升高温度 ③降低温度 ④缩小体积 ⑤增大HI的浓度 ⑥减小压强
A. ①③⑥ B. ③⑤⑥ C. ①③⑤ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是( )
A.标准状况下,22.4L二氯甲烷的分子数约为NA
B.乙烯和丙烯组成的42g混合气体中含碳原子数为6NA
C.1mol甲醇完全燃烧生成CO2和H2O,转移的电子数目为12NA
D.将1molCH3COONa溶于稀醋酸中溶液呈中性,溶液中CH3COO-数目等于NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: (1)Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
![]() 则
则![]() 的ΔH是( )
的ΔH是( )
A.-824.4 kJmol-1B.-627.6kJmol-1C.-744.7kJmol-1D.-169.4kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄鸣龙是我国著名化学家,利用“黄鸣龙反应”合成一种环己烷衍生物的路线如下:

已知:①R—Cl![]() R—COOH
R—COOH
②![]()
![]() R1CH2R2
R1CH2R2
③RCOOR1+R2CH2COOR3 ![]()
 +R1OH
+R1OH
(1)A 可与NaHCO3 溶液反应,其结构简式是____________。B 中含有的官能团是─COOH 和______________。
(2)D 的结构简式是_______________。
(3)D→E 反应会生成副产物 Y(分子式为 C17H32O6),生成 Y 的化学方程式是_______。
(4)E→F 为两步连续氧化反应,中间产物 X 可发生银镜反应,X 的结构简式是____。
(5)H 的结构简式是________________。
(6)I 的分子式为 C5H8O2,能使Br2 的 CCl4 溶液褪色,H→J 的反应类型是________。
(7)由K 经两步反应可得到化合物 M,转化路线如下:
![]()
环己烷的空间结构可如图1或图2表示,请在图3中将M 的结构简式补充完整:____________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com