
| 11.65g |
| 233g/mol |
| 0.05mol×22.4lL/mol |
| 100L |
| 11.65g |
| 233g/mol |
| 0.05mol×22.4lL/mol |
| 100L |


科目:高中化学 来源: 题型:
| A、元素X、M可形成既含离子键又含共价键的化合物 |
| B、气态氢化物的稳定性:Z<W |
| C、Y元素在自然界中以化合物的形式存在 |
| D、W元素的含氧酸都属于强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
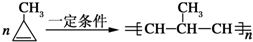 ;
; .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
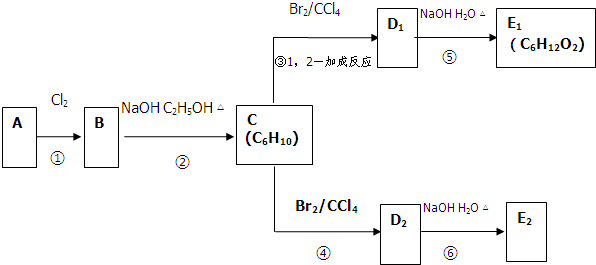
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
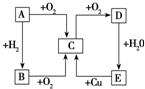 如图所示,A、B、C、D、E五种物质的相互转化关系
如图所示,A、B、C、D、E五种物质的相互转化关系查看答案和解析>>
科目:高中化学 来源: 题型:
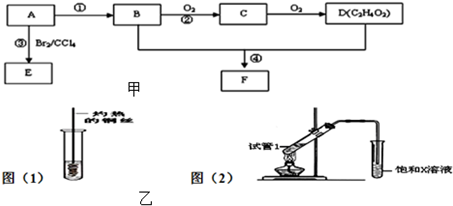
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com