
【题目】甲醇是一种可再生能源,具有广阔的开发和应用前景,可用Pt/Al2O3、Pd/C、 Rh/SiO2等作催化剂,采用如下反应来合成甲醇:2H2 (g)+CO(g)CH3OH(g)
(1)下表所列数据是各化学键的键能,该反应的ΔH=_______(用含字母的代数式表示)。
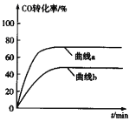
(2)某科研小组用Pd/C作催化剂,在450℃时,研究了n(H):n(CO)分别为2:1、3:1时CO转化率的变化情况(如图),则图中表示n(H2):n(CO)=3:1的变化曲线为______(填“曲线a"或“曲线b”)。
(3)某化学研究性学习小组模拟工业合成甲醇的反应,在2L的恒容密闭容器内充入1 mol CO和2molH2,加入合适催化剂后在某温度下开始反应,并用压力计监测容器内压强的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
则从反应开始到20min时,CO的平均反应速率为________,该温度下的平衡常数K为_______.
(4)将CO和H2加入密闭容器中,在一定条件下发生反应:CO(g)+2H2(g) CH3OH(g) ΔH<0。平衡时CO的体积分数(%)与温度和压强的关系如下图所示(虚线框表示没有测定该条件下的数据)。
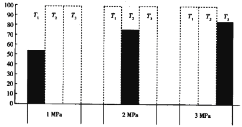
T1、T2、T3由大到小的关系是_________,判断理由是____________
(5)美国的两家公司合作开发了多孔硅甲醇直接燃料电池,其工作原理如图
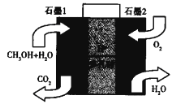
①石墨2为__________ (填“正“或“负“)极。
②石墨1极发生的电极反应式为________
【答案】(2a+b-3c-d-e)kJ·mol-1 曲线a 0.0125mol·L-1·min-1 4 T3>T2>T1 压强越大,CO的体积分数越小,T1、T2、T3对应的CO的体积分数逐渐增大,该反应向左移动,则T3>T2>T1 正 CH3OH+H2O-6e-=CO2↑+6H+
【解析】
(1)反应热ΔH=反应物的键能和生成物键能和;
(2)n(H2):n(CO)越大,CO的转化率越大;
(3)反应进行到20min时达到平衡,在恒温恒容容器中压强与气体的物质的量成正比,起始时总物质的量为3mol,压强为12.6MPa,平衡时压强为8.4MPa,则平衡时总物质的量为3mol![]() =2mol,设反应中参加反应的CO的物质的量为xmol,则:
=2mol,设反应中参加反应的CO的物质的量为xmol,则:
2H2 (g)+CO(g)CH3OH(g)
起始物质的量(mol) 2 1 0
变化物质的量(mol) 2x x x
平衡物质的量(mol) 2-2x 1-x x
故(2-2x)+(1-x )+x=2,解得x=0.5,再根据速率公式和平衡常数表达式计算即可;
(4)图示中压强越大,CO的体积分数越小,且CO(g)+2H2(g) ≒CH3OH(g) ΔH<0温度升高平衡逆向移动,CO的体积分数越大;
(5)由甲醇燃料电池工作原理可知,石墨2通入O2,发生还原反应生成H2O,而原电池的正极发生还原反应,则石墨1为原电池的负极,发生氧化反应,甲醇被氧化生成CO2;
(1)已知反应热ΔH=反应物的键能和-生成物键能和,则2H2 (g)+CO(g)CH3OH(g)的反应热ΔH=(2a+b)kJ/mol-(3c+d+e)kJ/mol=(2a+b-3c-d-e)kJ·mol-1;
(2)n(H2):n(CO)越大,CO的转化率越大,故曲线a表示n(H2):n(CO)=3:1的变化曲线;
(3)反应进行到20min时达到平衡,在恒温恒容容器中压强与气体的物质的量成正比,起始时总物质的量为3mol,压强为12.6MPa,平衡时压强为8.4MPa,则平衡时总物质的量为3mol![]() =2mol,设反应中参加反应的CO的物质的量为xmol,则:
=2mol,设反应中参加反应的CO的物质的量为xmol,则:
2H2 (g)+CO(g)CH3OH(g)
起始物质的量(mol) 2 1 0
变化物质的量(mol) 2x x x
平衡物质的量(mol) 2-2x 1-x x
故(2-2x)+(1-x )+x=2,解得x=0.5,
则从反应开始到20min时,CO的平均反应速率为 =0.0125mol·L-1·min-1;
=0.0125mol·L-1·min-1;
该温度下的平衡常数K=![]() =
=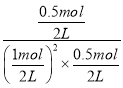 =4;
=4;
(4)已知CO(g)+2H2(g) CH3OH(g) ΔH<0,平衡时温度升高平衡逆向移动,CO的体积分数增大,由图示可知压强越大,CO的体积分数越小,T1、T2、T3对应的CO的体积分数逐渐增大,该反应向左移动,则T3>T2>T1;
(5)①石墨2通入O2,发生还原反应生成H2O,而原电池的正极发生还原反应,则石墨2为正极;
②石墨1为燃料电池的负极,甲醇被氧化生成CO2,发生的电极反应式为CH3OH+H2O-6e-=CO2↑+6H+。


科目:高中化学 来源: 题型:
【题目】三氯化硼(BCl3)是一种重要的化工原料。实验室制备BCl3的原理B2O3+3C+3Cl2 =2BCl3+3CO,某实验小组利用干燥的氯气和下列装置(装置可重复使用)制备BCl3并验证反应中有CO生成。(已知:BCl3的熔点为-107.3℃,沸点为12.5℃;硝基苯的密度比水大。)请回答下列问题:

实验Ⅰ:制备BCl3并验证产物CO
(1)该实验装置中合理的连接顺序为G→___→___→__→__→F→D→I;其中装置E的作用是______。
(2)BCl3接触潮湿空气时会形成白雾,请写出该反应的化学方程式____。
(3)能证明反应中有CO生成的现象是_____。
实验Ⅱ:产品中氯含量的测定
①准确称取少许m克产品,置于蒸馏水中完全水解,并配成100mL溶液。
②取10.00mL溶液于锥形瓶中
③加入V1mL浓度为C1 mol/LAgNO3溶液使氯离子完全沉淀;向其中加入少许硝基苯用力摇动。
④以硝酸铁为指示剂,用C2 mol/L KSCN标准溶液滴定过量的AgNO3溶液。重复步骤②~④二次,达到滴定终点时用去KSCN溶液的平均体积为V2mL。
已知:Ksp(AgCl)>Ksp(AgSCN)。
(4)步骤②移取溶液时所需仪器名称为____,步骤④中达到滴定终点的现象为_____。
(5)产品中氯元素的质量分数为_______。
(6)下列操作,可能引起测得产品中氯含量偏高是_____。
A.步骤③中未加硝基苯
B.步骤①中配制100mL溶液时,定容时俯视刻度线
C.用KSCN溶液滴定剩余AgNO3溶液时,滴定前有气泡,滴定后无气泡
D.滴定剩余AgNO3溶液时,KSCN溶液滴到锥形瓶外面一滴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B的产量可以衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示(部分反应条件、产物省略):(已知 2R-CHO + O2→2R-COOH R为烃基)
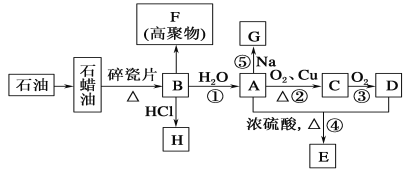
回答下列问题:
(1)①决定化合物A的化学特性的原子团的名称为________;F的结构简式为______________。
②B到A的反应类型为________,A到C的反应类型为________;
(2)写出下列反应的化学方程式:
反应②:______________________________________,
反应⑤:________________________________________。
(3)工业上制备H有以下两种方案:
Ⅰ.乙烷与氯气反应; Ⅱ.乙烯与氯化氢反应。
你认为最合理的方案是(填代号)________,理由是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度时,向2.0 L恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:2SO2(g)+O2(g) ![]() 2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t / s | 0 | 2 | 4 | 6 | 8 |
n(SO3) / mol | 0 | 0. 8 | 1. 4 | 1.8 | 1.8 |
下列说法正确的是
A. 反应在前2 s 的平均速率v(O2) = 0. 4 mol·L-1·s-1
B. 保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C. 相同温度下,起始时向容器中充入4 mol SO3,达到平衡时,SO3的转化率大于10%
D. 保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时n(SO3)/n(O2)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)一种熔融碳酸盐燃料电池原理示意如图:电池工作时,外电路上电流的方向应从电极___(“填A或B”)流向用电器。内电路中,CO32-向电极_____(“填A或B”)移动,电极A上CO参与的电极反应为______________________。

(2)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷和氧气构成燃料电池,则通入甲烷气体的电极是原电池的____极,该极的电极反应式是___________。如果消耗甲烷160g,假设化学能完全转化为电能,需要消耗标准状况下氧气的体积为_______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吡贝地尔(  )是多巴胺能激动剂,合成路线如下:
)是多巴胺能激动剂,合成路线如下:
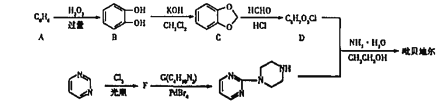
已知:①![]()
②D的结构简式为![]()
(1)A的名称是__________。
(2)E→F的反应类型是__________。
(3)G的结构简式为________;1molB最多消耗NaOH与Na的物质的量之比为_______。
(4)D+H→吡贝地尔的反应的化学方程式为_______。
(5)D的同分异构体中满足下列条件的有______种(碳碳双键上的碳原子不能连羟基),其中核磁共振氢谱有5种峰且峰面积之比为2:2:1:1:1的结构简式为_______(写出一种即可)。①与FeCl3溶液发生显色反应②苯环上有3个取代基③1mol该同分异构体最多消耗3molNaOH。
(6)已知:![]() ;参照上述合成路线,以苯和硝基苯为原料(无机试剂任选)合成
;参照上述合成路线,以苯和硝基苯为原料(无机试剂任选)合成![]() ,设计制备的合成路线:_______。
,设计制备的合成路线:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型镁-锂双离子二次电池如图,下列关于该电池的说法不正确的是

A. 放电时,Li+由左向右移动
B. 放电时,正极的电极反应式为Li1-xFePO4+xLi++xe-= LiFePO4
C. 充电时,外加电源的正极与Y相连
D. 充电时,导线上每通过1mol e-,左室溶液质量减轻12g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。
![]()
若A 是一种淡黄色固体单质.则C与H2O反应的生成物为______(填化学式)。
(2)Na2O2也是一种淡黄色固体,Na2O2与CO2反应生成O2和_______(填化学式)。
(3)写出在催化剂作用下N2与H2合成氨的化学方程式:_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com