
【题目】全球碳计划组织(GCP,The Global Carbon Project)报告称,2018年全球碳排放量约371亿吨,达到历史新高。
(1)中科院设计了一种新型的多功能复合催化剂,实现了CO2直接加氢制取高辛烷值汽油,其过程如图1所示。

①已知:CO2(g)+H2(g)=CO(g)+H2O(g) △H= + 41 kJ·mol-1
2CO2(g)+6H2(g)=4H2O(g)+CH2=CH2(g) △H= -128 kJ·mol-1
则上述过程中CO和H2转化为CH2=CH2的热化学方程式是_________。
②下列有关CO2转化为汽油的说法,正确的是___________________(填标号)。
A. 该过程中,CO2转化为汽油的转化率高达78%
B. 中间产物Fe5C2的生成是实现CO2转化为汽油的关键
C. 在Na-Fe3O4上发生的反应为CO2+H2=CO+H2O
D. 催化剂HZSM-5可以提高汽油中芳香烃的平衡产率
③若在一容器中充入一定量的CO2和H2,加入催化剂恰好完全反应,且产物只生成C5以上的烷烃类物质和水。则起始时CO2和H2的物质的量之比不低于_________。
(2)研究表明,CO2和H2在一定条件下可以合成甲醇。反应方程式为CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0。一定条件下,往2L恒容密闭容器中充入1.0molCO2和3.0molH2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化关系如图2所示。
CH3OH(g)+H2O(g) △H<0。一定条件下,往2L恒容密闭容器中充入1.0molCO2和3.0molH2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化关系如图2所示。
①该反应自发进行的条件是__________(填“高温”“低温”或“任意温度”)
②催化效果最佳的催化剂是__________(填“A”“B”或“C”);b点时,![]() ________
________![]() (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③若容器容积保持不变,则不能说明该反应达到化学平衡状态的是________。
a.c(CO2)与c(H2)的比值保持不变
b.v(CO2)正=v(H2O)逆
c.体系的压强不再发生变化
d.混合气体的密度不变
e.有lmolCO2生成的同时有断开3mol的H-H键
f.气体的平均相对分子质量不变
④已知容器内的起始压强为100 kPa,若图2中c点已达到平衡状态,则该温度下反应的平衡常数Kp =____________________(只列出计算式,不要求化简,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
【答案】2CO(g)+4H2(g)=CH2=CH2(g)+2H2O(g) H=-210kJmol-1 B 6:19 低温 A > ad 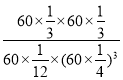
【解析】
根据已知热化学方程式运用盖斯定律书写新的热化学方程式;根据图示反应历程分析反应的中间产物,判断催化剂对反应的影响;根据烷烃的通式及题干信息进行相关计算;根据熵变和焓变判断反应是否自发进行;根据平衡状态的特征分析反应是否达到平衡状态;根据各物质的分压计算平衡常数。
(1)①已知:I CO2(g)+H2(g)=CO(g)+H2O(g) △H= + 41 kJ·mol-1,II 2CO2(g)+6H2(g)=4H2O(g)+CH2=CH2(g) △H= -128 kJ·mol-1,根据盖斯定律 II-I×2 得:2CO(g)+4H2(g)=CH2=CH2(g)+2H2O(g) △H=-128 kJ·mol-1-(+ 41 kJ·mol-1)×2=-210kJmol-1,故热化学方程式为:2CO(g)+4H2(g)=CH2=CH2(g)+2H2O(g) H=-210kJmol-1;
②A. 由图示分析78%并不是表示CO2转化为汽油的转化率,故A错误;
B. 中间产物Fe5C2是无机物转化为有机物的中间产物,是转化的关键,故B正确;
C. 根据图1所示,在Na-Fe3O4上发生的反应应为CO2生成CO的反应,氢气未参加反应,故C错误;
D. 催化剂HZSM-5的作用是加快反应速率,对平衡产率没有影响,故D错误;
故答案为:B;
③烷烃的通式为CnH(2n+2),假设只生成C6H14和水,则根据原子守恒知:6molCO2恰好完全反应生成1molC6H14和12molH2O需要的H2的物质的量为:![]() ,所以CO2和H2的物质的量之比不低于6mol:19mol=6:9,故答案为:6:9;
,所以CO2和H2的物质的量之比不低于6mol:19mol=6:9,故答案为:6:9;
(2)①该反应为放热反应,△H<0,根据方程式知:△S<0,根据ΔG=ΔH-TΔS,若ΔG<0则T较小,即低温时该反应自发进行,故答案为:低温;
②如图所示相同时间内催化剂A的转化率较高,说明反应较快催化效果好;b点时,还未达到平衡,则说明![]() >
>![]() ,故答案为:A;>;
,故答案为:A;>;
③a.c(CO2)与c(H2)初始时比值为1:3,所以按照化学计量数1:3反应后,比值始终保持不变,不能说明该反应达到平衡,故a选;
b.根据化学计量数之比知:v(CO2)正=v(H2O)正=v(H2O)逆,正逆反应速率相等,则说明已经达到平衡,故b不选;
c.该反应为气体减小的反应,所以当体系的压强不再发生变化,说明反应物和生成物浓度保持不变,能说明达到平衡状态,故c不选;
d.根据质量守恒原理知,反应前后总质量始终不变,且容器体积不变,则混合气体的密度始终不变,所以气体密度不变不能说明达到平衡,故d选;
e.断开3mol的H-H键时说明有3mol氢气消耗,则应该消耗1molCO2,则CO2的浓度保持不变,能说明达到平衡状态,故e不选;
f.反应前后气体的物质的量减小,质量保持不变,则气体的平均相对分子质量应增大,若不变,说明达到平衡状态,故f不选;
故答案为:ad;
④c点时CO2的转率为80%,则反应掉1mol×80%=0.8mol,

起始状态容器中气体总物质的量为1mol+3mol=4mol,平衡时容器中气体总物质的量为0.2mol+0.6mol+0.8mol+0.8mol=2.4mol,容器体积不变,起始压强为100 kPa,则平衡时总压强为:100kPa×![]() =60kPa,根据分压=总压×物质的量分数计算得:
=60kPa,根据分压=总压×物质的量分数计算得: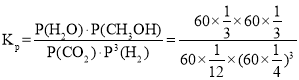 ,故答案为:
,故答案为: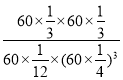 。
。


科目:高中化学 来源: 题型:
【题目】下列化学用语或分子结构模型表示正确的是
A.中子数为146、质子数为92的铀(U)原子![]()
B.四氯甲烷的球棍模型:![]()
C.乙烷的结构简式:CH3CH3
D.HClO的电子式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意图如下。下列有关该电池的说法正确的是( )
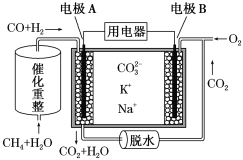
A.电池工作时,CO32-向电极B移动
B.电极B上发生的电极反应为O2+2CO2+4e-=2 CO32-
C.电极A上H2参与的电极反应为H2+2OH--2e-=2H2O
D.反应CH4+H2O 3H2+CO,每消耗1 mol CH4转移12 mol电子
3H2+CO,每消耗1 mol CH4转移12 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分离提纯、溶液的配制和分析是化学家常用的研究物质的实验方法,根据所学知识,回答下列问题:
Ⅰ.实验室从海藻中提取碘的流程如图:

(1)提取碘的过程中,操作③的名称为___。
(2)“后期处理”中涉及的操作为___。
(3)在灼烧过程中,使用到的实验仪器有___(除三脚架和酒精灯外)。
A.烧杯 B.蒸发皿 C.坩埚钳 D.瓷坩埚 E.泥三角
Ⅱ.依据粗盐提纯的原理,除去硝酸钾固体中少量的硝酸镁、硫酸镁杂质,按如图步骤操作,回答下列问题:

(1)试剂A和B的化学式分别是___,___。
(2)操作Ⅱ为___,___,___。
Ⅲ.实验室现需配制物质的量浓度为1mol/L的NaOH溶液480mL。
(1)实验过程中用到的玻璃仪器有:烧杯、玻璃棒、___、___。
(2)要配制此溶液,需要称量NaOH固体的质量为___。
(3)下列操作会使所配溶液浓度偏大的有___。
A.溶解固体溶质时,未冷却到室温即转入容量瓶定容
B.容量瓶中原有少量蒸馏水
C.定容时仰视读数
D.砝码生锈但未脱落
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,用![]() 滴定
滴定![]() 某一元酸HX,滴定过程中pH变化曲线如图所示。
某一元酸HX,滴定过程中pH变化曲线如图所示。

下列说法正确的是
A. HX溶液显酸性的原因是![]()
B. 点a,![]()
C. 点b,![]() 与
与![]() 恰好完全反应
恰好完全反应
D. 点c,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着氮氧化物对环境及人类活动影响的日趋严重,如何消除大气污染物中的氮氧化物成为人们关注的主要问题之一。
Ⅰ.利用NH3的还原性可以消除氮氧化物的污染,其中除去NO的主要反应如下:4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l) △H<0
5N2(g)+6H2O(l) △H<0
(1)写出一种可以提高NO的转化率的方法:__________
(2)一定温度下,在恒容密闭容器中按照n(NH3)︰n(NO) =2︰3充入反应物,发生上述反应。下列不能判断该反应达到平衡状态的是___________
A.c(NH3)︰c(NO) =2︰3 B.n(NH3)︰n(N2) 不变 C.容器内压强不变 D.容器内混合气体的密度不变 E.1molN—H键断裂的同时,生成1molO—H键
(3)已知该反应速率v正=k正·c4(NH3)·c6 (NO),v逆=k逆·cx(N2)·cy(H2O) (k正、k逆分别是正、逆反应速率常数),该反应的平衡常数K=k正/k逆,则x=_____,y=_______。
(4)某研究小组将2molNH3、3molNO和一定量的O2充入2L密闭容器中,在Ag2O催化剂表面发生上述反应,NO的转化率随温度变化的情况如图所示:

①在5min内,温度从420K升高到580K,此时段内NO的平均反应速率v(NO)=_______;
②在有氧条件下,温度580K之后NO生成N2的转化率降低的原因可能是___________。
Ⅱ.用尿素[(NH2)2CO]水溶液吸收氮氧化物也是一种可行的方法。NO和NO2不同配比混合气通入尿素溶液中,总氮还原率与配比关系如图。

(5)用尿素[(NH2)2CO]水溶液吸收体积比为1∶1的NO和NO2混合气,可将N元素转变为对环境无害的气体。写出该反应的化学方程式____。
(6)随着NO和NO2配比的提高,总氮还原率降低的主要原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸是一种二元弱酸,可用作还原剂、沉淀剂等。某校课外小祖的同学设计利用C2H2气体制取H2C2O42H2O。回答下列问题:
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用如图装置制取C2H2。

①电石与水反应很快,为了减缓反应速率,装置A中除用饱和食盐水代替水之外,还可以采取的措施是____________________________ (写一种即可)。
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为________________________。
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如图所示:

①装置D中多孔球泡的作用是______________________。
②装置D中生成H2C2O4的化学方程式为___________________________________。
③从装置D中得到产品,还需经过__________________(填操作名称)、过滤、洗涤及干燥。
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol/L酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定时高锰酸钾标准溶液盛放在滴定管中_____________(填“酸式”或“碱式”)。
②滴定过程中发现褪色速率开始很慢后逐渐加快,分析可能的原因是______________ 。
③产品中H2C2O4·2H2O的质量分数为_________________(列出含 m、c、V 的表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在一容积不变的密闭容器中,充入一定量HI气体,发生如下可逆反应:
2HI(g)![]() H2(g)+I2(g)ΔH>0。下列说法正确的是( )
H2(g)+I2(g)ΔH>0。下列说法正确的是( )
A.若每消耗2n mol HI的同时生成n mol H2,表明该反应已达平衡
B.容器内的压强不发生变化,表明该反应已达平衡
C.平衡时,若其他条件不变,再充入一定量HI,重新达平衡后,I2的百分含量增大
D.平衡时,若其他条件不变,升高温度,混合气体的颜色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用反应: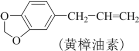
![]()
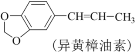
![]()
![]() 合成洋茉莉醛的流程如图所示。下列说法错误的是( )
合成洋茉莉醛的流程如图所示。下列说法错误的是( )
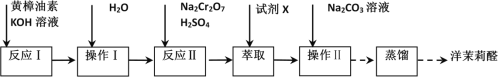
A.水洗的目的是除去KOH
B.试剂X应选用有机溶剂
C.黄樟油素和异黄樟油素互为同分异构体
D.进行蒸馏操作时可选用球形冷凝管
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com