
【题目】一种熔融碳酸盐燃料电池原理示意图如下。下列有关该电池的说法正确的是( )
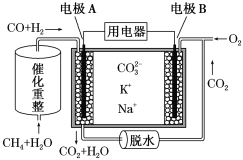
A.电池工作时,CO32-向电极B移动
B.电极B上发生的电极反应为O2+2CO2+4e-=2 CO32-
C.电极A上H2参与的电极反应为H2+2OH--2e-=2H2O
D.反应CH4+H2O 3H2+CO,每消耗1 mol CH4转移12 mol电子
3H2+CO,每消耗1 mol CH4转移12 mol电子
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】下面是合成药物格列卫的中间体J的一种合成路线:
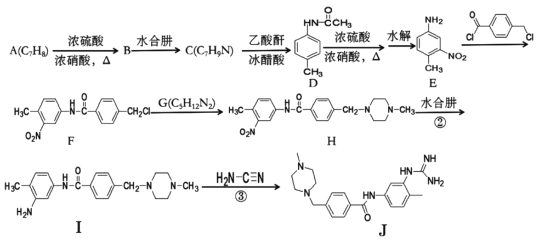
回答下列问题:
(1)A的名称为____,B的化学式为____。
(2)F中含氧官能团名称为____
(3)B→C和I→J的反应类型分别为____、____。
(4)G的结构简式为____。
(5)芳香化合物X是D的同分异构体,苯环上具有三个取代基且氨基与苯环直接相连,X能发生银镜反应,分子结构只有一个乙基,符合条件的X的结构式有____种。
(6)写出用甲苯、乙醇为原料制备对氨基苯甲酸乙酯的合成路线:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)利用如图装置,进行NH3与金属氧化物MxOy反应生成M、N2、H2O,通过测量生成水的质量来测定M的相对原子质量。a中试剂是浓氨水。

①仪器a的名称为_________,仪器b中装入的试剂可以是___________。
②按气流方向正确的装置连接顺序为_________(填字母,装置可重复使用)。
(2)亚硝酸钠是一种工业盐,在生产、生活中应用广泛。现用下图所示装置(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物成分。

已知:ⅰ.NO+NO2+2OH-=2NO2-+H2O
ⅱ.气体液化的温度:NO2(21℃)、NO(-152℃)
①反应前应打开弹簧夹,先通入一段时间氮气,目的是________________。
②为了检验装置A中生成的气体产物,仪器的连接顺序(从左向右连接):A→_________;组装好仪器后,接下来进行的操作是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学通过实验研究FeCl3溶液与Cu粉发生的氧化还原反应。实验记录如下:
序号 | I | II | III |
实验步骤 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
实验现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀 |
下列说法不正确的是
A. 实验I、II、III中均涉及Fe3+被还原
B. 对比实验I、II说明白色沉淀的产生与铜粉的量有关
C. 实验II、III中加入蒸馏水后c(Cu2+)相同
D. 向实验III反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室通常用图所示的装置来制取氨气。请按要求回答下列问题:
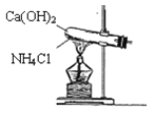
(1)实验室制取氨气的化学反应方程式为__。
(2)除了以上方法。下面也能用于制备氨气的是___。
①固态氯化铵加热分解
②浓氨水中加入固体氢氧化钠
③加热浓氨水
(3)NH3的催化氧化的化学反应方程式为__。
(4)①用装置A收集氨气时,应选择氨气的进气口是___(选填“a”或“b”),并说明选择的理由___。
②打开装置A中的止水夹,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是___、___。
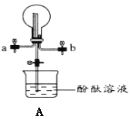
(5)通常可以用什么方法来检验无色溶液中是否有NH4+___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO 和 NO 是汽车尾气中的主要污染物,易引起酸雨、温室效应和光化学烟雾等环境污染问题。随着我国机动车保有量的飞速发展, 汽车尾气的有效处理变得迫在眉睫。其中的一种方法为2CO(g)+2NO(g)=N2(g)+2CO2(g),请回答下列问题:
(1)已知该反应为自发反应,则该反应的反应热△H ______0(填“>”或“<”或“=”)
(2)已知:N2 (g) + O2(g)=2NO(g) △H= a kJmol -1
C(s) + O2 (g)=CO2 (g) △H= b kJmol -1
2C(s) + O2 (g)=2CO(g) △H= c kJmol -1
则 2CO(g)+2NO(g)=N2 (g)+2CO2 (g) △H=______kJmol-1 (用含 a、b、c 的表达式表示)。
(3)一定温度下,将 a molCO、b molNO 充入一恒压真空密闭容器。已知起始压强为 c kPa,到达平衡时, 测得N2 的物质的量为 d mol,则:
①该温度此反应用平衡分压代替平衡浓度的平衡常数Kp=_____(用含 a、b、c、d 的式子表示)
②该条件下,可判断此反应到达平衡的标志是_____。
A.单位时间内,断裂 2n molC=0 同时形成 n mol N≡N
B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变
(4)某研究小组探究催化剂对 CO、NO 转化的影响。将 CO 和 NO 以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中 N2 的含量,从而确定尾气脱氮率(即 NO 的转化率),结果如图所示:
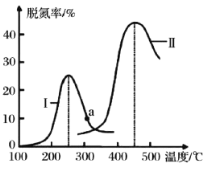
①由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为_____________。
②若低于 200℃,图中曲线 I 脱氮率随温度升高变化不大的主要原因为________。
(5)己知常温下, Kb(NH3·H 2O)=1.8×10-5,Ka1(H2CO3) =4.4×10-7,Ka2(H2CO3) =4.4×10-11。此温度下某氨水的浓度为 2mol/L,则溶液中c(OH-)= ____mol/L,将脱氮反应后生成CO2 通入氨水中使溶液恰好呈中性,则此时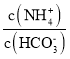 =____________(保留小数点后4位数字)
=____________(保留小数点后4位数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请用下图所示仪器装置设计一个包括电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。其中A是金属Fe,B是石墨电极。
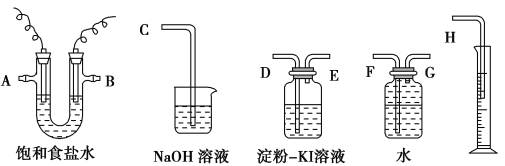
(1)所选仪器连接时,各接口的顺序是(填各接口的代号字母):A接______,________接______,B接________,________接________。
(2)实验时,装置中的石墨电极接电源的________极,所发生的电极反应式为_____________;铁电极接电源的________极,所发生的电极反应式为___________;
此电解总反应的离子方程式为________________________________。
(3)实验测得产生的氢气体积(已折算成标准状况)为5.60 mL,电解后溶液的体积恰好为50.0 mL,则溶液中OH—的浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.原子序数之差为2的两种元素不可能位于同一主族
B.D-核外有36个电子 ,则元素D位于第四周期第ⅦA族
C.位于同一主族相邻的甲、乙两种元素,甲的原子序数为![]() ,则乙的原子序数可能为
,则乙的原子序数可能为![]()
D.位于同一周期的甲、乙两种元素,甲位于第IIA族,原子序数为![]() ,乙位于第ⅢA族,则乙原子序数可能为
,乙位于第ⅢA族,则乙原子序数可能为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一块镁铝合金(不含其它物质)投入到50ml的稀盐酸溶液中,充分反应后,固体无剩余,向所得溶液中逐滴滴入cmol/LNaOH溶液时,得到沉淀的质量与所滴加NaOH溶液的体积有如图关系:
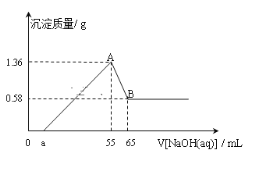
(1)图中B点表示沉淀的化学式为___;AB段发生反应的离子方程式为___。
(2)合金中金属铝的物质的量为___mol;
(3)稀盐酸溶液的浓度为___mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com