
【题目】CO 和 NO 是汽车尾气中的主要污染物,易引起酸雨、温室效应和光化学烟雾等环境污染问题。随着我国机动车保有量的飞速发展, 汽车尾气的有效处理变得迫在眉睫。其中的一种方法为2CO(g)+2NO(g)=N2(g)+2CO2(g),请回答下列问题:
(1)已知该反应为自发反应,则该反应的反应热△H ______0(填“>”或“<”或“=”)
(2)已知:N2 (g) + O2(g)=2NO(g) △H= a kJmol -1
C(s) + O2 (g)=CO2 (g) △H= b kJmol -1
2C(s) + O2 (g)=2CO(g) △H= c kJmol -1
则 2CO(g)+2NO(g)=N2 (g)+2CO2 (g) △H=______kJmol-1 (用含 a、b、c 的表达式表示)。
(3)一定温度下,将 a molCO、b molNO 充入一恒压真空密闭容器。已知起始压强为 c kPa,到达平衡时, 测得N2 的物质的量为 d mol,则:
①该温度此反应用平衡分压代替平衡浓度的平衡常数Kp=_____(用含 a、b、c、d 的式子表示)
②该条件下,可判断此反应到达平衡的标志是_____。
A.单位时间内,断裂 2n molC=0 同时形成 n mol N≡N
B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变
(4)某研究小组探究催化剂对 CO、NO 转化的影响。将 CO 和 NO 以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中 N2 的含量,从而确定尾气脱氮率(即 NO 的转化率),结果如图所示:
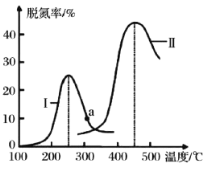
①由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为_____________。
②若低于 200℃,图中曲线 I 脱氮率随温度升高变化不大的主要原因为________。
(5)己知常温下, Kb(NH3·H 2O)=1.8×10-5,Ka1(H2CO3) =4.4×10-7,Ka2(H2CO3) =4.4×10-11。此温度下某氨水的浓度为 2mol/L,则溶液中c(OH-)= ____mol/L,将脱氮反应后生成CO2 通入氨水中使溶液恰好呈中性,则此时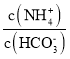 =____________(保留小数点后4位数字)
=____________(保留小数点后4位数字)
【答案】< 2b-a-c ![]() BC 催化剂 II,450℃ 温度较低时,催化剂 I 的活性偏低 6×10-3 1.0009
BC 催化剂 II,450℃ 温度较低时,催化剂 I 的活性偏低 6×10-3 1.0009
【解析】
(1)反应自发进行的判断依据为△H-T△S<0;
(2)根据盖斯定律,得到目标方程式的计算式为2×②-①-③,据此计算△H2;
(3)①根据Kp=![]() 计算平衡分压代替平衡浓度的平衡常数;
计算平衡分压代替平衡浓度的平衡常数;
②结合平衡的特征“等、定”及衍生的物理量判定平衡状态;
(4)①由图象的脱氮率观察适当反应条件;
②催化剂在低温下活性不大,反应随温度变化速率变化不大;
(5)NH3H2O的Kb=1.8×10-5,若氨水的浓度为2.0molL-1,可结合Kb=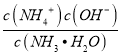 计算c(OH-),将CO2通入该氨水中,当溶液呈中性时溶液中c(OH-)=c(H+)=10-7mol/L,电荷守恒得到:c(NH4+)=c(HCO3-)+2c(CO32-),
计算c(OH-),将CO2通入该氨水中,当溶液呈中性时溶液中c(OH-)=c(H+)=10-7mol/L,电荷守恒得到:c(NH4+)=c(HCO3-)+2c(CO32-),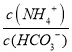 =1+
=1+![]() ,H2CO3的Ka2=4.4×10-11,结合Ka2=
,H2CO3的Ka2=4.4×10-11,结合Ka2=![]() 计算
计算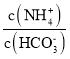 。
。
(1)反应 2NO(g)+2CO(g)2CO2(g)+N2(g)能够自发进行,反应△S<0,若满足△H-T△S<0,必须△H<0,故答案为:<;
(2)根据盖斯定律,得到目标方程式的计算式为2×②-①-③,代入a、b、c计算得△H=2b-a-c,
故答案为:2b-a-c;
(3)①根据三段式,
![]()
![]() n(起始)/mol
n(起始)/mol![]()
n(改变)/mol![]()
n(平衡)/mol![]()
平衡时,NO和CO的体积分数都等于![]() ,CO2的体积分数为
,CO2的体积分数为![]() ,N2的体积分数为
,N2的体积分数为![]() ,因为是恒压容器,故平衡时的总压也为c kPa,Kp=
,因为是恒压容器,故平衡时的总压也为c kPa,Kp=![]() =
= =
=![]() ,故答案为:
,故答案为:![]() ;
;
②A.单位时间内,断裂 2n molC=0 同时形成 n mol N≡N,正反应速率和逆反应速率不相等,不能说明达到平衡,故A错误;
B.该反应是气体分子数不相等的反应,混合气体的平均相对分子质量不再改变,可以说明达到平衡,故B正确;
C. 容器是恒压容器, 反应是气体分子数不相等的反应,混合气体的密度不再改变可以说明达到平衡,故C正确;
故答案为BC。
(4)①由图象可知,在催化剂 II,450℃条件下达到最大脱氮率,故答案为:催化剂 II,450℃;
②温度较低时,催化剂的活性偏低,反应速率慢,所以脱氮率随温度升高变化不大,故答案为:温度较低时,催化剂的活性偏低;
(5)NH3H2O的Kb=1.8×10-5,若氨水的浓度为2.0molL-1,由Kb=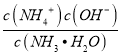 ,可知c(OH-)=
,可知c(OH-)=![]() mol/L=6×10-3mol/L,将CO2通入该氨水中,当溶液呈中性时溶液中c(OH-)=c(H+)=10-7mol/L,电荷守恒得到:c(NH4+)=c(HCO3-)+2c(CO32-),
mol/L=6×10-3mol/L,将CO2通入该氨水中,当溶液呈中性时溶液中c(OH-)=c(H+)=10-7mol/L,电荷守恒得到:c(NH4+)=c(HCO3-)+2c(CO32-),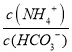 =1+
=1+![]() ,H2CO3的Ka2=4.4×10-11,结合Ka2=
,H2CO3的Ka2=4.4×10-11,结合Ka2=![]() 计算
计算![]() ,
,![]() =
=![]() =
=![]() ,
,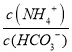 =1+
=1+![]() =1+
=1+![]() =1.0009,故答案为:6×10-3;1.0009。
=1.0009,故答案为:6×10-3;1.0009。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】金刚烷是一种重要的化工原料,工业上可通过下列途径制备:

下列说法正确的是
A.环戊二烯分子中所有原子可能共面
B.金刚烷的二氯代物有 6 种
C.二聚环戊二烯与 HBr 加成反应最多得 7 种产物
D.上述四种烃均能使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】属于加成反应的是
A.CH2=CH2 + Br2→CH2BrCH2Br
B.2CH3CH2OH + O2![]() 2CH3CHO + 2H2O
2CH3CHO + 2H2O
C.CH3COOH + CH3CH2OH![]() CH3COOCH2CH3 + H2O
CH3COOCH2CH3 + H2O
D.CH4 + 2O2![]() CO2 + 2H2O
CO2 + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热催化合成氨面临的两难问题是:采用高温增大反应速率的同时会因平衡限制导致 NH3 产率降低。我国科研人员研制了 Ti-H-Fe 双温区催化剂(Ti-H 区域和 Fe 区域的温度差可超过 100℃)。Ti-H-Fe 双温区催化合成氨的反应历程如图,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是

A.①为氮氮三键的断裂过程
B.①②③在高温区发生,④⑤在低温区发生
C.③为N 原子由 Fe 区域向 Ti-H 区域的传递过程
D.使用 Ti-H-Fe 双温区催化剂使合成氨反应转变为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意图如下。下列有关该电池的说法正确的是( )
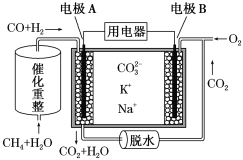
A.电池工作时,CO32-向电极B移动
B.电极B上发生的电极反应为O2+2CO2+4e-=2 CO32-
C.电极A上H2参与的电极反应为H2+2OH--2e-=2H2O
D.反应CH4+H2O 3H2+CO,每消耗1 mol CH4转移12 mol电子
3H2+CO,每消耗1 mol CH4转移12 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaNO3和Cu(NO3)2的混合溶液体积为500mL,测得其中c(NO3-)=6.0mol·L-1,用铂电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
A.电解得到铜的物质的量为0.5mol
B.上述电解过程中共转移2mol电子
C.原混合溶液中c(Na+)为2mol·L-1
D.电解后溶液中c(H+)为2mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁溶液和过量碳酸氢铵溶液混合,过滤、洗涤、干燥得到碳酸亚铁,在空气中灼烧碳酸亚铁得到铁的氧化物M。利用滴定法测定M的化学式,其步骤如下:
①称取3.92g样品M溶于足量盐酸,并配成100mL溶液A。
②取20.00mL溶液A于锥形瓶中,滴加KSCN溶液,溶液变红色;再滴加双氧水至红色刚好褪去,同时产生气泡。
③待气泡消失后,用1.0000 mol·L-1 KI标准溶液滴定锥形瓶中的Fe3+,达到滴定终点时消耗KI标准溶液10.00 mL。
(1)实验中必需的定量仪器有量筒、电子天平、____________和____________。
(2)在滴定之前必须进行的操作包括用标准KI溶液润洗滴定管、__________、___________。
(3)步骤②中“气泡”有多种可能,完成下列猜想:
①提出假设:
假设1:气泡可能是SCN-的反应产物N2、CO2、SO2或N2,CO2。
假设2:气泡可能是H2O2的反应产物____________,理由___________。
②设计实验验证假设1:
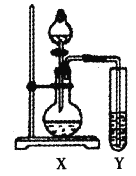
试管Y中的试剂是_______。
(4)根据上述实验,写出硫酸亚铁溶液和过量碳酸氢铵溶液混合制备碳酸亚铁的离子方程式_____。
(5)根据数据计算,M的化学式为_______。
(6)根据上述实验结果,写出碳酸亚铁在空气中灼烧的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个化学过程的示意图,回答下列问题:

(1)甲池是 装置,电极A的名称是 。
(2)甲装置中通入CH4的电极反应式为 ,乙装置中B(Ag)的电极反应式为 ,丙装置中D极的产物是 (写化学式),
(3)一段时间,当丙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃ 时的pH =__________。(已知:NaCl溶液足量,电解后溶液体积为500 mL)。
若要使丙池恢复电解前的状态,应向丙池中通入 (写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2通入足量的氢氧化钠溶液,温度不同时充分反应后产物溶液中除大量OH-外,还有Cl-、ClO-、ClO3-,已知:Cl2+OH-→Cl-+ClO-+H2O(冷碱)、Cl2+OH-→Cl-+ClO3-+H2O(热碱),并知ClO-、ClO3-离子的物质的量比为2:1,试问原混合气体中Cl2与反应后溶液中的Cl-物质的量之比为( )
A.2:5B.3:1C.1:1D.5:7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com