
【题目】下列说法正确的是( )
A.原子序数之差为2的两种元素不可能位于同一主族
B.D-核外有36个电子 ,则元素D位于第四周期第ⅦA族
C.位于同一主族相邻的甲、乙两种元素,甲的原子序数为![]() ,则乙的原子序数可能为
,则乙的原子序数可能为![]()
D.位于同一周期的甲、乙两种元素,甲位于第IIA族,原子序数为![]() ,乙位于第ⅢA族,则乙原子序数可能为
,乙位于第ⅢA族,则乙原子序数可能为![]()
【答案】B
【解析】
A、氢和锂两种元素原子序数之差为2是同一主族,原子序数之差为2的两种元素可能位于同一主族,故A选项错误。
B、D-核外有36个电子,则D原子有35个电子,为Br元素,Br位于第四周期第VIIA族,故B选项正确。
C. 同主族相邻两周期原子序数差值可能为2、8、18、32等,所以同一主族的甲乙两种元素,甲的原子序数为x,则乙的原子序数不可能为x+4,故C选项错误。
D. 第二周期,IIA族4号的Be---IIIA族元素5号的B,y可能等于x+1;第三周期,IIA族与IIIA族元素也相差1(因为没有副族元素);第四、五周期,IIA族与IIIA族元素相差11,y可能等于x+11 (因为出现副族元素)例如:20元素钙与31号元素镓;第六周期,IIA族与IIIA族元素相差25,y可能等于x+25 (因为出现镧系元素)例如:56号元素Ba与81号元素Tl,所以不可能为:x+19,故D选项错误。
故答案选B。


科目:高中化学 来源: 题型:
【题目】硫酸镍是电镀镍和化学镀镍时使用的主要镍盐。以废镍催化剂(主要成分为NiCO3和SiO2,还含有少量Fe2O3、Cr2O3)为原料制备硫酸镍晶体的流程如图所示:
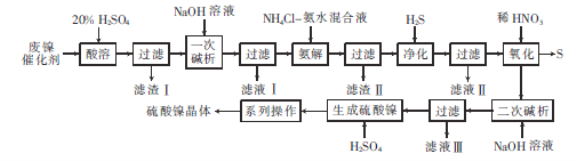
已知:Ni3+的氧化性比稀HNO3强。
回答下列问题:
(1)已知:Cr3++4OH-= CrO2-+2H2O。“一次碱析”时,需加入过量的NaOH溶液的目的是______________________。
(2)“氨解”的目的为_______________________。
(3)“净化”“过滤”后得到含有两种元素的不溶性化合物,该化合物的化学式为________,写出“氧化”中发生反应的离子方程式:____________________________________。
(4)从NiSO4溶液中得到硫酸镍晶体需经过“系列操作”为__________,__________,过滤,洗涤,干燥(填操作名称)。
(5)1844年,科学家发现金属镍可以用NaH2PO2将水溶液中的Ni2+还原出来,NaH2PO2将转化为H3PO3,这一原理现用于化学镀镍。写出化学镀镍原理的离子方程式___________。
(6)为测定硫酸镍晶体(NiSO4·n H2O)的组成,进行如下实验:称取2.63g样品,配成250.00mL溶液,准确量取配制的溶液25.00mL,用0.0400mol/L EDTA(Na2H2Y)标准溶液滴定Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00mL。则硫酸镍晶体的化学式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意图如下。下列有关该电池的说法正确的是( )
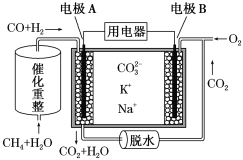
A.电池工作时,CO32-向电极B移动
B.电极B上发生的电极反应为O2+2CO2+4e-=2 CO32-
C.电极A上H2参与的电极反应为H2+2OH--2e-=2H2O
D.反应CH4+H2O 3H2+CO,每消耗1 mol CH4转移12 mol电子
3H2+CO,每消耗1 mol CH4转移12 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁溶液和过量碳酸氢铵溶液混合,过滤、洗涤、干燥得到碳酸亚铁,在空气中灼烧碳酸亚铁得到铁的氧化物M。利用滴定法测定M的化学式,其步骤如下:
①称取3.92g样品M溶于足量盐酸,并配成100mL溶液A。
②取20.00mL溶液A于锥形瓶中,滴加KSCN溶液,溶液变红色;再滴加双氧水至红色刚好褪去,同时产生气泡。
③待气泡消失后,用1.0000 mol·L-1 KI标准溶液滴定锥形瓶中的Fe3+,达到滴定终点时消耗KI标准溶液10.00 mL。
(1)实验中必需的定量仪器有量筒、电子天平、____________和____________。
(2)在滴定之前必须进行的操作包括用标准KI溶液润洗滴定管、__________、___________。
(3)步骤②中“气泡”有多种可能,完成下列猜想:
①提出假设:
假设1:气泡可能是SCN-的反应产物N2、CO2、SO2或N2,CO2。
假设2:气泡可能是H2O2的反应产物____________,理由___________。
②设计实验验证假设1:
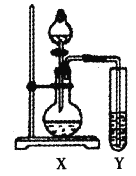
试管Y中的试剂是_______。
(4)根据上述实验,写出硫酸亚铁溶液和过量碳酸氢铵溶液混合制备碳酸亚铁的离子方程式_____。
(5)根据数据计算,M的化学式为_______。
(6)根据上述实验结果,写出碳酸亚铁在空气中灼烧的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】材料的不断发展可以促进社会进步。 完成下列填空:
(1) “玉兔”号月球车开创了我国月球表面探索的先河,其制备材料中使用了镁铝合金,选用镁铝合金的优点是____________________。(任写一点)
(2)光导纤维简称“光纤”,是一种由玻璃制成、能传输光线、结构特殊的玻璃纤维。现在家中的电话线和网线大都采用光纤线。光纤的主要成分是二氧化硅,二氧化硅的晶体类型是____________________。(单选)
a.金属晶体 b.离子晶体 c.原子晶体 d.分子晶体
(3)随着我国经济的快速发展,对电池新材料需求的不断增加,再加上手机、笔记本电脑、数码相机、摄像机、汽车等产品对新型、高效、环保电池材料的强劲需求,我国电池新材料市场将不断扩大。而铜锌原电池是一种最基本的将化学能转变为电能的装置,其中铜作________极,锌作_________极。
(4)塑料制品作为一种新型材料,具有质轻、防水、耐用、生产技术成熟、成本低的优点,在全世界被广泛应用且呈逐年增长趋势。乙烯通过加聚反应可以制成聚乙烯塑料,请写出聚乙烯的结构简式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个化学过程的示意图,回答下列问题:

(1)甲池是 装置,电极A的名称是 。
(2)甲装置中通入CH4的电极反应式为 ,乙装置中B(Ag)的电极反应式为 ,丙装置中D极的产物是 (写化学式),
(3)一段时间,当丙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃ 时的pH =__________。(已知:NaCl溶液足量,电解后溶液体积为500 mL)。
若要使丙池恢复电解前的状态,应向丙池中通入 (写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家发明了一种“可固氮”的锂氮二次电池,将可传递离子的醚类做电解质,电池的总反应(固氮过程)为6Li+N2=2Li3N。下列说法不正确的是( )
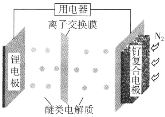
A.固氮时,阳极区发生反应Li-e-=Li+
B.脱氮过程,钌复合电极的电极反应:2Li3N-6e-=6Li++N2↑
C.醚类电解质可换成硫酸锂溶液
D.脱氮时,锂离子移向锂电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的一部分如图所示,W、X、Y、Z均为短周期主族元素,X与Z的最高正价之和与W的相等。下列说法错误的是
![]()
A.原子半径:X>Y>Z>W
B.X2W2中含有离子键和共价键
C.Y的最高价氧化物对应的水化物难溶于水
D.将由X、Z的单质组成的混合物放入冷水中,Z的单质不发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸金刚烷胺是一种治疗和预防病毒性感染的药物,可用于抑制病毒穿入宿主细胞,从结构上看是一种对称的三环状胺,可以利用环戊二烯(CPD)来制备合成,流程图如下:

(1)下列关于X和金刚烷说法正确的是_________
A.金刚烷和X互为同分异构体,均可以发生氧化反应和取代反应
B.金刚烷和X均可以使溴水褪色
C.金刚烷和X均具有与芳香烃相似的化学性质
D.金刚烷和X均不存在手性碳原子
(2)反应①的反应类型为____________,反应②的条件为________________。
(3)有机物Y的一氯代物的同分异构体的数目为___________,写出Y与氢氧化钠的乙醇溶液反应的化学方程式___________________________________。
(4)有机物Z是一种重要的有机氮肥,在核磁共振氢谱谱图中只有一个峰,写出Z与浓硫酸反应的化学方程式___________________________________。
(5)CPD可以与Br2的CC14溶液反应,写出其所有可能产物的结构简式_______________。
(6)参照上述流程图,并用流程图中出现的试剂和![]() 为原料合成
为原料合成 ,
,
设计其合成路线_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com