
【题目】(一)某实验小组利用如下装置(部分固定装置略)进行氮气与钙的反应,并探究其产物的性质及化学式。请回答下列问题。

(1)反应过程中末端导管必须插入试管C的水中,目的是____。(填字母)
A.吸收反应中剩余的氮气
B.控制通入气体的流速
C.防止空气中的氧气倒流进入反应装置,干扰反应
(2)该小组同学认为根据相应的质量关系可以求出生成物的化学式,数据记录如下:
A的质量m0/g | A与钙的质量m1/g | A与产物的质量m2/g |
14.80 | 15.08 | 15.15 |
①通过计算得到化学式CaxN2,其中x=____。
②小组同学查阅资料得知产物为Ca3N2,能与水强烈反应,请写出Ca3N2与水反应的化学方程式_____。
(二)铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2![]() 6SO2+Fe3O4,若有3molFeS2参加反应,转移电子的物质的量为_____。
6SO2+Fe3O4,若有3molFeS2参加反应,转移电子的物质的量为_____。
(2)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为____。
(3)将一定量的Fe2O3溶于160mL 5molL-1盐酸中,再加入一定量铁粉,铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶夜中无Fe3+,则参加反应的铁粉的质量为____。
【答案】BC 2.8 Ca3N2+6H2O=3Ca(OH)2+2NH3 32 2Fe3++2I-=2Fe2++I2 11.2g
【解析】
(一)(1)反应产生的尾气氮气不与水反应也不溶于水,把导管插入水中可以防止空气从导管进入装置而造成氧气与钙发生反应;
(2)由实验数据表中数据,计算参加反应钙的质量及生成氮化钙的质量,根据反应的化学方程式,由两物质的质量计算氮化钙化学式中x值;
(3)Ca3N2与水反应生成氢氧化钙与氨气。
(二)(1)根据电子得失,得出SO2与电子数的关系;
(2)氯化铁具有氧化性碘化氢具有还原性,二者发生氧化还原反应生成氯化亚铁和碘单质;(3)参加反应的铁粉为与铁离子反应及与氢离子反应的两部分之和,根据氢气的体积计算出与盐酸反应的铁的物质的量及HCl的物质的量,再根据氯原子守恒,求出氯化铁的物质的量,进而求出与铁离子反应的铁的物质的量。
(1)末端导管必须插入试管C的水中,可起到观察气体流速以及防止氧气进入反应装置,起到隔绝氧气的作用,防止钙与氧气反应而变质,故答案为:BC。
(2)参加反应钙的质量=15.08g14.80g=0.28g,参加反应的氮元素的质量为: 15.15g15.08g=0.07g,
xCa+N2═CaxN2
40x 28
0.28g 0.07g
![]() =
=![]() ,解得 x=2.8。
,解得 x=2.8。
故答案为:2.8。
(3)Ca3N2能与水反应生成氨气和氢氧化钙,反应方程式为:Ca3N2+6H2O=3Ca(OH)2+2NH3,故答案为:Ca3N2+6H2O=3Ca(OH)2+2NH3。
(二)(1)3FeS2+8O2![]() 6SO2+Fe3O4中,Fe、S元素的化合价升高,O元素的化合价降低,SO2和Fe3O4为氧化产物。3molFeS2参加反应,由O元素的化合价变化可知,转移的电子为8mol×2×(2-0)=32mol,故答案为:32mol。
6SO2+Fe3O4中,Fe、S元素的化合价升高,O元素的化合价降低,SO2和Fe3O4为氧化产物。3molFeS2参加反应,由O元素的化合价变化可知,转移的电子为8mol×2×(2-0)=32mol,故答案为:32mol。
(2)氯化铁具有氧化性碘化氢具有还原性,二者发生氧化还原反应生成氯化亚铁和碘单质,离子方程式为:2Fe3++2I-=2Fe2++I2,故答案为:2Fe3++2I-=2Fe2++I2。
(3)依次发生反应为Fe2O3+6HCl=2FeCl3+3H2O;Fe+ 2FeCl3=3FeCl2;Fe+2HCl=FeCl2+H2↑;n(H2)=![]() =0.1mol,过量的铁粉与盐酸反应的物质的量为:
=0.1mol,过量的铁粉与盐酸反应的物质的量为:
Fe~~~~2HCl~~~~H2
0.1mol 0.2mol 0.1mol
根据氯原子守恒,FeCl3的物质的量为×[n(HCl)-2n(H2)]=0.16L×5mol/L-0.2mol)=0.2mol
Fe~~~2FeCl3
0.1mol 0.2mol
所以参加反应的铁粉的质量为(0.1mol+0.1mol)×56g/mol=11.2g,故答案为:11.2g。


科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应aX(g)+bY(g)=cZ(g)+dW(g),反应达到平衡后,保持温度不变,将容积扩大到原来的2倍,当再次达到平衡时,W的浓度为原平衡时的3/5,下列叙述正确的是( )
A. 平衡向逆反应方向移动 B. a+b<c+d
C. X的体积分数增大 D. X的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在温度低于570℃ 时,还原铁粉与水蒸气反应的产物是FeO;高于570℃ 时,生成Fe3O4。老师用下图所示实验装置,完成了还原铁粉与水蒸气反应的演示实验。

甲同学为探究实验后试管内固体的成分,进行了下列实验:
实验编号 | 实验操作 | 实验现象 |
① | 取少量黑色粉末放入试管中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
② | 向试管中滴加几滴KSCN溶液,振荡 | 溶液没有出现血红色 |
试回答下列问题:
(1)湿棉花的作用是______________。
(2)写出高于570℃ 时,Fe 与水蒸气反应的化学方程式:___________。
(3)乙同学认为加入KSCN 溶液没有出现血红色的原因可能是固体中没有Fe3O4,也有可能是因为___(填物质名称)过量造成的。该物质过量时,溶液中还会发生反应,导致加入KSCN 溶液时没有出现血红色,该反应的离子方程式是______________。
(4)丙同学利用上述实验①加盐酸后的溶液制取白色的Fe(OH)2沉淀,向滤液中加入足量NaOH 溶液后,观察到的实验现象为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D 四种短周期元素,A 与B 可形成离子化合物BA,BA 中阴阳离子的核外电子排布相同;B 原子最外层只有-个电子;C 元素有三种不同的核素C1、C2、C3,且三种核素的质量数之比为1:2:3;D 原子的质子数是A、B、C 三种原子质子数之和的![]() 。
。
回答下列问题:
(1)写出各元素的元素符号:A____,B____,C____,D____。
(2)写出C1、C2、C3三种核素的原子符号:C1____,C2_____,C3______。
(3)C、D 两种元素形成的微粒X 与化合物BA 中的阳离子所含的质子数和电子数分别相等,则X 的化学式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1 L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,下列对该溶液成分说法不正确的是( )
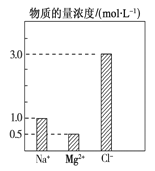
A. NaCl的物质的量为0.1mol
B. 该混合液中BaCl2的物质的量为0.05mol
C. 溶质MgCl2的质量为9.5 g
D. 将该混合液加水稀释至体积为1 L,稀释后溶液中的Na+物质的量的浓度为0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法错误的是
A. 标准状况下,30.8gCCl4中所含的原子数为NA
B. 100g46%乙醇溶液中含有的H-O键的数目为NA
C. 1molNa2O2与足量的CO2充分反应,转移的电子数为NA
D. n(H2SO3)+n(HSO3-)=1mol的NaHSO3溶液中,含有Na+的数目大于NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香叶醇是合成玫瑰香油的主要原料,其结构简式如图:下列有关香叶醉的叙述正确的是( )

A. 香叶醇的分子式为C10H18O
B. 不能使溴的四氯化碳溶液褪色
C. 不能使酸性高锰酸钾溶液褪色
D. 能发生加成反应不能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A. 氯气与碘化钾溶液反应:Cl2 + I- = Cl- + I2
B. 醋酸除去水垢:2H+ + CaCO3 = Ca2+ + CO2↑ + H2O
C. 铜和浓硝酸反应:Cu + 4H+ + 2NO![]() = Cu2+ + 2NO2↑ + 2H2O
= Cu2+ + 2NO2↑ + 2H2O
D. 二氧化锰与浓盐酸反应:MnO2 + 4H+ + 4Cl- ![]() Mn2+ + 2Cl2↑ + 2H2O
Mn2+ + 2Cl2↑ + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列物质:①氢氧化钡固体②KHSO4③HNO3④稀硫酸⑤二氧化碳气体⑥铜⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠⑩CuSO4·5H2O晶体。
请用序号填空:
(1)上述状态下可导电的是___。
(2)属于电解质的是___。
(3)属于非电解质的是___。
(4)②在水溶液中的电离方程式为___,①与②以物质的量之比为1:2在溶液中反应的离子方程式为___。
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,还原产物是___(填名称)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com