
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。其它条件相同时,
 在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,
在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,
发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?)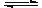 aZ(g)。
aZ(g)。
此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )
A.若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ
B.若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ
C.a为2
D.平衡时Ⅰ容器的体积小于V L
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
在无土栽培中,配制1 L内含0.5 mol/L NH4Cl、0.16 mol/L KCl、0.24 mol/L K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量分别为 , , 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列方法中可以说明2HI(g)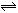 H2(g)+I2(g)已达到平衡的是:①单位时间内生成n mol H2的同时生成n mol HI;②一个H–H键断裂的同时有两个H–I键断裂;③百分组成ω(HI)=ω(I2);④反应速率υ(H2)=υ(I2)=1/2υ(HI)时;⑤ c(HI):c(H2):c(I2)=2:1:1时;⑥温度和体积一定时,容器内压强不再变化;⑦温度和体积一定时,某一生成物浓度不再变化;⑧条件一定,混合气体的平均相对分子质量不再变化;⑨温度和体积一定时,混合气体的颜色不再变化;⑩温度和压强一定时,混合气体的密度不再变化。( )
H2(g)+I2(g)已达到平衡的是:①单位时间内生成n mol H2的同时生成n mol HI;②一个H–H键断裂的同时有两个H–I键断裂;③百分组成ω(HI)=ω(I2);④反应速率υ(H2)=υ(I2)=1/2υ(HI)时;⑤ c(HI):c(H2):c(I2)=2:1:1时;⑥温度和体积一定时,容器内压强不再变化;⑦温度和体积一定时,某一生成物浓度不再变化;⑧条件一定,混合气体的平均相对分子质量不再变化;⑨温度和体积一定时,混合气体的颜色不再变化;⑩温度和压强一定时,混合气体的密度不再变化。( )
A、②③⑤ B、①④⑦ C、②⑦⑨ D、⑧⑨⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分。
(1)Cu2+基态的电子排布式可表示为 ;
(2)SO42-的空间构型为 (用文字描述);中心原子采用的轨道杂化方式是 ;写出一种与SO42-互为等电子体的分子的化学式: ;
(3) 向CuSO4 溶液中加入过量NaOH溶液可生成[Cu (OH)4 ]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为 ;
(4)资料显示ZnS为难溶物,在活化过程中,CuSO4能转化为CuS的原因是 。
(5)CuS比CuO的熔点 (填高或低),原因是 。
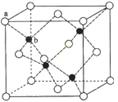
(6)闪锌矿的主要成分ZnS,晶体结构如下图所示,其晶胞边长为540.0 pm,密度为____________(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为___________________pm(列式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
管道煤气的主要成分是H2、CO和少量的甲烷。相应的热化学反应方程式为:
2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ/mol
2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ/mol
CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3 kJ/mol
当使用管道煤气的用户改用天然气后,在相同条件下燃烧等体积的天然气,
理论上所获得的热值,前者大约是后者的多少倍( )
A.0.8 B.1.3 C.3.1 D.0.32
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒容密闭容器中A(g)+3B(g)
 2C(g) ΔH<0,达平衡后,将气体混
2C(g) ΔH<0,达平衡后,将气体混
合物的温度降低,下列叙述中不正确的是 ( )
A.容器中混合气体的平均相对分子质量增大
B.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
C.正反应速率和逆反应速率都变小,C的百分含量增加
D.混合气体密度的变化情况不可以作为判断反应是否再次达平衡的依据
查看答案和解析>>
科目:高中化学 来源: 题型:
恒容密闭容器中,发生反应H2(g)+Br2(g) 
 2HBr(g) ΔH<0。恒温下
2HBr(g) ΔH<0。恒温下
发生反应,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述
反应,平衡时Br2(g)的转化率为b。a与b的关系是( )
A.a>b B.a=b C.a<b D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )
A.从1L1mol/L的氯化钠溶液中取出10ml,其浓度仍是1mol/L
B.制成0.5L10mol/L的盐酸,需要氯化氢气体112L(标准状况)
C.0.5 L 2mol/L的氯化钡溶液中,钡离子和氯离子总数为 2×6.02×1023
D.10g 98%硫酸(密度为1.84g/cm3)与10 mL 18.4 mol/L硫酸的浓度是相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中,将1.0molCO与1.0molH2O混合加热到800℃,发生下列反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),一段时间后该反应达到平衡,测得CO的物质的量为0.5mol.求:
(1)达到平衡时CO2的物质的量分数和该反应的化学平衡常数;
(2)达到平衡后向该平衡体系中通入1.0mol水蒸气,达到新的平衡状态时,求水蒸气的物质的量和CO2的物质的量分数.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com