
下列说法错误的是( )
A.从1L1mol/L的氯化钠溶液中取出10ml,其浓度仍是1mol/L
B.制成0.5L10mol/L的盐酸,需要氯化氢气体112L(标准状况)
C.0.5 L 2mol/L的氯化钡溶液中,钡离子和氯离子总数为 2×6.02×1023
D.10g 98%硫酸(密度为1.84g/cm3)与10 mL 18.4 mol/L硫酸的浓度是相同的
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
不能用来判断醋酸属于弱电解质的实验事实是
A.向某浓度的醋酸钠溶液滴入几滴酚酞试液:溶液由无色变为浅红色
B.向滴有甲基橙试液的醋酸溶液加入少量醋酸钠晶体:振荡后溶液由红色变为橙色
C.通过对比不同浓度的导电实验:醋酸溶液的导电性较盐酸溶液的导电性弱
D.取相同体积pH=1的盐酸和醋酸溶液,分别加入足量的锌,用排水法收集生成的氢气:相同条件下,醋酸生成的氢气体积大
查看答案和解析>>
科目:高中化学 来源: 题型:
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。其它条件相同时,
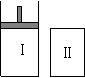 在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,
在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,
发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?)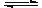 aZ(g)。
aZ(g)。
此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )
A.若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ
B.若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ
C.a为2
D.平衡时Ⅰ容器的体积小于V L
查看答案和解析>>
科目:高中化学 来源: 题型:
测定稀硫酸和稀氢氧化钠中和热的实验装
置如右图所示.
(1)写出该反应的热化学方程式(中和热为57.3 kJ/mol):
__________________________________________;
(2) 装置图中碎泡沫塑料所起作用为: ;
(3) ①取50 mL NaOH溶液和30 mL硫酸溶液进行实验,
实验数据如下表.请填写下表中的空白:
| 温度 实验次数 | 起始温度T1/℃ | 终止温度T2/℃ | 温度差平均值(T2-T1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | ________ |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 |
②若上述实验所测中和热数值偏小,产生偏差的原因可能是( )
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
300mL某浓度的NaOH溶液中含有60g溶质,现欲配制1mol/L NaOH溶液,应取原溶液与蒸馏水的体积比约为( )
A.1∶4 B.1∶5 C.2∶1 D.2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
将a%的某物质的水溶液加热蒸发掉m g水(溶质不挥发、且蒸发过程无溶质析出),所得溶液体积为V L,溶质的质量分数为蒸发前的2倍,设溶质的相对分子质量为M,则蒸发后所得溶液的物质的量浓度为( )mol/L
A ma/2VM B ma/100VM C 20ma/2VM D ma/50VM
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质全部是弱电解质的是( )
A.H2SiO3 H2S CO2 B.MgSO4 CH3COOH CH3CH2OH
C.H2SO3 BaSO4 CH4 D.H2O NH3•H2O H3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g)⇌nY(g);△H=Q kJ/mol.反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
| /L积体气温体c(Y)/mol•L﹣1度/℃ | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
下列说法正确的是( )
|
| A. | m>n |
|
| B. | Q<0 |
|
| C. | 温度不变,压强增大,Y的质量分数减少 |
|
| D. | 体积不变,温度升高,平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
可以将反应Zn+Br2 = ZnBr2设计成蓄电池,下列4个电极反应
①Br2 + 2e- = 2Br- ②2Br- - 2e- = Br2 ③Zn – 2e- = Zn2+ ④Zn2+ + 2e- = Zn
其中表示充电时的阳极反应和放电时的负极反应的分别是
A.②和③ B.②和① C.③和① D.④和①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com