
【题目】国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:__________________________。
(2)小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:_________________。
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与金属铜发生反应的离子方程式:_________________________________。
(4)除去Na2CO3粉末中混入的NaHCO3杂质最佳方法是_________,化学方程式为________________________。
【答案】2Na2O2+2CO2=2Na2CO3+O2 NaHCO3=Na++HCO3- Cu+2Fe3+=2Fe2++Cu2+ 加热 2NaHCO3![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
【解析】
根据钠及其化合物的性质分析解答;根据离子反应方程式的书写规则分析解答。
(1)过氧化钠作供氧剂时,是与呼出的CO2和水反应,生成O2,方程式为:2Na2O2+2CO2=2Na2CO3+O2;
(2) 小苏打常作面包和糕点的发泡剂,是由于NaHCO3受热分解生成CO2气体,它的电离方程式为:NaHCO3=Na++HCO3-;
(3) 电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板,即FeCl3与Cu反应生成FeCl2和CuCl2,方程式为:Cu+2FeCl3=2FeCl2+CuCl2,离子方程式为:Cu+2Fe3+=2Fe2++Cu2+;
(4)由于NaHCO3受热分解生成CO2气体和Na2CO3利用这一性质,我们可以除去Na2CO3粉末中混入的NaHCO3杂质,方程式为:2NaHCO3![]() Na2CO3+CO2↑+H2O。
Na2CO3+CO2↑+H2O。


科目:高中化学 来源: 题型:
【题目】己知 2Na+O2![]() Na2O2,2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2=2NaCO3+O2↑,下列灭火剂能用于扑灭金属钠着火的是()
Na2O2,2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2=2NaCO3+O2↑,下列灭火剂能用于扑灭金属钠着火的是()
A. 干冰灭火剂 B. 水 C. 黄沙 D. 泡沫灭火剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为一定条件下采用多孔惰性电极的储氢电池充电装置(忽略其他有机物)。
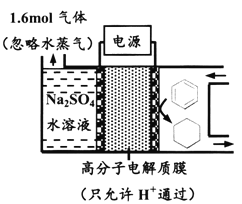
已知储氢装置的电流效率![]() 100%,下列说法不正确的是
100%,下列说法不正确的是
A. 若η=75%,则参加反应的苯为0.8mol
B. 过程中通过C—H键断裂实现氢的储存
C. 采用多孔电极增大了接触面积,可降低电池能量损失
D. 生成目标产物的电极反应式为:C6H6+6e-+6H+=C6H12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,既是化合反应,又是氧化还原反应的是
A. 生石灰与水反应:CaO+ H2O =Ca(OH)2
B. 氯气通入溴化钠溶液:C12+2NaBr= 2NaCl+Br2
C. 铁和氯气反应:2Fe+3Cl2![]() 2FeC13
2FeC13
D. 氯化钠溶液和浓硫酸混合加热:2NaCl+H2SO4(浓)![]() Na2SO4+2HCl↑
Na2SO4+2HCl↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】电化学还原技术是一种处置CO2的绿色环保、有发展潜力的方法。铜、铂、铟(In)等金属都是该反应的催化剂。
(1)In元素基态原子的价电子排布式为____________。与Cu元素同周期,且基态原子有2个未成对电子的过渡元素是_________________(填元素符号)。
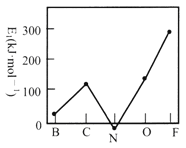
(2)第一电子亲和能(E1)是元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量。第二周期部分元素的E1变化趋势如图所示。试分析碳元素的E1较大的原因_____________________________。
(3)[PtC14(NH3)2]中N原子的杂化方式为________,所含化学键类型包括_______(填字母)。
a.离子键b.共价键c.金属键d.配位键e.氢键
[PtCl4(NH3)2]中H-N-H键之间夹角______(填“>”“<”或“=”)NH3分子中H-N-H键之间夹角,原因是__________________________________。
(4)C60晶体可采取非最密堆积,然后在空隙中插入金属离子获得超导体,如图为K3C60的面心立方晶胞。则K+占据的是C60围成的正四面体空隙和_____空隙,若C60分子的原子坐标参数分别为A(0,0,0),B(![]() ),C(1,1,1)等,则距离A位置C60分子最近的K+的原子坐标参数为_____________。判断晶体熔沸点高低:C60_________K3C60(填“>”“<”或“=”)。
),C(1,1,1)等,则距离A位置C60分子最近的K+的原子坐标参数为_____________。判断晶体熔沸点高低:C60_________K3C60(填“>”“<”或“=”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,反应后固体物质增重的是( )
A.氢气通过灼热的CuO粉末
B.二氧化碳通过Na2O2粉末
C.氢氧化铝受热分解
D.将锌粒投入CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。

填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的是________,A中反应的离子方程式是________。
(2)实验开始时应先将活塞a打开,其目的是____________________。
(3)简述生成Fe(OH)2的操作过程:_______________________
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为____。
(5)图中________(填“能”或“不能”)较长时间看到Fe(OH)2白色沉淀。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com