
【题目】下列关于原电池的叙述中正确的是
A.正极和负极必须是两种不同的金属
B.电子流入的一极为正极
C.原电池工作时,正极和负极上发生的都是氧化还原反应
D.原电池工作时,实现了将电能转化为化学能
科目:高中化学 来源: 题型:
【题目】已知H2C2O4是二元弱酸,室温下向某浓度的草酸溶液中逐滴加入KOH溶液,所得溶液中H2C2O4、HC2O4-、C2O42-的组成百分率与pH的关系如图所示,下列说法正确的是
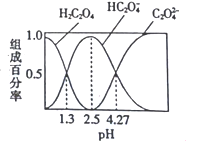
A. pH=4.27的溶液中:c(K+)+c(H+)=c(OH-)+3c(C2O42-)
B. 反应HC2O4-+H2O![]() H2C2O4+OH-的平衡常数为10-4.27
H2C2O4+OH-的平衡常数为10-4.27
C. 向溶液中加入KOH溶液将pH由1.3调至4.27的过程中水的电离程度先增大后减小
D. pH=2.5的溶液中:c(H+)+2c(H2C2O4)=c(OH-)+c(C2O42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A、B、C均是由短周期元素组成的单质,其余物质均为化合物.F在常温常压下为液态,I为具有磁性的黑色晶体.它们有下图所示的转化关系: 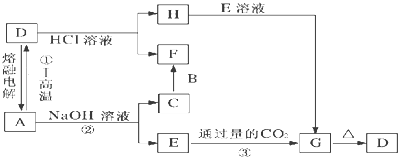
根据以上转换关系回答:
(1)写出反应①的化学方程式:;
(2)写出反应②的离子方程式:;写出H+E反应的离子方程式:;
(3)将I溶于足量盐酸,请分别写出反应后混合溶液中存在的阳离子、检验所需试剂及相应现象(可不填满):
阳离子 | 检验试剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对化学用语的理解,正确的是( )
A. 结构式:A=B=A,既可以表示CO2,也可以表示SiO2
B. 电子式![]() 可以表示羟基,也可以表示氢氧根离子
可以表示羟基,也可以表示氢氧根离子
C. 比例模型![]() :可以表示甲烷分子,也可以表示四氯化碳分子
:可以表示甲烷分子,也可以表示四氯化碳分子
D. 离子结构示意图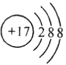 :可以表示35Cl-,也可以表示37Cl-
:可以表示35Cl-,也可以表示37Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析如图所示的四个原电池装置。其中结论正确的是( )
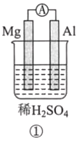
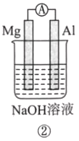
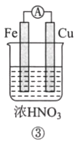
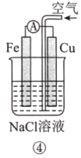
A. ①②中Mg作负极,③④中Fe作负极
B. ②中Mg作正极,OH-向Al电极移动
C. ③中Fe作负极,电极反应式为Fe-2e-=Fe2+
D. ④中Cu作正极,电极反应式为2Na++2e-=2Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单质A、B、C在一定条件下,可以按下面的流程进行反应.已知单质A、B常温下分别为无色气体和黄绿色气体,单质C是常见的金属,D的水溶液常温下能与单质C反应生成F和单质A. 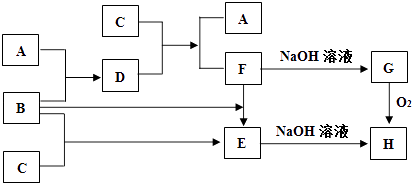
请完成下列填空:
(1)写出单质B的化学式 , D物质的电子式 .
(2)写出E→H的化学方程式 .
(3)写出D+C→F+A的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有Mg2+、Ba2+、Cl-、CO32-、Cu2+、Fe3+中的一种或几种离子。为确定其成分,进行以下实验:
实验1:取10mL无色溶液,滴加过量稀盐酸无明显现象。
实验2:另取10mL无色溶液,加入足量的Na2SO4溶液,有白色沉淀生成。
实验3:取实验1后的溶液于锥形瓶中,向锥形瓶中逐滴加入NaOH溶液,滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如右图所示。

回答下列问题:
(1)原溶液中不存在的离子是__________,存在的离子是________________。
(2)实验3中,图像中OA段反应的离子方程式为____________________________。
(3)根据图像计算原溶液中Mg2+的物质的量浓度_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com