
A、CH4+Cl2
| |||
B、CH3Cl+Cl2
| |||
C、CH3OH+HCl
| |||
D、CH2=CH2+H2
|


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
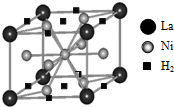 能源、材料和信息是现代社会的三大“支柱”.
能源、材料和信息是现代社会的三大“支柱”.
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SiO2既能溶于NaOH溶液,又能与氢氟酸反应,属于两性氧化物 |
| B、电解熔融NaCl或其水溶液都可制得Cl2 |
| C、铝热反应不仅可用于焊接钢轨,还可用于金属的冶炼 |
| D、化石燃料燃烧产生大量CO2,会导致温室效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S(s)在氧气中燃烧的反应是放热反应 |
| B、S(s)+O2(g)═SO2(g)△H=b kJ?mol-1,则a<b |
| C、1mol SO2(g)所具有的能量低于1mol S(s)与1mol O2(g)所具有的能量之和 |
| D、16g固体硫在氧气中充分燃烧,可放出148.6kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、负极减重0.35g |
| B、正极Mn元素化合价降低,被氧化 |
| C、可以用某盐的水溶液作电解质溶液 |
| D、负极发生还原反应,反应式为Li++e-=Li |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com