
| A、Al2 (SO4)3=2Al3++3SO42- |
| B、Ba(OH)2=Ba2++2OH- |
| C、Na2SO4=Na2++SO42- |
| D、NH4NO3=NH4++NO3- |


科目:高中化学 来源: 题型:
| A、将142g Na2SO4溶于少量水后再稀释到 100mL |
| B、1 L溶液中含有142 g Na2SO4 |
| C、1 mol Na2SO4溶于1 L蒸馏水中 |
| D、溶液中含有1molNa+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向含有Hg2+的废水中加入Na2S:Hg2++S2-═HgS |
| B、用碳酸氢钠作为抗酸药来中和胃酸 2H++CO32-═H2O+CO2↑ |
| C、用熟石灰来中和酸性废水 Ca(OH)2+2H+═Ca2++2H2O |
| D、用H2SO4来中和碱性废水 2H++2OH-═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、可通过溶液导电能力的大小判断强弱电解质 |
| D、在NaHSO4溶液中存在的离子有:Na+、H+、HSO4-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
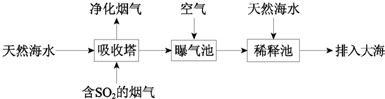
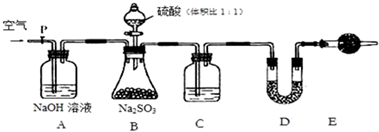
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com