
【题目】为更有效处理工业废气中排放的氮氧化物(NOx)、SO2等,减少大气污染。科学家不断对相关反应进行研究尝试。
(1)脱硝反应机理如图,Cu+的作用是____________,C2H4参与的反应方程式 ______________ 。
(2) 选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g);ΔH= -1627 kJmol-1
4N2(g)+6H2O(g);ΔH= -1627 kJmol-1
① 其中被NO和O2氧化的NH3的比例 ________ 。
②该方法应控制反应温度在315~400℃之间,反应温度不宜过高的原因是________ 。
③ 氨氮比 n(NH3)/n(NO) 会直接影响该方法的脱硝率。如图为350 ℃时,只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当 n(NH3)/n(NO) >1.0时,烟气中NO含量反而增大,主要原因是_________________________________。

(3) 烟气脱硫、脱硝一体化技术是大气污染防治研究的热点。ClO2及NaClO2均是性能优良的脱硫脱硝试剂。
① ClO2在酸性条件下稳定,在NaOH溶液中可歧化为NaClO3和NaClO2,该反应的化学方程式为____。

② 某研究小组用ClO2进行单独脱除SO2实验时,测得SO2的脱除率随溶液pH变化如图所示。当3<pH<7时,随pH的增大,SO2脱除率逐渐降低,其原因是________;在pH约7.8之后,随pH的增大,SO2脱除率又开始升高,其原因是________。
【答案】催化剂 2C2H4 + 6Cu+(NO2) = 3N2 + 4CO2 + 4H2O + 6Cu+ 2:1 正反应放热,温度过高会降低NO的转化率 NH3和O2再次反应生成NO(或4NH3+5O2=4NO+6H2O) 2ClO2 + 2NaOH = NaClO3 + NaClO2 + H2O pH<7时,随着pH值的增大,ClO2的稳定性降低氧化性减弱,SO2的脱除率降低。 当pH>7.8后,随着碱性的增强,生成ClO2-增多,氧化性增强,SO2的脱除率上升
【解析】
(1) Cu+在反应前后不变为催化剂;用乙烯进行脱硝(NO),从图示可以知道,乙烯被氧化成二氧化碳;
(2)①根据得到电子的比例计算;
②根据温度对速率和化学平衡的影响分析;
③根据过量氨气与氧气的反应的产物分析;
(3)① ClO2在NaOH溶液中可歧化为NaClO3和NaClO2,根据得失电子守恒写出该反应的化学方程式;
②由图可知,当3<pH<7时,随pH的增大,ClO2的稳定性降低,氧化性减弱,SO2脱除率逐渐降低;在pH约7.8之后,随pH的增大,生成ClO2-增多,氧化性增强,SO2脱除率又开始升高。
(1) 催化剂在化学反应前后性质、质量不变,图示中Cu+在反应前后不变,为催化剂;用乙烯进行脱硝(NO),从图示可以知道,乙烯被NO氧化成二氧化碳(其中C由-2→+4),NO自身被还原成N2(其中N由+2→0),反应方程式为:2C2H4 + 6Cu+(NO2) = 3N2 + 4CO2 + 4H2O + 6Cu+,
因此,本题正确答案是:催化剂;2C2H4 + 6Cu+(NO2) = 3N2 + 4CO2 + 4H2O + 6Cu+;
(2)①由方程式4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)可知,该反应O2和NO都作氧化剂,1molO2得4mol电子,4molNO得8mol电子,因此被NO和O2氧化的NH3的比例为2:1,
4N2(g)+6H2O(g)可知,该反应O2和NO都作氧化剂,1molO2得4mol电子,4molNO得8mol电子,因此被NO和O2氧化的NH3的比例为2:1,
因此,本题正确答案是:2:1;
②该方法应控制反应温度在315~400℃之间,反应温度不宜过高,温度过高,使脱硝的主要反应的平衡向逆方向移动,脱硝率降低,
因此,本题正确答案是:正反应放热,温度过高会降低NO的转化率;
③当 n(NH3)/n(NO) >1.0时,过量的氨气与氧气反应生成NO,所以烟气中NO浓度增大,
因此,本题正确答案是:NH3和O2再次反应生成NO;
(3)① ClO2在NaOH溶液中可歧化为NaClO3和NaClO2,反应的化学方程式为2ClO2 + 2NaOH = NaClO3 + NaClO2 + H2O,
因此,本题正确答案是:2ClO2 + 2NaOH = NaClO3 + NaClO2 + H2O;
②由图可知,当3<pH<7时,随pH的增大,ClO2的稳定性降低,氧化性减弱,SO2脱除率逐渐降低;在pH约7.8之后,随pH的增大,生成ClO2-增多,氧化性增强,SO2脱除率又开始升高。
因此,本题正确答案是:pH<7时,随着pH值的增大,ClO2的稳定性降低氧化性减弱,SO2的脱除率降低;当pH>7.8后,随着碱性的增强,生成ClO2-增多,氧化性增强,SO2的脱除率上升。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某硫原子的质量是ag,12C原子的质量是bg,若NA只表示阿伏加德罗常数的数值,则下列说法中正确的是( )
①该硫原子的相对原子质量为![]() ②mg该硫原子的物质的量为
②mg该硫原子的物质的量为![]() mol
mol
③该硫原子的摩尔质量是aNA g ④ag该硫原子所含的电子数为16NA
A. ①③ B. ②④ C. ①② D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达平衡,平衡常数K=![]() 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
A、该反应的焓变为正值
B、恒温恒容下,增大压强,H2浓度一定减小
C、升高温度,逆反应速率减小
D、该反应化学方程式为CO+H2O=CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是形成单质和化合物最多的元素,其单质及化合物有独特的性质和用途。请回答下列问题。
(1)C原子的价电子轨道表达式为______________________。
(2)碳元素是组成有机物必不可少的元素。1828年,化学家维勒首次用加热的方法将无机物氰酸铵[NH4(OCN)]转化为有机物尿素,开启了人造有机物的大门。氰酸铵中阳离子的立体构型是___________。有机物M( )在一定条件下生成N(
)在一定条件下生成N( )
)
①沸点:M___________N(填“大于”或“小于”)。
②M中碳原子的杂化类型为___________,不同杂化类型的碳原子数之比为___________。
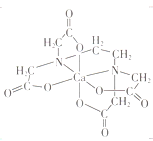
(3)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图所示。该配离子的配位数是___________,配体中碳原子的杂化方式有_________。
(4)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图所示,图中用实线标出了石墨的一个六方晶胞。

①石墨中C原子上未参与杂化的所有p轨道相互平行且重叠,使p轨道中的电子可在整个碳原子平面中运动而导电。六方氮化硼(BN)与石墨晶体结构类似,硼原子和氮原子交替相连,而六方BN却无法导电,其原因是___________。
②晶胞有两个基本要素:石墨一种晶胞结构和部分晶胞参数如图。

a.原子坐标参数描述的是晶胞内原子间的相对位置。石墨晶胞中碳原子A、B的坐标参数分别为A(0,0,0)、B(0,1,![]() ),则C原子的坐标参数为___________。
),则C原子的坐标参数为___________。
b. 晶胞参数用以描述晶胞的大小和形状。已知石墨晶胞底边长为acm,层间距为 d cm,阿伏加德罗常数的值为NA,则石墨的密度为___________g·cm-3(写出表达式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列A、B、C、D是中学常见混合物分离或提纯的基本装置。请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。

(1)除去Ca(OH)2溶液中悬浮的CaCO3_________________;
(2)从碘水提取碘______________;
(3)用自来水制取蒸馏水_________________;
(4)分离植物油和水_____________;
(5)与海水晒盐原理相符的是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A. 糖类都是天然高分子化合物,组成与结构比较复杂
B. 可以用酸性高錳酸鉀溶液鉴别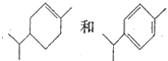
C. 体积分数为90%的乙醇溶液能使蛋白质变性,常用于医疗消毒
D. 甲苯的一溴代物和2一甲基丁烷的一溴代物都有4种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下各组列物质反应的化学方程式并指出反应类型:
(1)硫酸和Ba(OH)2溶液_____________、______________ ;
(2)盐酸和Na2CO3溶液____________、______________;
(3)H2O2溶液和MnO2混合_________、_________________;
(4)铝和氯化铜溶液__________、______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用密度1.18g/mL、质量分数为36.5%的浓盐酸配制250mL0.1mol/L的盐酸,回答下列问题:
(1)配制250mL0.1mol/L的盐酸
应量取的浓盐酸的体积/mL | 应选用的容量瓶的规格/mL | 除容量瓶外需要的其他仪器 |
____ | ____ | ____ |
(2)配制时,正确的操作顺序是____(填编号)。
A.用适量蒸馏水洗涤烧杯和玻璃棒2~3 次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸,沿玻璃棒倒入烧杯中,再加入适量蒸馏水,用玻璃棒搅拌, 使其混合均匀
C.将已冷却的溶液沿玻璃棒注入所选容量瓶中
D.盖好瓶塞,上下颠倒摇匀
E 改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm 处
(3)操作A中,将洗涤液都注入容量瓶,其目的是______, 若无操作A,则所配溶液浓度____(填“偏大”、“偏小”或“不变”)
(4)E中加蒸馏水不慎超过了刻度线,则所配溶液浓度____(填“偏大”、“偏 小”或“不变”),应如何处理______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com