
【题目】下列有关电解质及其溶液的说法正确的是
A. 向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中![]() 增大
增大
B. 将CH3COONa溶液从20℃升温至30℃,溶液中![]() 减小
减小
C. 厕所清洁剂、醋、肥皂和厨房清洁剂等物质是按酸碱性的一定顺序依次排列的
D. 将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓AgNO3溶液,溶液中会有等物质的量的沉淀生成[已知:Ksp(AgCl)>Ksp(AgBr)]
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
【题目】电子工业中,常用FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。某同学为了从腐蚀废液中回收铜,并重新获得FeCl3溶液,设计如下流程图
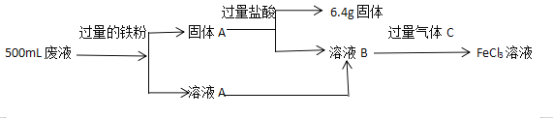
请回答下列问题:
(1)FeCl3溶液腐蚀铜箔反应的离子方程式为___________。
(2)固体A的成分是_______,气体C的化学式为____________。
(3)设计实验方案证明FeCl3溶液中的金属阳离子_____________。
(4)反应消耗铁粉11.2g,则废液中Fe3+的物质的量浓度是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3 mol·L-1 NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g,则下列有关叙述中正确的是( )
A. 加入合金的质量不可能为6.4 g
B. 参加反应的硝酸的物质的量为0.1 mol
C. 沉淀完全时消耗NaOH溶液的体积为150 mL
D. 溶解合金时收集到NO气体的体积在标准状况下为2.24 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①R—NO2![]() R—NH2;②苯环上的取代基对新导入的取代基进入苯环的位置有显著的影响。如图表示以苯为原料制备一系列有机物的转化过程:
R—NH2;②苯环上的取代基对新导入的取代基进入苯环的位置有显著的影响。如图表示以苯为原料制备一系列有机物的转化过程:
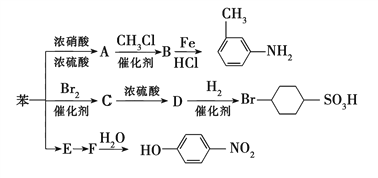
(1)A是一种密度比水___(填“大”或“小”)的无色液体,苯转化为A的化学方程式是________________________________________________。
(2)在“苯![]() C
C![]() D
D![]()
![]() ”的转化过程中,属于取代反应的是___(填序号,下同),属于加成反应的是_______。
”的转化过程中,属于取代反应的是___(填序号,下同),属于加成反应的是_______。
(3)图中“苯→E→F”的转化过程省略了反应条件,请写出E的结构简式:________。
(4)有机物B苯环上的二氯代物有___种结构;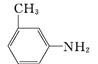 的所有原子___(填“在”或“不在”)同一平面上。
的所有原子___(填“在”或“不在”)同一平面上。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA 表示阿伏加德罗常数,下列说法不正确的是( )
A. 4.6 克金属钠与 500mL0.2molL-1 稀盐酸反应,转移电子数为 0.1NA
B. 0.012kg12C 含有 NA 个 12C 原子
C. 等 物 质 的 量 的OH- 与 NH4+ 所 含 电 子 数 相 同
D. 标准状况下,以任意比例混合的 CH4 和 CO2 混合物 22.4L,含有的碳原子数约为 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学方法是化工生产及生活中常用的一种方法。回答下列问题:
(1)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺如右图所示。
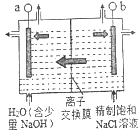
①图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。产生ClO2的电极应连接电源的______(填“正极”或“负极”),对应的电极反应式为_____________________。
②a极区pH________(填“增大”、“减小”或“不变”)。
③图中应使用_______(填“阴”或“阳”)离子交换膜。
(2)燃料电池因具有发电效率高、环境污染少等优点而备受人们关注。某燃料电池以足量NaOH溶液为电解质,以甲烷为燃料,空气为氧化剂,以具有催化作用和导电性能的某金属材料为电极,则电池的负极反应式为_____________。
(3)银白光亮的银器用久后表面易出现黑斑(Ag2S),利用电化学原理可处理黑斑。将银器置于铝制容器里的食盐水中并与铝接触,Ag2S转化为Ag,则正极的电极反应式为____,处理过程中,发现有白色沉淀和臭鸡蛋气味的气体产生,它们分别是______、______(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某微粒的核外电子排布式为1s22s22p63s23p6,下列关于该微粒的说法正确的是( )
A.它的质子数一定是18
B.它的原子和37Cl可能互为同位数
C.它的单质一定是强还原剂
D.可以确定该微粒为Ar
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正硼酸(H3BO3)是一种片层状结构白色晶体,有与石墨相似的层状结构,受热易分解,层内的H3BO3分子通过氢键相连(如图所示),则下列有关说法中不正确的是
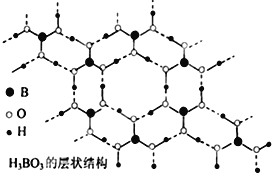
A. 正硼酸晶体属于分子晶体
B. 正硼酸分子的稳定性与氢键无关
C. 1molH3BO3晶体中含有3mol氢键
D. B原子杂化轨道的类型sp2,层间的H3BO3分子通过共价键相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分条件已略去)。 A 为海水中含量最高的盐类物质, C 为黄绿色气体, F 为生活中常见的金属单质, I 为红褐色沉淀。
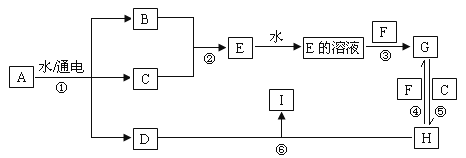
(1)E的化学式为____,I的化学式为____。
(2)写出反应①的化学方程式:____;写出反应⑤的离子方程式:____。
(3)检验 H 溶液中金属阳离子的方法是____。
(4)保存 G 溶液时要加少量固体 F 的原因是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com