
【题目】某同学用不同方法制得白色的Fe(OH)2沉淀。
(1)用未被氧化的FeSO4溶液与煮沸过的蒸馏水配制的NaOH溶液反应制备,制备过程中下列说法正确的是_______
A.用硫酸亚铁晶体配制上述FeSO4溶液时还需加入适量盐酸防止水解
B.除去蒸馏水中溶解的O2也可以采取振摇、静止的方法
C.生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液
D.FeSO4溶液上面加一层苯可以防止空气中氧气直接与溶液接触
(2)在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。在试管I 里加入稀H2SO4和铁屑,在试管II里加入NaOH溶液,打开止水夹,塞紧塞子,检验试管Ⅱ出口处排出的氢气的纯度。当排出的H2纯浄时,再____(填操作步骤),这样一段时间后试管Ⅲ中制得的Fe(OH)2沉淀能较长时间保持白色,其理由是__________________。
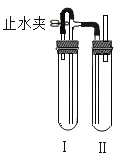
【答案】CD 夹紧止水夹试管 试管I和试管II充满了H2,且外界空气不容易进入
【解析】
(1)A.配制溶液时不能引入新的杂质;
B.摇动会增大O2在蒸馏水中的溶解度;
C.制取白色Fe(OH)2沉淀,要防止O2与制取Fe(OH)2的溶液接触;
D.苯密度比水小,覆盖在溶液液面上,可以防止空气中氧气直接与溶液接触;
(2)Fe与稀硫酸反应产生H2,H2通过导气管进入试管II,将试管II中溶液中的空气排出后,关闭止水夹,试管I中产生的FeSO4溶液进入试管II中,与II中NaOH反应产生Fe(OH)2沉淀,由于装置内无O2,因此可以较长时间观察到白色沉淀。
(1) A.用硫酸亚铁晶体配制上述FeSO4溶液时,FeSO4发生水解反应:FeSO4+2H2O![]() Fe(OH)2+H2SO4,为了抑制盐的水解,要加入酸,同时不能引入杂质离子,所以应该加入适量稀H2SO4,不能加入盐酸,A错误;
Fe(OH)2+H2SO4,为了抑制盐的水解,要加入酸,同时不能引入杂质离子,所以应该加入适量稀H2SO4,不能加入盐酸,A错误;
B.蒸馏水中溶解的O2若采取振摇、静止的方法,就会增大O2与蒸馏水的接触面积,不仅不能除去O2,反而会增大O2的溶解度,B错误;
C.用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,会发生反应:FeSO4+2NaOH= Fe(OH)2↓+Na2SO4,由于装置中避免了与O2的接触,因此可以较长时间观察到白色沉淀,C正确;
D.苯的密度比水小,难溶于水,覆盖在FeSO4溶液上面,就可以防止空气中氧气直接与溶液接触,因此可以制取得到Fe(OH)2白色沉淀,D正确;
故合理选项CD;
(2)在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备Fe(OH)2。在试管I 里加入稀H2SO4和铁屑,Fe与稀硫酸反应产生氢气和FeSO4,反应产生的氢气通过导气管进入到试管II里,将NaOH溶液及溶液上部空间的空气排出,使NaOH溶液周围充满了氢气当排出的H2纯浄时,再夹紧止水夹,试管I中反应产生的氢气使I中气体压强增大,将FeSO4溶液压入到试管II中,发生反应:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4,由于试管I和试管II整个装置中都充满了H2,且外界空气不容易进入装置内,所以制得的Fe(OH)2沉淀能较长时间保持白色。


科目:高中化学 来源: 题型:
【题目】下列溶液中Cl-浓度与50 mL 1 mol·L-1AlCl3溶液中Cl-浓度相等的是( )
A. 150 mL 1 mol·L-1的NaCl溶液B. 75 mL 2 mol·L-1NH4Cl溶液
C. 150 mL 2 mol·L-1的KCl溶液D. 100 mL 1.5mol·L-1的MgCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+ 5O2(g)![]() 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是
A. 达到化学平衡时,4υ正(O2)= 5υ逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
C. 达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D. 化学反应速率关系是:2υ正(NH3)= 3υ正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常温条件下甲、乙、丙三种溶液,甲为0.1mol·L-1的NaOH溶液,乙为0.1mol·L-1的HCl溶液,丙为0.1mol·L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的pH=_______;
(2)丙溶液中存在的电离平衡为________________(用电离平衡方程式表示);
(3)甲、乙、丙三种溶液中由水电离出的c(OH-)的由小到大顺序为________;

(4)某同学用甲溶液分别滴定20.00mL乙溶液和20.00mL丙溶液,得到如图所示两条滴定曲线,请完成有关问题:
①甲溶液滴定丙溶液的曲线是________(填“图1”或“图2”);
②a=_________mL
③pH试纸测定溶液pH的操作方法为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为应对全球石油资源口益紧缺。提高煤的利用效率,我国开发了煤制烃技术,并进入工业化试验阶段。
(1)煤气化制合成气(CO和H2):C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.3kJ/mol该反应在高温下能自发进行,理由是_____________。
(2)由合成气制甲醇:合成气CO和H2在一定条件下能发生如下反应:
主反应I.CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
反应II.CO(g)+H2(g)![]() C(s)+H2O(g)
C(s)+H2O(g)
①在容积均为VL的甲、乙、丙三个密闭容器中分别充入amolCO和2 amolH2,三个容器的反应温度分别为T1、T2、T3(T1<T2<T3)且恒定不变,若只发生反应I,在其他条件相同的情况下,实验测得反应均进行到tmin时CO的体积分数如图所示,此时三个容器中一定处于化学平衡状态的是_____(填“T1”、“T2”或“T3”):该温度下的化学平衡常数为_____(用a、V表示)。

②为减弱副反应的发生,下列采取的措施合理的是______。
A.反应前加入少量的水蒸气 B.增压
C.降低反应温度 D.使用合适催化剂,提高甲醇的选择性
(3)由甲醇制烯烃
主反应:i.2CH3OH![]() C2H4+2H2O
C2H4+2H2O
ii.3CH3OH![]() C3H6+3H2O
C3H6+3H2O
副反应:iii.2CH3OH![]() CH3OCH3+H2O
CH3OCH3+H2O
某实验室控制反应温度为400℃,在相同的反应体系中分别填装等量的两种催化剂(Cat.1和Cat.2),以恒定的流速通入CH3OH,在相同的压强下进行两种催化剂上甲醇制烯烃的对比研究。得到如图实验数据:(选择性:转化的甲醇中生成乙烯和丙烯的百分比)


下列说法不正确的是_________。
A.反应进行一段时间后甲醇的转化率减小,可能的原因是催化剂失活,工业生产中需定期更换催化剂
B.使用Cat.2反应2h后乙烯和内烯的选择性下降,可能的原因是生成副产物二甲醚
C.使用Cat.1产生的烯烃主要为丙烯,使用Cat.2产生的烯烃主要为乙烯
D.不管使用Cat.1还是使用Cat.2都能提高活化分子的百分数
(4)已知:2CrO42-+2H+![]() Cr2O72-+H2O。以铬酸钾为原料,电化学法备重铬酸钾的实验装置示意图如下
Cr2O72-+H2O。以铬酸钾为原料,电化学法备重铬酸钾的实验装置示意图如下

①a为电源的________(填“正极”或“负极”)
②该制备过程总反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1mol/LCH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+对于该平衡,下列叙述正确的是( )
CH3COO-+H+对于该平衡,下列叙述正确的是( )
A. 加入水时,平衡向逆反应方向移动
B. 加入少量NaOH固体,平衡向正反应方向移动
C. 加入少量0.1mol·L-1 HCl溶液,溶液中c(H+)减小
D. 加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年4月,我国自主设计,被称为“人造太阳”的“东方超环”核聚交实验装置取得重大突破,该核聚变的基础原料是海水中提取的氘和氚。下列叙述中错误的是
A.氘原子的相对原子质量为2
B.氚原子内中子数和核外电子数之差为1
C.氘原子和氚原子互为同位素
D.海水中的H2O与D2O互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸具有抗氧化、延缓衰老、减肥降脂等功效,它的结构简式为:  ,以邻苯二酚为原料合成迷迭香酸的路线如下所示,下列说法错误的是
,以邻苯二酚为原料合成迷迭香酸的路线如下所示,下列说法错误的是

A. 有机物A分子中所有原子可能在同一平面上
B. 有机物B可以发生取代、加成、消去、氧化反应
C. 1molC在催化剂作用下,与H2加成最多可消耗8mol
D. 1molC与足量的NaOH溶液反应,最多可消耗6 molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】O3能吸收有害紫外线,保护人类赖以生存的空间。O3的分子结构如图,呈V形,两个键的夹角为116.5°,三个原子以一个O原子为中心,与另外两个O原子分别构成一个共价键;中间O原子提供两个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键——三个O原子均等地享有这些电子。请回答:

(1)臭氧与氧气互为________________。
(2)下列分子与O3分子的结构最相似的是________。
A. H2O B. CO2 C. SO2 D. BeCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com