
| A、羟基与氢氧根有相同的化学式和电子式 |
| B、乙醇的官能团是-OH,乙醇是含-OH的化合物 |
| C、常温下,1mol乙醇可与足量的Na反应生成11.2L H2 |
D、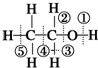 已知乙醇的结构式如图所示,则乙醇催化氧化时断裂的化学键为②③ |
 ;
; ;故A错误;
;故A错误;

 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,1.12L氦气所含原子数为0.1NA |
| B、1.6gNH2-离子所含质子数为NA |
| C、22.4LHCI溶于水,溶液中H数为NA |
| D、9gD2O所含的中子数为4.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CH2=CH2+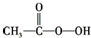 (过氧乙酸)→ (过氧乙酸)→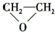 +CH3COOH +CH3COOH | ||
B、CH2=CH2+Cl2+Ca(OH)2→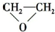 +CaCl2+H2O +CaCl2+H2O | ||
C、2CH2=CH2+O2
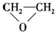 | ||
D、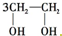
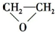 +HOCH2CH2-O-CH2CH2OH+2H2O +HOCH2CH2-O-CH2CH2OH+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入浓硫酸后再小心常压蒸馏 |
| B、各仪器连接处的橡皮塞应塞紧防止漏气 |
| C、加入浓硫酸后再减压蒸馏 |
| D、加入浓硫酸后再加压蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、x≥1.5 | B、x=1.5 |
| C、x≤1.5 | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某分子的球棍模型如图所示.已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连.下列有关说法中错误的是 ( )
某分子的球棍模型如图所示.已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连.下列有关说法中错误的是 ( )| A、X原子可能为第ⅤA族元素 |
| B、Y原子一定为第ⅠA族元素 |
| C、该分子中,既含极性键,又含非极性键 |
| D、从圆球的大小分析,该分子可能为N2F4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com