
| A、加入浓硫酸后再小心常压蒸馏 |
| B、各仪器连接处的橡皮塞应塞紧防止漏气 |
| C、加入浓硫酸后再减压蒸馏 |
| D、加入浓硫酸后再加压蒸馏 |


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
| A、煤等化石燃料是可再生能源,提高物质的燃烧效率对于节约能源十分重要 |
| B、需要加热才能发生的反应一定是吸热反应 |
| C、强电解质溶液的导电能力一定强 |
| D、化合物不是电解质就是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、羟基与氢氧根有相同的化学式和电子式 |
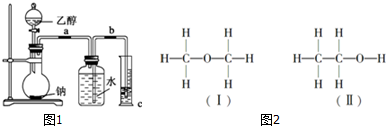
| B、乙醇的官能团是-OH,乙醇是含-OH的化合物 |
| C、常温下,1mol乙醇可与足量的Na反应生成11.2L H2 |
D、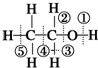 已知乙醇的结构式如图所示,则乙醇催化氧化时断裂的化学键为②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
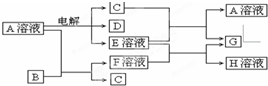
查看答案和解析>>
科目:高中化学 来源: 题型:
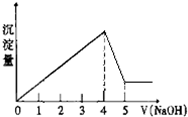 有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量之比为( )
有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量之比为( )| A、1:1 | B、1:2 |
| C、1:3 | D、2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
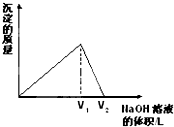 向aL一定浓度的AlCl3溶液中,逐滴加入c mol/L的NaOH溶液,生成沉淀的质量与滴入NaOH溶液体积的关系如图所示.下列代数式中不能表示AlCl3溶液中AlCl3的物质的量浓度的数值的是( )
向aL一定浓度的AlCl3溶液中,逐滴加入c mol/L的NaOH溶液,生成沉淀的质量与滴入NaOH溶液体积的关系如图所示.下列代数式中不能表示AlCl3溶液中AlCl3的物质的量浓度的数值的是( )A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、亚硫酸钠 | B、溴化铁 |
| C、锌粉 | D、铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com