
ЁОЬтФПЁПЙЄвЕКЯГЩАБЕФЗДгІN2+3H2===2NH3ЕФФмСПБфЛЏШчЭМЫљЪО,ЧыЛиД№гаЙиЮЪЬт:
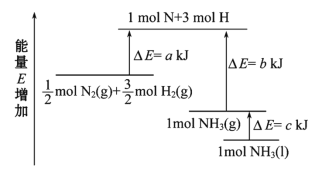
(1)КЯГЩ1 mol NH3(l)________(ЬюЁАЮќЪеЁБЛђЁАЗХГіЁБ)________ kJЕФШШСПЁЃ
(2)вбжЊ:В№ПЊ 1 mol HЁЊHМќЁЂ1 mol NЁЊHМќЁЂ1 mol NЁдN МќЗжБ№ашвЊЕФФмСПЪЧ436 kJЁЂ391 kJЁЂ946 kJЁЃдђЭМжаЕФa=________ kJ;1 mol N2(g) ЭъШЋЗДгІЩњГЩNH3(g)ВњЩњЕФФмСПБфЛЏЮЊ________ kJЁЃ
(3)ЭЦВтЗДгІ 2NH3(l)=== 2N2 (g)+3H2(g) БШЗДгІ2NH3(g)=== 2N2 (g)+3H2(g) ______(ЬюЁАЮќЪеЁБЛђЁАЗХГіЁБ)ЕФШШСП________(ЬюЁАЖрЁБЛђЁАЩйЁБ)ЁЃ
ЁОД№АИЁПЗХГі b+c-a 1127 92 ЮќЪе Жр
ЁОНтЮіЁП
НсКЯИЧЫЙЖЈТЩвдМАЗДгІШШ=ЗДгІЮяЕФЛюЛЏФм-ЩњГЩЮяЕФЛюЛЏФм=ЗДгІЮяЕФМќФмКЭ-ЩњГЩЮяЕФМќФмКЭЗжЮіХаЖЯЁЃ
(1) ЗДгІЮяЕФзмФмСПДѓгкЩњГЩЮяЕФзмФмСПЃЌДЫЗДгІЮЊЗХШШЗДгІЃЌдђгЩФмСПБфЛЏЭМЃЌКЯГЩ1molNH3(l)дђЗХГіЕФШШСПЕШгк(b+c-a)kJЃЛ
(2) ЩЯЭМжаЕФaЕШгкЖЯСб0.5molЕЊЦјКЭ1.5molЧтЦјЫљЮќЪеЕФШШСПЃЌМД(946ЁС0.5+436ЁС1.5)kJ=1127kJЃЛ1molN2(g)ЭъШЋЗДгІдђЯћКФ3molЧтЦјЩњГЩ2molNH3(g)ВњЩњЕФФмСПБфЛЏЮЊ(946+436ЁС3-391ЁС6)kJ=-92kJЃЛ
(3) вђЮЊКЯГЩNH3дђЗХГіШШСПЃЌЫљвдАБЦјЗжНтдђЮќЪеШШСПЃЌгжвКЬхАБЦјзЊЛЏЮЊЦјЬЌЛЙвЊЮќШШЃЌЫљвдвКЬЌАБЗжНтЮќЪеЕФШШСПБШЦјЬЌАБЮќЪеЕФШШСПЖрЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЪЕбщаЁзщгУЯТСазАжУжЦБИфхБНЃЌЯТСаЫЕЗЈДэЮѓЕФЪЧ
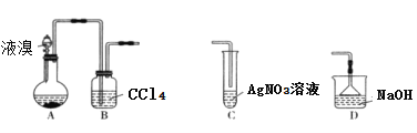
A. зАжУAжаГЄВЃСЇЕМЙмНіЦ№РфФ§ЛиСїзїгУЃЌзАжУBжаЕФЪЕбщЯжЯѓЪЧCCl4гЩЮоЩЋБфГШЩЋ
B. ШєзАжУBКѓСЌНгзАжУCЃЌзАжУCжаЩњГЩЕЛЦЩЋГСЕэЃЌПЩжЄУїзАжУAжаЗЂЩњШЁДњЗДгІ
C. ШєзАжУBКѓСЌНгзАжУDЃЌдђзАжУDЕФзїгУЪЧЮќЪеЮВЦј
D. ЯђЗДгІКѓЕФзАжУAжаМгШыNaOHШмвКЃЌеёЕДОВжУЃЌЯТВуЮЊЮоЩЋгЭзДвКЬх
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПТШдзгЖдO3ЕФЗжНтгаДпЛЏзїгУЃК
O3ЃЋCl === ClOЃЋO2ЁЁІЄH1
ClOЃЋO === ClЃЋO2ЁЁІЄH2
ДѓЦјГєбѕВуЕФЗжНтЗДгІЪЧO3ЃЋO===2O2ЁЁІЄHЃЌИУЗДгІЕФФмСПБфЛЏШчЭМЃК
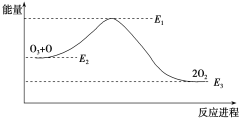
ЯТСаа№ЪіжаЃЌе§ШЗЕФЪЧ(ЁЁЁЁ)
A. ЗДгІO3ЃЋO===2O2ЕФІЄHЃНE1ЃE3
B. O3ЃЋO===2O2ЪЧЮќШШЗДгІ
C. ІЄHЃНІЄH1ЃЋІЄH2
D. 2O2===O3ЃЋO ЪЧЗХШШЗДгІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁППЦбЇМвдЄбдЃЌШМСЯЕчГиНЋЪЧ21ЪРМЭЛёЕУЕчФмЕФживЊЭООЖЁЃНќМИФъПЊЗЂЕФМзЭщШМСЯЕчГиВЩгУВЌзїЕчМЋДпЛЏМСЃЌгУKOHзїЮЊЕчГижаЕФЕчНтвКЃЌЦфЙЄзїдРэЕФЪОвтЭМШчЯТЃК
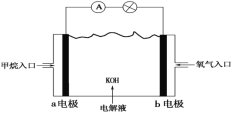
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)МзЭщШМСЯЕчГиЕФФмСПзЊЛЏжївЊаЮЪНЪЧ__________________ЁЃ
(2)Pt(a)ЕчМЋЪЧЕчГиЕФ________МЋЃЌЕчМЋЗДгІЪНЮЊ________________ЃЛPt(b)ЕчМЋЗЂЩњ________ЗДгІ(ЬюЁАбѕЛЏЁБЛђЁАЛЙдЁБ)ЃЌЕчМЋЗДгІЪНЮЊ________________ЁЃ
(3)ЕчГиЕФзмЗДгІЗНГЬЪНЮЊ_______________________________ЁЃ
(4)ШчЙћИУЕчГиЙЄзїЪБЕчТЗжаЭЈЙ§4 molЕчзгЃЌдђЯћКФЕФCH4га________molЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁППЇЗШЫсОпгажЙбЊЙІаЇЃЌДцдкгкЖржжжавЉжаЃЌЦфНсЙЙМђЪНШчЯТЭМЃЌЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
![]()
A. ПЇЗШЫсПЩвдЗЂЩњШЁДњЁЂМгГЩЁЂбѕЛЏЁЂѕЅЛЏЁЂМгОлЗДгІ
B. 1mol ПЇЗШЫсзюЖрФмгы5 mol H2ЗДгІ
C. ПЇЗШЫсЗжзгжаЫљгадзгПЩФмЙВУц
D. ЗфНКЕФЗжзгЪНЮЊC17H16O4ЃЌдквЛЖЈЬѕМўЯТПЩЫЎНтЩњГЩПЇЗШЫсКЭвЛжжвЛдЊДМAЃЌдђДМA ЕФЗжзгЪНЮЊC8H10O
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌЗжБ№ЯђЬхЛ§ЯрЭЌЁЂХЈЖШОљЮЊ1 molЃЏLЕФHAЁЂHBСНжжЫсШмвКжаВЛЖЯМгЫЎЯЁЪЭЃЌЫсШмвКЕФpHгыЫсШмвКХЈЖШЕФЖдЪ§(lg C)МфЕФЙиЯЕШчЭМЁЃЯТСаЖдИУЙ§ГЬЯрЙиЗжЮіе§ШЗЕФЪЧ
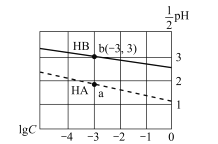
A. HBЕФЕчРыГЃЪ§(KA)Ъ§СПМЖЮЊ10-3
B. ЦфФЦбЮЕФЫЎНтГЃЪ§(Kh)ДѓаЁЙиЯЕЪЧЃКNaB>NaA
C. aЁЂbСНЕуШмвКжаЃЌЫЎЕФЕчРыГЬЖШb<a
D. ЕБlg C= -7ЪБЃЌСНжжЫсШмвКОљгаpH=7
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТЭМБэЪОЩјЭИзїгУзАжУЭМЃЌЦфжаАыЭИФЄЮЊАђызФЄЃЌМзЁЂБћзАжУжаAЁЂBЁЂaЁЂbШмвКХЈЖШЗжБ№гУMAЁЂMBЁЂMaЁЂMbБэЪОЃЌввЁЂЖЁзАжУЗжБ№БэЪОвЛЖЮЪБМфКѓМзЁЂБћзАжУЕФзДЬЌЃЌвКУцЩЯЩ§ЕФИпЖШЗжБ№ЮЊh1ЁЂh2ЁЃШчЙћAЁЂBЁЂaЁЂbОљЮЊесЬЧШмвКЃЌЧвMA>MBЃЌMaЃНMb>MAЃЌдђДяЕНЦНКтКѓ(ЁЁЁЁ)


A. h1>h2ЁЂMa>MbB. h1>h2ЁЂMa<Mb
C. h1<h2ЁЂMa<MbD. h1<h2ЁЂMa>Mb
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌЯТСаИїзщРызгдкжИЖЈШмвКжавЛЖЈФмДѓСПЙВДцЕФЪЧ
A. ЪЙМзЛљГШБфКьЩЋЕФШмвКЃКNa+ЁЂCu2+ЁЂClOЃЁЂClЃ
B. 0.1 molЁЄL-1 Na2CO3ШмвКЃКKЃЋЁЂAlO![]() ЁЂClЃЁЂSO42-
ЁЂClЃЁЂSO42-
C. 0.1 molЁЄL-1 (NH4)2Fe(SO4)2ШмвКжаЃКH+ЁЂAl3+ЁЂClЃЁЂNO![]()
D. KW/c(HЃЋ)ЃН0.1 molЁЄL-1ЕФШмвКжаЃКCa2+ЁЂNH4+ЁЂCH3COOЃЁЂHCO![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМзЭщЁЂввЯЉЁЂЛЗбѕввЭщЁЂЖЁЭщЖМЪЧживЊЕФЛЏЙЄдСЯЃЌгУЭОЙуЗКЃЌЛиД№ЯТСаЮЪЬтЃК
вбжЊЃКЂёЃЎ2CH2=CH2(g)+O2(g)2![]() (g) ІЄH1ЃМ0
(g) ІЄH1ЃМ0
ЂђЃЎCH2=CH2(g)+3O2(g)2CO2(g)+2H2O(l) ІЄH2
ЂѓЃЎ2![]() (g) +5O2(g) 4CO2(g)+4H2O(l) ІЄH3
(g) +5O2(g) 4CO2(g)+4H2O(l) ІЄH3
(1)ШєЗДгІЂѓЪЧдквЛЖЈЮТЖШЯТПЩздЗЂНјааЃЌдђІЄH3______(ЬюЁАЃОЁБЁАЃМЁБЛђЁА=ЁБ)0ЁЃ
(2)ШШжЕЪЧБэЪОЕЅЮЛжЪСПЕФШМСЯЭъШЋШМЩеЪБЫљЗХГіЕФШШСПЃЌЪЧШМСЯжЪСПЕФвЛжжживЊжИБъЁЃвбжЊввЯЉЕФШШжЕЮЊ50.4kJЁЄg-1ЃЌдђЁїH2=________kJЁЄmol-1ЁЃ
(3)ЪЕбщВтЕУ2CH2=CH2(g)+O2(g)2![]() (g) ІЄH1ЃМ0жаЃЌvе§=kе§ЁЄc2(CH2=CH2)ЁЄc(O2)ЃЌvФц=kФцЁЄc2(
(g) ІЄH1ЃМ0жаЃЌvе§=kе§ЁЄc2(CH2=CH2)ЁЄc(O2)ЃЌvФц=kФцЁЄc2(![]() )(kе§ЁЂkФцЮЊЫйТЪГЃЪ§ЃЌжЛгыЮТЖШгаЙи)ЁЃ
)(kе§ЁЂkФцЮЊЫйТЪГЃЪ§ЃЌжЛгыЮТЖШгаЙи)ЁЃ
ЂйДяЕНЦНКтКѓЃЌНіЩ§ИпЮТЖШЃЌkе§діДѓЕФБЖЪ§________(ЬюЁАДѓгкЁБЁАаЁгкЁБЛђЁАЕШгкЁБ) kФцдіДѓЕФБЖЪ§ЁЃ
ЂкШєдк1LЕФУмБеШнЦїжаГфШы1mol CH2=CH2(g)КЭ1mol O2(g)ЃЌдквЛЖЈЮТЖШЯТжЛЗЂЩњЗДгІЂёЃЌОЙ§10min ЗДгІДяЕНЦНКтЃЌCH2=CH2(g)ЕФзЊЛЏТЪЮЊ40%ЃЌдђ0~10minФкЃЌv(O2)=_________ЃЌ![]() =___________(БЃСєСНЮЛгааЇЪ§зж)ЁЃ
=___________(БЃСєСНЮЛгааЇЪ§зж)ЁЃ
(4)ЯТСагаЙиЛЗбѕввЭщжЦБИЕФЫЕЗЈе§ШЗЕФЪЧ________(ЬюзжФИ)ЁЃ
AЃЎгЩЭМ1ПЩжЊЃЌНјСЯЦјЬхЕФГѕЪМЮТЖШЖдЛЗбѕввЭщЕФбЁдёадгАЯьВЛДѓЃЌПЩЕУГіввЯЉЕФзЊЛЏТЪЪмГѕЪМЮТЖШЕФгАЯьВЛДѓ
BЃЎгЩЭМ2ПЩжЊЃЌдСЯЦјЕФСїЫйМгПьЃЌввЯЉзЊЛЏТЪЯТНЕЃЌжївЊЪЧдСЯЦјгыДпЛЏМСНгДЅЪБМфЙ§ЖЬдьГЩ
CЃЎШєНјСЯЦјжабѕЦјБШР§діДѓЃЌЛЗбѕввЭщВњТЪНЕЕЭЃЌЦфжївЊдвђЪЧВПЗжввЯЉЁЂЛЗбѕввЭщзЊЛЏЮЊЖўбѕЛЏЬМКЭЫЎ
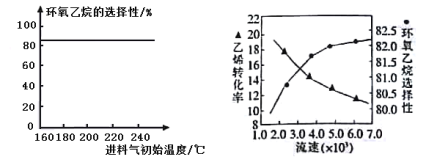
ЭМ1ЛЗбѕввЭщбЁдёадгыНјСЯЦјЬхГѕЪМЮТЖШЙиЯЕ ЭМ2ввЯЉзЊЛЏТЪ-ЛЗбѕввЭщбЁдёадгыНјСЯЦјЬхСїЫйЙиЯЕ
(5)вЛжжвдЬьШЛЦјЮЊЮяШМСЯЕФЙЬЬхбѕЛЏЮяШМСЯЕчГиЕФдРэШчЭМЫљЪОЃЌЦфжаYSZЮЊ6%ЁЋ10%Y2O3ВєдгЕФZrO2ЙЬЬхЕчНтжЪЁЃ
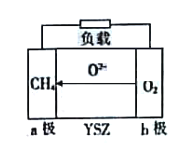
aМЋЩЯЕФЕчМЋЗДгІЪНЮЊ_____________ЃЛШєЕчТЗжазЊвЦ0.1molЕчзгЃЌдђЯћКФБъзМзДПіЯТCH4ЕФЬхЛ§ЮЊ_____________ LЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com