
【题目】下列关于共价键的说法,正确的是
A.分子内部一定会存在共价键
B.由非金属元素组成的化合物内部一定全是共价键
C.非极性键只存在于双原子单质分子中
D.离子化合物的内部可能存在共价键
科目:高中化学 来源: 题型:
【题目】合成药物中间体M的流程如下。
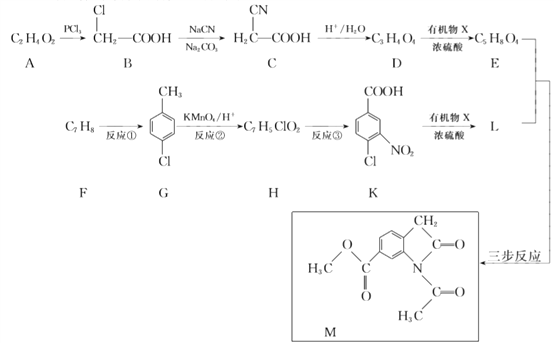
已知:
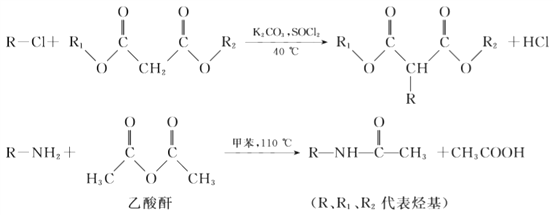
(1)A的名称是________。
(2)B中含有的官能团是________。
(3)D的结构简式是________。
(4)反应①的化学方程式是________。
(5)反应②的反应类型是________。
(6)反应③的试剂和条件是________。
(7)由K生成L反应的化学方程式是________
(8)
写出中间产物的结构简式: 中间产物Ⅰ ______ , 中间产物Ⅱ ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于钠的说法中错误的是
A. 金属钠有强的还原性
B. 钠可以从硫酸铜溶液中还原出铜单质
C. 钠在氯气中燃烧产生大量的白烟
D. 钠元素在自然界中都是以化合态存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现欲用98%的浓硫酸(密度为1.84g·cm-3)配制浓度为1mol·L-1的稀硫酸480mL。
(1)从下列用品中 选出实验所需要的仪器________________(填写序号)
A.1000mL烧杯 B.100mL烧杯 C.10mL量筒 D.50mL量筒
E.500mL容量瓶 F.1000mL容量瓶 G.广口瓶 H.托盘天平
(2)除选用上述仪器外,还缺少的必要仪器或用品是_______________________
(3)需取用浓硫酸的体积为________mL (结果保留一位小数)
(4)配制时,一般可分为以下几个步骤,请在下列横线填写所缺步骤的名称:
计算、称量、溶解、冷却、转移、洗涤、转移、_______、摇匀。
(5)下列情况中,会使所配溶液的浓度偏低的是________
A.将量筒中的浓硫酸转入烧杯后,用水洗涤量筒,将洗液也转入在烧杯中
B.稀释浓硫酸后立即转入容量瓶
C.定容时加水不慎超过刻度线
D.定容时仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: ①亚硝酸钠(NaNO2)是一种食品添加剂,为无色、无气味的同体,具有防腐和抗氧化作用。②AgNO2是一种微溶于水、易溶于酸的浅黄色固体。
I.问题探究
(1)人体正常的血红蛋白中应含Fe2+,误食亚硝酸盐(如NaNO2)会致使机体组织缺氧,出现青紫而中毒,原因是___________。若发生中毒时,你认为下列物质有助于解毒的是____(填字母)。
A.牛奶 B.Mg(OH)2 C.维生素C D.小苏打
(2)由于亚硝酸钠和食盐性状相似,曾多次发生过将NaNO2误当食盐食用的事件。要区别NaNO2和NaCl两种固体,你需用的试剂是_______________。
II.实验测定
为了测定某样品中NaNO2的含量,某同学进行如下实验:
①称取样品ag,加水溶解,配制成100mL溶液。
②取25.00mL溶液于锥形瓶中,用0.0200mol/LKMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液VmL。
(1)上述实验①所需玻璃仪器除玻璃棒、胶头滴管之外还有________。
(2)在进行滴定操作时,KMnO4溶液盛装在______(填“酸式”或“碱式”)滴定管中。当滴入最后一滴溶液,________时达到滴定终点。
(3)滴定过程中发生反应的离子方程式是________;测得该样品中NaNO2的质量分数为_____。
(4)若滴定管未用KMnO4标准溶液润洗就直接注入,则测定结果______(填“偏大”、“偏小”或“无影响”,下同);若滴定过程中刚出现颜色变化就停止滴定,则测定结果________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是
选项 | A | B | C | D |
实验 | 用CCl4提取溴水中的Br2 | 从食盐水中提取NaCl固体 | 从KI和I2的固体混合物中回收I2 | 配制100 mL 0.100 0 mol·L-1 K2Cr2O7溶液 |
装置或仪器 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁泥是硼镁矿生产硼砂晶体(Na2B4O7·10H2O)时的废渣,其主要成分是MgO,还含有Na2B4O7、CaO、Fe2O3、FeO、MnO、SiO2等杂质。以硼镁泥为原料制取MgSO4·7H2O的工艺流程如下:
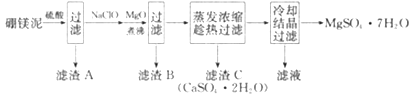
回答下列问题:
(1)Na2B4O7·10H2O中B的化合价为_______;Na2B4O7可制备强还原剂NaBH4,写出NaBH4的电子式:_______。
(2)滤渣A中除含有H3BO3外。还含有_______;加入硫酸时Na2B4O7发生反应的化学方程式为_______。
(3)滤渣B中含有不溶于稀盐酸,但加热时能溶于浓盐酸的黑色固体,写出生成黑色固体的离子方程式:_______;加入MgO的目的是_______。
(4)碱性条件下,阴极上电解NaBO2溶液也可制得硼氢化钠,其电极反应式为_______;“有效氢含量”(即:每克含氢还原剂的还原能力相当于多少克H2的还原能力)可用来衡量含氢还原剂的还原能力,则NaBH4的有效氢含量为_______(保留2位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①H2 ②铝 ③CaO固体 ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦熔融的KNO3 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质之间可发生离子反应:H++OH﹣=H2O,该离子反应对应的化学方程式为____________________________________。
(2)⑩在水中的电离方程式为___________________________。
(3)以上属于电解质的共有____________种。
(4)将少量的④通入⑥的溶液中反应的离子方程式为___________________________。
(5)配平② 与 ⑨发生反应的化学方程式,并用双线桥法标明该反应中电子转移的方向和数目____Al + ___HNO3 = ___Al(NO3)3 + ___NO↑ +__ ______ ;当有8.1g Al发生反应时,转移电子的物质的量为__________mol,HNO3的作用是酸和氧化剂其物质的量之比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近热播剧《外科风云》中利多卡因药物引发的医疗问题扑朔迷离,盐酸利多卡因(F)葡萄糖注射液,可用于抗心律失常。其合成路线如下:
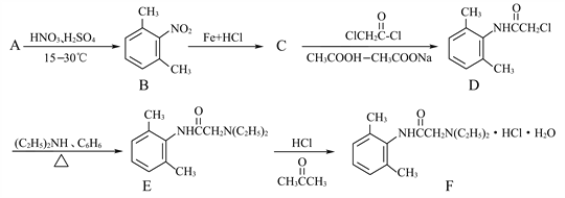
(1)写出A的名称______________________。
(2)C的结构简式为______________________.
(3)B有多种同分异构体,符合以下条件的B的同分异构体(不包括B本身)共有_______________种,请写出其中一种的结构简式_____________________。
①苯环上共有三个取代基 ②与碳酸氢钠溶液反应可放出CO2气体
(4)对氨基苯甲酸是机体细胞生长和分裂所必需的叶酸的组成成分。现以甲苯为原料,结合题干有关信息,补充完成以下合成路线:____________
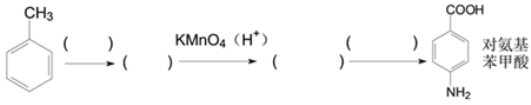
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com