
【题目】下列物质中,含有共价键的离子化合物是
A. NH3 B. HCl C. NaOH D. NaCl
科目:高中化学 来源: 题型:
【题目】常温下,水存在H2O![]() H++OH--Q的平衡,下列叙述一定正确的是
H++OH--Q的平衡,下列叙述一定正确的是
A. 向水中滴入少量稀盐酸,平衡逆向移动,Kw减小
B. 将水加热,Kw增大,pH减小
C. 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D. 向水中加入少量固体NH4Cl,c(H+)=10-7mol/L,Kw不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经研究发现白蚁信息素有:![]() (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯),![]() (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH==CH—CH==CH(CH2)8CH3。下列说法不正确的是
(3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH==CH—CH==CH(CH2)8CH3。下列说法不正确的是
A.2,4-二甲基1庚烯的分子式为C9H18
B.2,4-二甲基-1-庚烯与3,7-二甲基-1-辛烯互为同系物
C.以上三种信息素均能使溴的四氯化碳溶液褪色
D.1 mol家蚕的性信息素与1 mol Br2加成,产物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
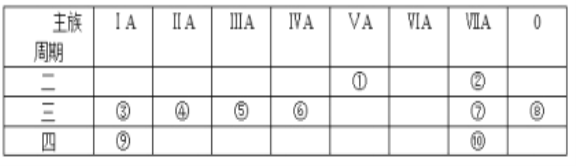
(1)在③~⑦元素中,原子半径最大的元素是________,其离子结构示意图为________
(2)元素的最高价氧化物对应的水化物中酸性最强的物质是________,碱性最强的物质是_______,呈两性的氢氧化物是________;
(3)按要求写出下列两种物质的电子式:①的氢化物________;⑨的最高价氧化物对应的水化物________;
(4)在⑦与⑩的单质中,化学性质较活泼的是_______,可用什么化学反应说明该事实(写出反应的化学方程式):_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液态化合物AB会发生微弱的自身电离,电离方程式为AB![]() A++B-,在不同温度下其平衡常数为K(25 ℃)=1.0×10-14,K(35 ℃)=2.1×10-14。则下列叙述正确的是 ( )。
A++B-,在不同温度下其平衡常数为K(25 ℃)=1.0×10-14,K(35 ℃)=2.1×10-14。则下列叙述正确的是 ( )。
A.c(A+)随温度升高而降低
B.在35 ℃时,c(A+)>c(B-)
C.AB的电离程度(25 ℃)>(35 ℃)
D.AB的电离是吸热过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度时,100 mL 0.01 mol/L的醋酸溶液与10mL 0.l mol/L的醋酸溶液相比较,下列数值前者大于后者的是
A. 中和时所需NaOH的量 B. OH-的物质的量浓度
C. 与Mg反应的起始速率 D. 溶液中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。

完成下列填空:
(1)写出电解饱和食盐水的离子方程式:___________________________________________。
(2)离子交换膜的作用为__________________、___________________________。
(3)精制饱和食盐水从图中________(选填“a”、“b”、“c”或“d”)位置补充,氢氧化钠溶液从图中________位置流出。
Ⅱ.(4)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3H2O.已知:
a.常温下,醋酸和NH3H2O的电离平衡常数均为1.74×10﹣5;
b.CH3COOH+NaHCO3═CH3COONa+CO2↑+H2O.
则CH3COONH4溶液呈_____性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈_____性,NH4HCO3溶液中物质的量浓度最大的离子是_____(填化学式).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com