
����Ŀ����1������ʹ�û�ѧ֪ʶ�������������
�ټ��þ�ˮ����ʹ�û���̿��ˮ���������˻���̿��____________________�ԡ�
����ʳ�ؽ����λ�ʹ���ж���Ӧ�ڷ�_______________���ⶾ
�����г�������������ѩ�������к�Ӧ��ʱ���ɣ�����һ��ʱ�����Щ������ֺ���ɫ��ߣ���Ҫԭ������������___________________����ѧ��ʴ���绯ѧ��ʴ����
��Ϊ��ֹ��ɫ��Ⱦ���Ͼɵ�������Ͷ�뵽����ͼ��ʾ������Ͱ�ڣ��ñ�־��ʾ����_____________��

��2������Ӫ����������ҩ�DZ�֤���彡������Ҫ��֤��С����ij�����Ͳ�������ͼ��ʾ��
����ˡ��ཷ����˿�������������۲���ɡ������廨�⡢������ե����
�ٲ����и���֬����ʳ����______________��
�ڼ����к��зḻ�ĵ����ʣ���������Ҫ��Ӫ����֮һ������������������ȫˮ��IJ�����___________�������ƣ���
������˿�е���ҪӪ�������ǵ��ۣ�д�����۵Ļ�ѧʽ__________���ཷ�����������߲˸���ά����C��ά����C �ֳ�____________�ᣬ�õ�����Һ�͵�ˮ�ɼ���ά����C��_________�ԡ�
�ܵ�����θ����ڹ���ʱ��ҽ���Ὠ��������³���ҩ���е�__________������ĸ����
a.��˾ƥ�� b.��ù��Ƭ C.������������Ƭ d.�ϳɿ���ҩ
��3�����·�չ��Դ�����ϼ������ƶ��������Ľ�����
�ٽ��գ��п�Ժ�����������」��������о�Ա�Ŷӷ����˶�����̼��Чת���¹��̣�ͨ�����һ�����Ͷ�ܸ��ϴ������״�ʵ����CO2 ֱ�Ӽ�����ȡ������ֵ���ͣ���������C5H12��д���÷�Ӧ�ķ���ʽ____________________________________��
�ڿ�ȼ���ֳ���Ȼ��ˮ�����һ�ּ����ˮ�����ڵ��¸�ѹ����½����һ��Ļ����������������ȡ��ú��ʯ�͵�����Դ��д����ȼ����CH4��nH2O���ڿ����г��ȼ�յķ���ʽ__________��
���й���ѧԺ����ֲ���о����������Ŷӽ������������������オ������ȡ���ش�ͻ�ơ���������������ù���ܶ����ϵ����オ�����á�д������ϩ���ϵĽṹ��ʽ________________________��
���𰸡� ������ ţ�̻� �绯ѧ��ʴ �ɻ������� �����廨�� ������ (C6H10O5)n ����Ѫ�� ��ԭ�� c 5CO2 +16 H2 ![]() C5H12 +10H2O CH4��nH2O+2 O2= CO2 + (n+2 )H2O
C5H12 +10H2O CH4��nH2O+2 O2= CO2 + (n+2 )H2O ![]()
���������ٻ���̿�Ľṹ�������ɶ�սṹ���ܹ����������ã���ȷ�𰸣������ԡ�
���ؽ����λ�ʹ�����ʱ��ԣ�ţ�̻������ڵ����ʣ�Ӧ�÷���ţ�̻����ⶾ����ȷ�𰸣�ţ�̻���
������̼������ԭ��أ�����������ʧ���ӣ���Ϊ�������ӣ�����Һ�б�Ϊ���������������������б�����Ϊ��������������ʧˮ��Ϊ����������ɫ��ߣ�����Ҫԭ��Ϊ�������˵绯ѧ��ʴ����ȷ�𰸣��绯ѧ��ʴ��
����ȷ�����ɻ���������
��2����������֬�������϶࣬��˲����и���֬����ʳ���Ǻ����廨�⣬��ȷ�𰸣������廨�⡣
�ڵ���������������ȫˮ��IJ���Ϊ���ְ����ᣬ��ȷ�𰸣������ᡣ
�۵��۵Ļ�ѧʽ(C6H10O5)n ��ά����C �ֳƿ���Ѫ����������Һ�͵�ˮ�����Һ����ɫ��ά����C���л�ԭ�������ѵԭΪ����������ɫ��Һ��ɫ����ȷ�𰸣�(C6H10O5)n������Ѫ���ԭ��
��θ����Ҫ�ɷ�Ϊ���ᣬ��Ҫ�ü����������к����ᣬ������������Ƭ���ܹ������ᷴӦ���ﵽ�к͵�Ŀ�ģ���ȷѡ�C��
��3����CO2������������Ӧ����C5H12������ԭ���غ���ɣ��÷�Ӧ�ķ���ʽ5CO2 +16 H2 ![]() C5H12 +10H2O ����ȷ����5CO2 +16 H2
C5H12 +10H2O ����ȷ����5CO2 +16 H2 ![]() C5H12 +10H2O��
C5H12 +10H2O��
�ڿ�ȼ����CH4��nH2O���ڿ����г��ȼ�����ɶ�����̼��ˮ������ԭ���غ���ɣ�����ʽ. CH4��nH2O+2 O2= CO2 + (n+2 )H2O ����ȷ����CH4��nH2O+2 O2= CO2 + (n+2 )H2O��
����ϩ�����Ӿ۷�Ӧ���ɾ���ϩ���ϣ�����ϩ���ϵĽṹ��ʽΪ![]() ����ȷ�𰸣�
����ȷ�𰸣� ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ũ��Ϊ0.100 mol��L��1��NaOH��Һ�ֱ���μ��뵽20.00 mL 0.100 0 mol��L��1��HX��HY��Һ����pH��NaOH��Һ����ı仯��ͼ������˵����ȷ����(����)
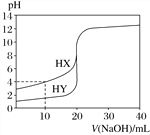
A. V(NaOH)��10.00 mLʱ��������Һ��c(X��)��c(Y��)
B. V(NaOH)��10.00 mLʱ��c(X��)��c(Na��)��c(HX)��c(H��)��c(OH��)
C. V(NaOH)��20.00 mLʱ��c(OH��)��c(H��)��c(Na��)��c(X��)
D. pH��7ʱ��������Һ��c(X��)��c(Na��)��c(Y��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ƿ�չ�е�����Դ���������ð�������Ʊ��������Ӧ���������ڡ��ش��������⣺
��1�������������Ʊ�H2O2����֪��
H2(g)+A(l)=B(l) ��H1
O2(g)+B(l)=A(l)+H2O2(l) ��H2
����A��BΪ�л������Ӧ��Ϊ�Է���Ӧ����H2(g)+ O2(g)= H2O2(l)�Ħ�H____0(�>������<����=��)��
��2���ں��º��ݵ��ܱ������У�ij���ⷴӦ��MHx(s)+yH2(g) ![]() MHx+2y(s) ��H<0�ﵽ��ѧƽ�⡣�����й�������ȷ����________��
MHx+2y(s) ��H<0�ﵽ��ѧƽ�⡣�����й�������ȷ����________��
������������ѹǿ���ֲ���
������y mol H2ֻ��1 mol MHx
�������£��÷�Ӧ��ƽ�ⳣ������
������������ͨ��������������v(����)>v(����)
��3�����������ĸ�����Ҳ����������Դ����ⷨ��ȡ�й㷺��;��Na2FeO4��ͬʱ���������Fe+2H2O+2OH![]() FeO42+3H2��������ԭ����ͼ1��ʾ��װ��ͨ������缫���������Ϻ�ɫ��FeO42�����缫�����ݲ�����������������ҺŨ�ȹ��ߣ����缫����������ɫ���ʡ���֪��Na2FeO4ֻ��ǿ�����������ȶ����ױ�H2��ԭ��
FeO42+3H2��������ԭ����ͼ1��ʾ��װ��ͨ������缫���������Ϻ�ɫ��FeO42�����缫�����ݲ�����������������ҺŨ�ȹ��ߣ����缫����������ɫ���ʡ���֪��Na2FeO4ֻ��ǿ�����������ȶ����ױ�H2��ԭ��

�ٵ������У��뽫�������������弰ʱ�ų�����ԭ����_______��
��c(Na2FeO4)���ʼc(NaOH)�ı仯��ͼ2���������N��c(Na2FeO4)�������ֵ��ԭ��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ�飺
����Fe2��SO4��3��CuSO4�Ļ��Һ�м���������ۣ���ַ�Ӧ���к�ɫ�������������ˡ�
��ȡ������Һ�������еμ�KSCN��Һ���۲�����
�ж�����˵����ȷ����
A. ������Cu2+>Fe3+
B. �������ù���ֻ��ͭ
C. ������Һ����Cu2+��Fe2+
D. ���в���۲쵽��Һ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C����ǿ����ʣ�������ˮ�е�������������±���ʾ��
������ | Cu2+ Na+ |
������ | NO3- SO42- Cl- |
��ͼ1��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��������A�� B�� C������Һ���缫��Ϊʯī�缫����ͨ��Դ������һ��ʱ��������c�缫����������32g�������¸��ձ�����Һ��pH����ʱ�䣨t���Ĺ�ϵ��ͼ2��ʾ���ݴ˻ش��������⣺

��1��MΪ��Դ��__________�����������������
��2��д�����ձ��з�Ӧ�Ļ�ѧ����ʽ____________________��
��3������缫f�����ɵ������ڱ�״���µ����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ˮ�ڽ���ת¯ǰ����������ʱ�����ķ�����������ij��������������������Ҫ�ɷ�ΪFe��CaO������MgO��Al2O3��SiO2��Ϊԭ�����Ʊ��ߴ��������������������������
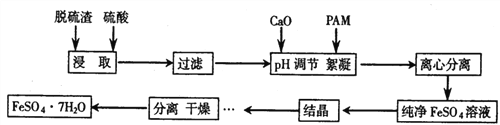
��1���ڽᾧ��������pH���¶ȶ������������ȵ�Ӱ����ͼ1��ͼ2���������ᾧʱ���˵�����Ϊ_____��
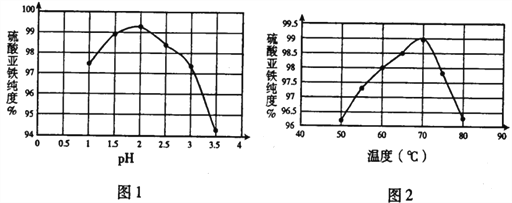
��2�����ķ������30���¸���6h��øߴ��������������壬30���¸�����ԭ�������______��
��3��ʵ���ҽ��й��˲���ʱ�����õ��IJ���������_______��
��4����������������������������������������������K2Cr2O7��ˮ��ȡһ��������FeSO4��7H2O ��������KOH��Һ���뵽��K2Cr2O7��ˮ�пɵõ�һ�����Ĵ��Բ���Cr0.5Fe1.5FeO4��������5.00��10-3mol K2Cr2O7�ķ�ˮ����Ҫ���ٿ˵�FeSO4��7H2O��д��������̣���_______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���Ũ��Ϊ0.1000mol/L������ֱ���μ��뵽20.00mL0.1000mol/L������һԪ��MOH��ROH��Һ�У�pH��������Һ����ı仯��ͼ��ʾ������˵����ȷ����

A. pH=10ʱ����Һ����Ũ�ȵĹ�ϵ�ǣ�c(M+)> c(Cl-)> c(MOH) >c(OH-)>c(H+)
B. ������MOH��ROH��Һ�������Ϻ�������ζ���MOHǡ�÷�Ӧʱ����Һ������Ũ��һֱ���ֵĹ�ϵ�ǣ�c(R+)>c(M+)>c(OH-)>c(H+)
C. 10mL<V(HCl)<20mLʱ����Һ����Ũ�ȵĹ�ϵ�ǣ�c(M+)+c(MOH)<c(Cl-)
D. V(HCl)>20mLʱ�������ܴ��ڣ�c(Cl-)>c(M+)=c(H+)>c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��300��ʱ����100mL��H2O��CO2��N2��ɵĻ������ͨ��ʢ������Na2O2���ܱ�������������������ֲ���������ַ�Ӧ��ָ���ԭ�¶�ʱ�����ڵ�ѹǿ��Ϊԭ����4/5����ԭ���������N2���������Ϊ
A. 33.3% B. 40% C. 60% D. 75%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����������������淴ӦA(g)+3B(g) ![]() 2C(g)�ﵽƽ��ı�־����
2C(g)�ﵽƽ��ı�־����
��C������������C�ķֽ�������ȣ��ڵ�λʱ����amol A���ɣ�ͬʱ����3amol B����A��B��C��Ũ�Ȳ��ٱ仯���ܻ���������ѹǿ���ٱ仯���ݻ����������ʵ������ٱ仯����λʱ������amol A��ͬʱ����2amol C����A��B��C�ķ�����Ŀ��Ϊ1:3:2��
A. �ڢݢ� B. �٢ۢ� C. �ڢޢ� D. �ڢۢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com