
【题目】A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Cu2+ Na+ |
阴离子 | NO3- SO42- Cl- |
下图1所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了32g。常温下各烧杯中溶液的pH与电解时间(t)的关系如图2所示。据此回答下列问题:

(1)M为电源的__________极(填“正”或“负”);
(2)写出甲烧杯中反应的化学方程式____________________;
(3)计算电极f上生成的气体在标准状况下的体积_____________。
【答案】 负 2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ 5.6L
2NaOH+H2↑+Cl2↑ 5.6L
【解析】(1)接通电源,经过一段时间后,测得乙中C电极质量增加了32g,说明C电极是阴极,所以连接阴极的电极M是原电池的负极,阴极是铜离子放电;(2)电解时,甲装置中溶液的pH值增大,说明阳极上是放电能力大于氢氧根离子的离子放电,根据表格知,为氯离子,甲中电解质溶液是氯化钠,所以甲装置电解质溶液是氯化钠溶液,电解的总反应式为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;(3)析出铜的物质的量是32g÷64g/mol=0.5mol,转移1.0mol电子,电解过程中丙中pH不变,说明电解质应该是硝酸钠或硫酸钠,f电极是阳极,溶液中的氢氧根放电,电极反应式为4OH――4e-=2H2O+O2↑,所以产生的氧气是1mol÷4=0.25mol,在标准状况下的体积是0.25mol×22.4L/mol=5.6L。
2NaOH+H2↑+Cl2↑;(3)析出铜的物质的量是32g÷64g/mol=0.5mol,转移1.0mol电子,电解过程中丙中pH不变,说明电解质应该是硝酸钠或硫酸钠,f电极是阳极,溶液中的氢氧根放电,电极反应式为4OH――4e-=2H2O+O2↑,所以产生的氧气是1mol÷4=0.25mol,在标准状况下的体积是0.25mol×22.4L/mol=5.6L。


科目:高中化学 来源: 题型:
【题目】为研究某溶液中溶质R的分解速率的影响因素,分别用三份不同初始浓度的R溶液在不同温度下进行实验,c(R)随时间变化如图。下列说法不正确的是( )

A. 25 ℃时,在0~30 min内,R的分解平均速度为0.033 mol·L-1·min-1
B. 对比30 ℃和10 ℃曲线,在50 min时,R的分解百分率相等
C. 对比30 ℃和25 ℃曲线,在0~50 min内,能说明R的分解平均速度随温度升高而增大
D. 对比30 ℃和10 ℃曲线,在同一时刻,能说明R的分解速率随温度升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室按如下装置测定纯碱(含少量NaC1)的纯度。下列说法不正确的是
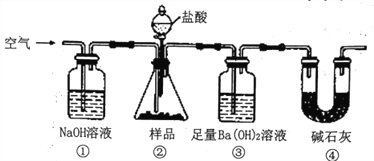
A. 滴入盐酸前,应将装置中含有CO2的空气排尽
B. 装置①、④的作用是防止空气中的CO2进入装置③
C. 必须在装置②、③间添加盛有饱和 NaHCO3溶液的洗气瓶
D. 反应结束时,应再通入空气将装置②中CO2转移到装置③中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是某兴趣小组根据教材实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验。请观察如下图所示实验装置,分析实验原理,并判断下列说法和做法,其中不科学的是( )

A. 甲为小苏打,乙为纯碱
B. 要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球
C. 加热不久就能看到A烧杯的澄清石灰水变浑浊
D. 整个实验过程中都没有发现A烧杯的澄清石灰水变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)(CH3)2CHCH(CH3)2的系统命名为___________________;
(2)有机物的结构可用“键线式”简化表示,CH3-CH=CH-CH3的键线式为________;
(3)下列化合物分子中,在核磁共振氢谱图中能给出一种信号的是(______)
A.CH3CH2CH3 B. CH3COCH2CH3 C.CH3CH2OH D.CH3OCH3
(4)分子式为C2H6O的有机物,有两种同分异构体,乙醇(CH3CH2OH)、甲醚(CH3OCH3),则通过下列方法,不可能将二者区别开来的是 (______)
A.红外光谱 B. 1H核磁共振谱 C.质谱法 D.与钠反应
(5)已知乙烯分子是平面结构, 1,2-二氯乙烯可形成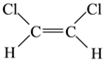 和
和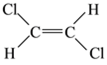 两种不同的空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是(_____)
两种不同的空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是(_____)
A.1-丙烯 B.4-辛烯 C.1-丁烯 D.2-甲基-1-丙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)合理使用化学知识可提高生活质量
①家用净水机常使用活性炭净水,其利用了活性炭的____________________性。
②误食重金属盐会使人中毒,应口服_______________来解毒
③自行车、助力车等雨雪天气骑行后,应及时擦干,否则一段时间后有些零件出现红棕色锈斑,主要原因是铁发生了___________________(化学腐蚀、电化学腐蚀)。
④为防止白色污染,废旧的塑料需投入到贴下图所示的垃圾桶内,该标志表示的是_____________。

(2)均衡营养、合理用药是保证人体健康的重要保证,小明家某次晚餐菜谱如下图所示。
炒青菜、青椒土豆丝、银鱼炖蛋、芹菜香干、红烧五花肉、西红柿榨菜汤
①菜谱中富含脂肪的食物是______________。
②鸡蛋中含有丰富的蛋白质,是人体需要的营养素之一,蛋白质在人体中完全水解的产物是___________(填名称)。
③土豆丝中的主要营养物质是淀粉,写出淀粉的化学式__________。青椒、西红柿等蔬菜富含维生素C,维生素C 又称____________酸,用淀粉溶液和碘水可检验维生素C的_________性。
④当体内胃酸分泌过多时,医生会建议服用以下常用药物中的__________(填字母)。
a.阿司匹林 b.青霉素片 C.复方氢氧化铝片 d.合成抗菌药
(3)创新发展能源、材料技术可推动人类社会的进步。
①近日,中科院大连化物所孙剑、葛庆杰研究员团队发现了二氧化碳高效转化新过程,通过设计一种新型多功能复合催化剂,首次实现了CO2 直接加氢制取高辛烷值汽油,如正戊烷C5H12,写出该反应的方程式____________________________________。
②可燃冰又称天然气水合物,是一种甲烷和水分子在低温高压情况下结合在一起的化合物,被看作是有望取代煤、石油的新能源。写出可燃冰(CH4·nH2O)在空气中充分燃烧的方程式__________。
③中国科学院昆明植物研究所许建初团队近日宣布,在塑料生物降解领域取得重大突破——发现了塔宾曲霉菌能对塑料的生物降解作用。写出聚乙烯塑料的结构简式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1-溴丁烷的原理为CH3CH2CH2CH2OH+NaBr+H2SO4![]() CH3CH2CH2CH2Br+NaHSO4+H2O,根据原理设计实验装置如图1所示(夹持装置已略去)
CH3CH2CH2CH2Br+NaHSO4+H2O,根据原理设计实验装置如图1所示(夹持装置已略去)
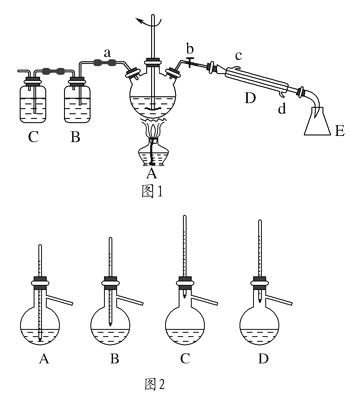
(1)仪器D的名称为________,使用玻璃棒搅拌的目的是__________________。
(2)1-溴丁烷的制备反应中可能有:________、________、溴化氢等副产物生成。熄灭图1中A装置中的酒精灯,打开a,余热会使反应继续进行。B、C装置可检验部分副产物,则B、C装置中所盛放的试剂分别是________、________。
(3)为了精制1-溴丁烷,待烧瓶冷却后,将A装置中的玻璃棒换成温度计,关闭a,打开b,使冷水从________(填“c”或“d”)处流入。对粗产品进行蒸馏提纯时,图2装置中温度计的位置正确的是________(填字母,下同),可能会导致收集到的产品中混有低沸点杂质的装置是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生可逆反应:Ni(s)+4CO(g)![]() Ni(CO)4(g),已知该反应在25℃、80℃时的平衡常数分别为5×104和2,下列说法正确的是( )
Ni(CO)4(g),已知该反应在25℃、80℃时的平衡常数分别为5×104和2,下列说法正确的是( )
A. 上述生成Ni(CO)4(g)的反应为吸热反应
B. 80℃时,测得某时刻Ni(CO)4(g)、CO(g)浓度均为0.5 mol/L,则此时v(正)<v(逆)
C. 恒温恒压下,向容器中再充入少量的Ar,上述平衡将正向移动
D. 恒温时将气体体积缩小到原来的一半,达到新平衡时CO浓度将要减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒是一种熔点很高的金属,具有良好的可塑性和低温抗腐蚀性,有延展性、硬度大,无磁性。广泛应用于钢铁、航空航天、能源、化工等领域。中铝集团 (平果铝业公司)目前使用一种新型工艺,以便从铝业生成的固体废料——赤泥中提取金属钒,具体工艺流程图如下:
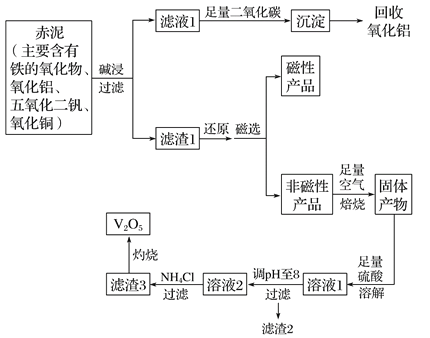
已知:
I.钒有多种价态,其中+5价最稳定。钒在溶液中主要以VO2+和VO3-的形式存在,存在平衡
VO2++H2O![]() VO3-+2H+。
VO3-+2H+。
Ⅱ.部分含钒物质在水中的溶解性如下表所示:
物质 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 难溶 | 难溶 | 易溶 |
Ⅲ.部分离子的沉淀pH值:
Cu2+ | Fe2+ | Fe3+ | |
开始沉淀pH值 | 5.2 | 7.6 | 2.7 |
完全沉淀pH值 | 6.4 | 9.6 | 3.7 |
请回答下列问题:
(1)碱浸步骤中最好选用 。
A.NaOH溶液 B.氨水 C.纯碱溶液
(2)写出滤液1与足量二氧化碳反应的离子方程式 。
(3)磁选步骤得到的磁性产品为 。
(4)溶液1到溶液2的过程中,调节pH值至8有两个目的,一是除去铜离子,二是使 。
(5)滤渣3的主要成分为 ,工业上常用铝热反应法由V2O5冶炼金属钒,请写出反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com