
【题目】向硝酸钠溶液中加入铜粉不发生反应,若再加入下列某溶液时,则铜粉可以逐渐溶解。不符合此条件的物质是 ( )
A. HCl B. NaHSO4 C. ZnSO4 D. Fe(NO3)3
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:

试回答下列问题:
(1)“酸溶”过程中Fe3O4发生反应的离子反应方程式为________________________;
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有_______、玻璃棒和烧杯等;步骤Ⅳ中应选用_______试剂调节溶液的pH(填字母编号)。
A.稀硝酸 B.氢氧化钠溶液 C.高锰酸钾溶液 D.氨水
(3)检验步骤Ⅲ已经进行完全的试剂是_____________________;
(4)步骤Ⅴ的反应温度一般需控制在35℃以下,其目的是_________________________;
(5)步骤Ⅵ中发生反应的化学反应方程式为_____________________________;
(6)欲测定硫铁矿矿渣中Fe元素的质量分数,称取ag样品,充分“酸溶”、“水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体bg,测得该样品中Fe元素的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将13.6g带铁锈的铁片完全溶解于25 mL 14 mol/L热的浓H2SO4中,收集到SO2体积为1.12 L(标准状况〉。将溶液稀释至100 mL,所得溶液遇KSCN溶液时无血红色出现。下列结论正确的是
A. 反应中:转移电子![]() 个 B. 原混合物:
个 B. 原混合物:![]()
C. 反应后:剩余 ![]() D. 所得溶液:
D. 所得溶液:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加徳罗常数的值,下列说法不正确的是( )
A. 9.2g NO2和N2O4的混合物中含氮原子数目为0.2NA
B. 常温常压下,35.5g Cl2与足量的NaOH溶液完全反应,转移的电子数为0.5NA
C. 标准状况下,2.24LNH3与1.6gCH4分子中所含电子数目均为NA
D. 已知反应N2(g)+3H2(g)![]() 2NH3(g)△H=-92.4kJ mol-1,当生成NA个NH3分子时,反应放出的热量小于46.2kJ
2NH3(g)△H=-92.4kJ mol-1,当生成NA个NH3分子时,反应放出的热量小于46.2kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备氯化物时,常用两种方法:①用金属与氯气直接化合制得;②用金属与盐酸反应制得.用以上两种方法都可制得的氯化物是( )
A. AlCl3 B. FeCl3 C. FeCl2 D. CuCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式书写正确的是
A.FeCl2溶液中通入Cl2:Fe2+ +Cl2 === Fe3+ + 2Cl-
B.实验室用固体氯化铵和熟石灰共热制取NH3:
2NH4++Ca(OH)2 === 2NH3↑+ Ca2++H2O
C.FeO与稀HNO3反应:3FeO + 10H+ + NO3- === 3Fe3+ + NO↑+5H2O
D.实验室用石灰石制CO2:CO32- + 2H+ === CO2↑+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧、硫、硒、碲等氧族元素在化合物中常表现出多种氧化态,含氧族元素的化合物在研究和生产中有许多重要用途。请回答以下问题:
(1)氧、硫、硒三元素的第一电离能由大到小的顺序为_______________________(用元素符号回答)。
(2)基态Se原子的价层电子排布式为___________,其原子核外有______________种运动状态不同的电子。
(3)气态SO3为单分子状态,其中S原子的杂化轨道类型为________。若SO3的三聚体(SO3)3的环状结构如图所示,则该结构中S原子的杂化轨道类型为____________________。
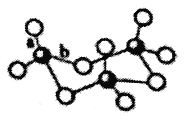
(4)氧族元素的气态氢化物中,H2S的稳定性强于H2Se,原因是________________________________。
(5)氧、硫分别与钙形成两种化合物的晶格能大小为 CaO __________CaS (填“>”,“<”或“=”)。 (6)硫化锌在光导材料、涂料等行业中应用广泛,其晶体结构如图,则该晶体属于________晶体,化学式为__________,若晶体的密度为ρg·cm-3,则晶胞边长为____________cm (阿伏加德罗常数的值用NA表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 60g水晶晶体中,含有“Si—O”键的数目为2NA
B. 14g氮气含有![]() 键的数目为2NA
键的数目为2NA
C. 18g冰中含有的氢键数目为2NA
D. 12g金刚石中含有C—C键的数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鉴别Na2CO3和NaHCO3两种固体,不可以采用的方法是( )
A. 溶于水,加石灰水 B. 加热,将产生的气体通入澄清石灰水
C. 配制成同物质的量浓度的溶液,测pH值 D. 滴加同浓度的盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com