
【题目】已知:2CO(g)+O2(g)=2CO2(g)ΔH=-566kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+![]() O2(g)ΔH=-226kJ/mol
O2(g)ΔH=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是
A. CO的燃烧热为283 kJ
B. 如图可表示由CO生成CO2的反应过程和能量关系
C. 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
D. CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
【答案】C
【解析】A.燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出热量;已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol,一氧化碳的燃烧热为283kJ/mol,故A错误;B.由热化学方程式,2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol,可知图象中一氧化碳和氧气物质的量为1、![]() 物质的量不符合反应物质的物质的量,故B错误;C.固体二氧化碳变化为气体二氧化碳需要吸热,焓变放热是负值,由2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H=-226kJ/mol,所以反应2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H>-532 kJ/mol,故C正确;D.已知:①2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol;②Na2O2(s)+CO2(g)=Na2CO3(s)+
物质的量不符合反应物质的物质的量,故B错误;C.固体二氧化碳变化为气体二氧化碳需要吸热,焓变放热是负值,由2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H=-226kJ/mol,所以反应2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H>-532 kJ/mol,故C正确;D.已知:①2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol;②Na2O2(s)+CO2(g)=Na2CO3(s)+![]() O2(g)△H=-226kJ/mol;依据盖斯定律②×2+①得到:2Na2O2(s)+2CO(g)=2Na2CO3(s)△H=-1018kJ/mol;即Na2O2(s)+CO(g)=Na2CO3(s)△H=-509kJ/mol;CO(g)与Na2O2(s)反应放出
O2(g)△H=-226kJ/mol;依据盖斯定律②×2+①得到:2Na2O2(s)+2CO(g)=2Na2CO3(s)△H=-1018kJ/mol;即Na2O2(s)+CO(g)=Na2CO3(s)△H=-509kJ/mol;CO(g)与Na2O2(s)反应放出![]() ×509 kJ=254.5kJ热量时,反应的一氧化碳物质的量为0.5mol,电子转移数为6.02×1023,故D错误;故选C。
×509 kJ=254.5kJ热量时,反应的一氧化碳物质的量为0.5mol,电子转移数为6.02×1023,故D错误;故选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】25℃时,向20mL 0.1mol/LH2R(二元弱酸)溶液中滴加0.1mol/LNaOH溶液,溶液pH与加入NaOH溶液体积的关系如图所示。下列有关说法正确的是
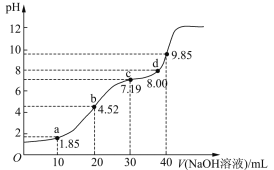
A. a点所示溶液中:c (H2R) + c (HR-)+ c (R2-)=0.lmol/L
B. b点所示溶液中:c (Na+) >c(HR-)> c (H2R)>c(R2-)
C. 对应溶液的导电性:b > c
D. a、b、c、d中,d点所示溶液中水的电离程度最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 化学反应中的能量变化主要是由化学键变化引起的
B. 铝热反应是放热反应,因此不需要加热就能使反应发生
C. 硝酸铵溶于水温度降低,这个变化是吸热反应
D. 化学反应中的能量变化的大小与反应物的质量大小无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检验SO2中是否混有CO2气体,可采用的方法是
A. 通过品红溶液,若品红溶液褪色,则说明混有CO2气体
B. 通过澄清石灰水,若变混浊,则说明混有CO2气体
C. 先通过足量NaOH溶液,再通过澄清石灰水,若变混浊,则说明混有CO2气体
D. 先通过足量KMnO4溶液,再通过澄清石灰水,若变混浊说明混有CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,既属于氧化还原反应,又属于吸热反应的是
A.锌片与稀硫酸的反应 B.灼热的碳与水蒸气的反应
C.甲烷在空气中的燃烧反应 D.Ba(OH)2·8H2O与NH4Cl的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘循环工艺不仅能吸收SO2降低环境污染,同时还能制得氢气,具体流程如下:

下列说法正确的是
A. 分离器中的物质分离操作为过滤
B. 膜反应器中,增大压强有利于提高HI的分解速率和平衡转化率
C. 该工艺中I2和HI的相互转化体现了“碘循环”
D. 碘循环工艺的总反应为2SO2+4H2O+I2 == H2+2H2SO4+ 2HI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大.A、D同主族,可形成离子化合物X;B的氢化物与F的氢化物可反应生成离子化合物Y,且B的单质是空气中含量最高的物质;C原子的最外层电子是次外层电子数的3倍;D、E、F 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水.
(1)B元素的名称是 , B单质的结构式为 .
(2)用电子式表示化合物X的形成过程 .
(3)化合物Y的电子式为 , A2C2的电子式为 .
(4)D、F最高价氧化物的水化物之间反应的离子方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com