
【题目】将 1molCO和 2molH2充入一容积为 1L的密闭容器中,分别在250°C、T°C下发生反应:CO(g)+2H2(g) ![]() CH3OH(g)。根据图,下列分析中正确的是( )
CH3OH(g)。根据图,下列分析中正确的是( )
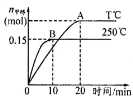
A. 250°C时,反应在前10s的平均速率υ(H2)=0.015mol/(L·min)
B. 平衡时CO的转化率:250°C>T°C
C. 反应达平衡后,其他条件不变,若减小容积体积,CO 体积分数增大
D. 该反应的正反应是放热反应
【答案】D
【解析】
依据先拐先平的判断方法可知T<250℃,升高温度,甲醇物质的量减少,平衡逆移,所以正反应为放热反应,△H<0;
A.0~10min内甲醇物质的量增加了0.15mol,根据方程式求出氢气的变化量,再求速率;
B.根据分析该反应△H<0,而且T<250℃,温度越低CO的转化率越大;
C.其他条件不变,若减小容积体积,压强增大,平衡正移;
D.T<250℃,升高温度,甲醇物质的量减少,平衡逆移,所以正反应为放热反应,△H<0。
依据先拐先平的判断方法可知T<250℃,升高温度,甲醇物质的量减少,平衡逆移,所以正反应为放热反应,△H<0;
A.0~10min内甲醇物质的量增加了0.15mol,根据方程式氢气的变化量为:0.15mol×2=0.3mol,所以υ(H2)= =0.03mol/(Lmin),选项A错误;
=0.03mol/(Lmin),选项A错误;
B.根据分析该反应△H<0,而且T<250℃,温度越低CO的转化率越大,所以CO的转化率:T℃时大于250℃时,选项B错误;
C.其他条件不变,若减小容积体积,压强增大,平衡正移,CO的物质的量减少,CO物质的量分数减小,所以CO体积分数减小,选项C错误;
D.先拐先平的判断方法可知T<250℃,升高温度,甲醇物质的量减少,平衡逆移,所以正反应为放热反应,△H<0,选项D正确;
答案选D。


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
【题目】钛是一种重要的金属,以钛铁矿[主要成分为钛酸亚铁(FeTiO3),还含有少量Fe2O3]为原料制备钛的工艺流程如图所示。
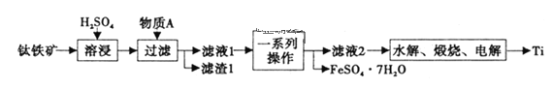
(1)滤液1中钛元素以TiO2+形式存在,则“溶浸”过程发生的主要反应的化学方程式为___。
(2)物质A为___(填化学式),“一系列操作”为___。
(3)“水解”步骤中生成TiO2·xH2O,为提高TiO2·xH2O的产率,可采取的措施有___、___。(写出两条)。
(4)将少量FeSO4·7H2O溶于水,加入一定量的NaHCO3溶液,可制得FeCO3,写出反应的离子方程式___;若反应后的溶液中c(Fe2+)=2×10-6mol·L-1,则溶液中c(CO32-)=___mol·L-1。(已知:KSP(FeCO3)=2.025×10-11)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500 mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子的浓度为( )。
A.0.1(b-2a) mol·L-1B.10(2a-b) mol·L-1
C.10(b-a) mol·L-1D.10(b-2a) mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,还含有少量Fe2O3 杂质。利用明矾石制备氢氧化铝的流程如下:
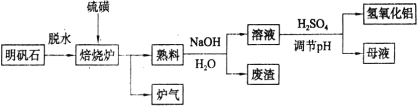
(1)焙烧炉中发生反应的化学方程式为2Al2(SO4)3+3S=2Al2O3+9SO2,若生成1molAl2O3,则转移的电子数为______。
(2)将标况下1.12L炉气通入100mL0.5mol/LNaOH 溶液中,得到一种酸性溶液,则该溶液中各种离子浓度由大到小的排列顺序为______。
(3)熟料溶解时反应的离子方程式为_________。
(4)检验废渣中含有Fe2O3所需的试剂是______________。
(5)母液中溶质主要成分的化学式为_______,溶液调节pH后经过滤、洗涤可得Al(OH)3沉淀,证明沉淀已洗涤干净的实验操作和现象是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油是工业的血液,通过它可以得到很多重要的化工产品。

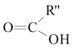
已知: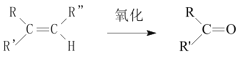 +
+
(1)B和A为同系物,B的结构简式为____,其含有的官能团名称为____。
(2)反应①的化学方程式为___,其反应类型为____。
(3)写出检验C3H5Cl中含有的Cl原子的方法____。
(4)C的结构简式为___。
(5)反应④的化学方程式为_____。
(6)设计一条由乙烯为原料制备D的合成路线(其他无机原料任选)。___
合成路线流程图示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]() BrH2C-CH2Br。
BrH2C-CH2Br。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对溴苯乙烯(![]() )与丙烯(CH2=CH-CH3)发生聚合反应的产物是一种高分子阻燃剂,具有低毒、热稳定好等优点。
)与丙烯(CH2=CH-CH3)发生聚合反应的产物是一种高分子阻燃剂,具有低毒、热稳定好等优点。
完成下列各小题:
(1)写出该产物的结构简式:___。
(2)实验室由乙苯制取对溴苯乙烯,需先经两步反应制中间体![]() 。写出该两步反应所需的试剂及条件____、____。
。写出该两步反应所需的试剂及条件____、____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AlCl3溶液蒸干灼烧得不到无水AlCl3,而用SOCl2与AlCl3·6H2O混合共热可得到无水AlCl3,试用相关化学原理与必要的化学方程式进行解释。已知液态化合物SOCl2遇水剧烈反应,生成SO2和HCl两种气体。_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是化合反应,又是氧化还原反应的是( )
A.2CO+O2![]() 2CO2B.CaO+H2O=Ca(OH)2
2CO2B.CaO+H2O=Ca(OH)2
C.C+H2O![]() CO+H2D.CO2+Ca(OH)2=CaCO3↓+H2O
CO+H2D.CO2+Ca(OH)2=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所示物质的制备方法合理的是
A.实验室从海帶中提取单质碘取样→灼烧→溶解→过滤→萃取→蒸馏
B.金红石(主要成分TiO2)为原料生产金属Ti:金红石、焦炭![]() TiCl4
TiCl4![]() Ti
Ti
C.从卤水中(溶质主要是MgCl2)提取Mg:卤水![]() Mg(OH)2
Mg(OH)2![]() MgCl2(aq)
MgCl2(aq) ![]() MgCl2(s)
MgCl2(s) ![]() Mg
Mg
D.由食盐制取漂粉精NaCl(ag) ![]() Cl2
Cl2![]() 漂粉精
漂粉精
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com