
����Ŀ��ij�о���ѧϰС����һ������NaHSO3��Һ�������������ۣ��м����Թ�����KIO3 ��Һ��һ��ʱ![]() �����ҺͻȻ����ɫ��Ϊ��һ���о��й����ضԷ�Ӧ���ʵ�Ӱ�죬̽�����¡�
�����ҺͻȻ����ɫ��Ϊ��һ���о��й����ضԷ�Ӧ���ʵ�Ӱ�죬̽�����¡�
��1���������� ֪NaHSO3�����KIO3��Ӧ��Ϊ�������У����䷴Ӧ������Ҫ�ɵ�һ����Ӧ��������֪��һ����Ӧ�����ӷ���ʽΪIO3��+3HSO3��===3SO42��+I��+3H+����ڶ�����Ӧ�����ӷ���ʽΪ________________��
��2��ͨ���ⶨ��Һ��������ʱ����̽����������Ը÷�Ӧ���ʵ�Ӱ�죬��¼���¡�
��� | 0.01mol/LNaHSO3��Һ/mL | 0.01mol/L KIO3 ��Һ/mL | H2O/mL | ��Ӧ�¶� /�� | ��Һ��������ʱ��t/s |
�� | 6.0 | 10.0 | 4.0 | 15 | t1 |
�� | 6.0 | 14.0 | 0 | 15 | t2 |
�� | 6.0 | a | b | 25 | t3 |
ʵ��������̽��_______________�Է�Ӧ���ʵ�Ӱ�죬����t1___________t2���>������=����<����;
ʵ��������̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죬����a=_____________��b=_____________����
��3����NaHSO3��Һ��KIO3��Һ�ں��������»�ϣ������ʼ���Ǽ�����ʼ�η�Ӧ���� ������С�����ԭ��������¼��裬������ɼ������
����һ�����ɵ�SO42���Է�Ӧ������ã�
�������___________________________������
��4���������ʵ����֤��������һ������±������ݡ�
ʵ�鲽�裨��Ҫ��д������������̣� | Ԥ��ʵ������ͽ��� |
���ձ����н�һ������NaHSO3��Һ��KIO3��Һ��ϣ������ʼ���Dzⶨ��ʼʱ�ķ�Ӧ����v(���� ���ձ������ȼ����������ߣߣߣߣ����������������ȫ��ͬ�������ʼ���Dzⶨ��ʼʱ�ķ�Ӧ����v(���� | ����v(�����ߣߣ�v(�����������һ������ ����v(�����ߣߣ�v(�����������һ���� ���>������=����<���� |
���𰸡���1��IO3��+5I��+6H+=3I2+3H2O��
��2��KIO3��Һ��Ũ�ȣ�> ��10.0��4.0��
��3�����ɵ�I����H+�Է�Ӧ���������
��4����Na2SO4��ĩ����=����< ��
��������
�����������1��(1��������Ϣ����Һ������˵������I2�����ӷ�Ӧ����ʽΪ��IO3��+5I��+6H��=3I2+3H2O����2��̽��Ӱ�췴Ӧ���ʵ����أ�Ҫ�������������䣬ͨ���٢ڶԱȣ�KIO3Ũ�Ȳ�ͬ�����ʵ��̽��KIO3��Һ��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬Ũ��Խ�ߣ���Ӧ����Խ�죬��t1>t2��a=10.0��b=4.0��(3�����ɵ�I����H���Է�Ӧ������ã���4�����о�SO42����������������м���Na2SO4��ĩ��������Ӧ������ȣ�����һ����ȣ���v(����<v(����������һ������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ�����ݻ�Ϊ2 L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ����ͼ�����ݷ������÷�Ӧ�Ļ�ѧ����ʽΪ____________________����Ӧ��ʼ��2 minʱ��Z��ƽ����Ӧ����Ϊ________________��
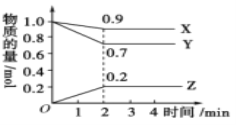
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����������������ɣ����кܴ�ĽӴ�������������ѡ��������������������ʩ�ú�������ͬ�����з��ϣ���Ч������
A��(NH4)2SO4 B��NH4HCO3 C��NH4NO3 D ��NH4Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�������ᷢչϢϢ��أ������й�˵������ȷ����
A. ������һ�գ���ˮ�����գ���ȡ֭���������������ص���ȡ�������ڻ�ѧ�仯
B. �����������Ѽ�·�������������γɵ����ܽ��ж����ЧӦ
C. ����������������֮�Ϊͭ�����ù��̷������û���Ӧ
D. �Ž�����¬�����Լ���Ϊ�У�����Ϊ���ɣ�������������������ָ�������ĺϽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������100mL 1.0mol/LNa2SO4 ��Һ������˵����ȷ���ǣ� ��
�� ��14.2gNa2SO4����100mLˮ��
�� ��20mL 5.0mol/L Na2SO4��Һ��ˮϡ����100mL
�� ����ʱ��������ƿ�̶��ߵ���Ũ��ƫ��
�� ҡ�Ⱥ���Һ����ڿ̶���è�ټ�ˮ���̶���
A. �ڢ� B. �ڢ� C. �٢� D. ���϶�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaOH��MgCl2��AlCl3���ֹ�����ɵĻ��������������ˮ��������1.16g��ɫ������������������Һ����μ���1.00mol/L HCl��Һ������HCl��Һ����������������Ĺ�ϵ��ͼ��ʾ���Իش�

��1��д��A�㵽B�㷢����Ӧ�����ӷ���ʽ
��2��C�����������Һ�����Ϊ ��
��3��ԭ�������MgCl2�����ʵ����� ��NaOH�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬ�¶��£������Ϊ1.5 L���������������з������淴Ӧ��X2 (g��+3Y2(g�� ![]() 2XY3(g�� ��H=��92.6 kJ��mol��1��ʵ�����й��������±���
2XY3(g�� ��H=��92.6 kJ��mol��1��ʵ�����й��������±���
������� | ��ʼʱ���������ʵ���/mol | ��ƽ��ʱ��ϵ�����ı仯 | ||
X2 | Y2 | XY3 | ||
�� | 1 | 3 | 0 | ����46.3 kJ |
�� | 0.8 | 2.4 | 0.4 | Q��Q��0�� |
������������ȷ���� �� ��
A���������дﵽƽ��ʱ��Y2��ת����Ϊ50%
B��Q=27.78 kJ
C����ͬ�¶��£���ʼʱ�������г���1.0 X2 mol ��3.0 mol Y2��2 mol XY3����Ӧ�ﵽƽ��ǰv(����>v(����
D�������������з�Ӧ��ƽ�ⳣ����ȣ�K=![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��
2H2(g����O2(g��===2H2O(l�� ��H����571.6 kJ��mol��1
2CH3OH(l����3O2(g��===2CO2(g����4H2O(l����H����1452 kJ��mol��1
H��(aq����OH��(aq��===H2O(l�� ��H����57.3 kJ��mol��1
����˵����ȷ���� �� ��
A. H2(g����ȼ����Ϊ571.6 kJ��mol��1
B. ͬ������H2(g����CH3OH(l����ȫȼ�գ�H2(g���ų���������
C. ![]() H2SO4(aq����
H2SO4(aq����![]() Ba(OH��2(aq��===
Ba(OH��2(aq��===![]() BaSO4(s����H2O(l�� ��H����57.3 kJ��mol��1
BaSO4(s����H2O(l�� ��H����57.3 kJ��mol��1
D. 3H2(g����CO2(g��=CH3OH(l����H2O(l�� ��H����135.9 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ͻ��������������о��й㷺��Ӧ�á����������������Ͻ����
A����ͭ B��ˮ�� C������� D��Ӳ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com