
����Ŀ���������������ԭ��Ӧ������⣺
I����ƽ�����������ԭ����ʽ��_______
___ Na2SO3��____ KIO3��____ H2SO4 =____ Na2SO4��____ K2SO4��____ I2��____ H2O
II��KClO3��Ũ������һ���¶��·�Ӧ�����ɻ���ɫ���ױ���������ȡ���仯�ɱ���Ϊ
![]() (Ũ)
(Ũ)![]()
![]() ��
��
��1��������÷�Ӧ�е���ת�Ƶ����(��˫���ű�ʾ)_______________��
��2��Ũ�����ڷ�Ӧ����ʾ������������________(�����)��
��ֻ�л�ԭ�� �ڻ�ԭ�Ժ����� ��ֻ�������� �������Ժ�����
����״���²���4.48L Cl2����μӷ�Ӧ��KClO3������Ϊ_______g������������������ʵ���Ϊ________mol��ת�Ƶ��ӵ����ʵ���Ϊ________mol��
��3��ClO2���к�ǿ��������,��˳�������������,��������Ч��(�Ե�λ�����õ��ĵ�������ʾ)��Cl2��________��������ʾ��ClO2��Cl2����ʱ��Ԫ�ض�����ԭΪ��ͼ���
���𰸡� 5 2 1 5 1 1 1  �� 49 0.4 0.4 2.63
�� 49 0.4 0.4 2.63
��������I��IԪ�صĻ��ϼ���+5����Ϊ0��SԪ�صĻ��ϼ�Ӧ��+4������Ϊ+6���ɵ��ӡ���ɡ�ԭ���غ��֪�����ӷ�ӦΪ5Na2SO3��2 KIO3��1 H2SO4 =5 Na2SO4��1K2SO4��1 I2��1H2O��II����1��KClO3����Ԫ����+5��Ϊ+4�ۣ� HCl����Ԫ����-1����0�ۣ��÷�Ӧ�е���ת�Ƶ����(��˫���ű�ʾ)��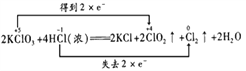 ����2��HCl����Ԫ����-1����0�ۣ����ֻ�ԭ�ԣ�Ũ�����ڷ�Ӧ�л�ԭ�ṩ���ԡ���ѡ�ڣ�����״���²���4.48L Cl2��
����2��HCl����Ԫ����-1����0�ۣ����ֻ�ԭ�ԣ�Ũ�����ڷ�Ӧ�л�ԭ�ṩ���ԡ���ѡ�ڣ�����״���²���4.48L Cl2�� ![]() =0.2mol����2KClO3��4HCl=2KCl��2ClO2��Cl2��2H2O��֪���μӷ�Ӧ��KClO3������Ϊm(KClO3)=122.5g��mol��1��0.2mol��2=49g������������������ʵ���Ϊ��n(HCl)=2n(Cl2)=0.2mol��2=0.4mol������1molCl2ת�Ƶ��ӵ����ʵ���Ϊ2mol,������0.2molCl2ת�Ƶ��ӵ����ʵ���Ϊ0.2mol��2=0.4mol����3������������71g�������õ��ĵ�����Ϊ
=0.2mol����2KClO3��4HCl=2KCl��2ClO2��Cl2��2H2O��֪���μӷ�Ӧ��KClO3������Ϊm(KClO3)=122.5g��mol��1��0.2mol��2=49g������������������ʵ���Ϊ��n(HCl)=2n(Cl2)=0.2mol��2=0.4mol������1molCl2ת�Ƶ��ӵ����ʵ���Ϊ2mol,������0.2molCl2ת�Ƶ��ӵ����ʵ���Ϊ0.2mol��2=0.4mol����3������������71g�������õ��ĵ�����Ϊ![]() ��2��1=2mol��ClO2�õ��ĵ�����Ϊ
��2��1=2mol��ClO2�õ��ĵ�����Ϊ![]() ��1��5=
��1��5=![]() mol=
mol=![]() mol����ClO2������Ч����Cl2�ı���Ϊ
mol����ClO2������Ч����Cl2�ı���Ϊ![]() =
=![]() =2.63��
=2.63��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ԭ��غ͵��ص�������ȷ����
A.ԭ�����ʧȥ���ӵĵ缫��Ϊ����
B.���ص�������ԭ��صĸ���������������Ӧ
C.ԭ��ص�����һ��Ҫ�ɻ�Բ�ͬ�����ֽ������
D.���ʱ�����ص�����һ���������ӷŵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��������п��ܺ���Cl2��O2��SO2��NO��NO2 �е����ֻ�������塣�ֽ�����ɫ�������ͨ��Ʒ����Һ��,Ʒ����Һ��ɫ����ʣ��������������У�����ܿ��Ϊ����ɫ�����ж�ԭ�������ɷֵ��ж�����ȷ���� (����)
A. �϶�ֻ��SO2 ��NO
B. �϶���Cl2��O2��NO2
C. ������Cl2��O2
D. �϶�û��NO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��xA��g��+yB��g��![]() zC��g������H=a����xmolA��ymolB������ܱ������У��ڲ�ͬ�¶ȣ�T1>T2����ѹǿ��P1>P2���£�C�����ʵ���n��C���뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ�������ж���ȷ����
zC��g������H=a����xmolA��ymolB������ܱ������У��ڲ�ͬ�¶ȣ�T1>T2����ѹǿ��P1>P2���£�C�����ʵ���n��C���뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ�������ж���ȷ����

A. x+y=z��a>0 B. x+y>z��a<0
C. x+y<z��a<0 D. x+y<z��a>0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�������׳��뻯ѧʽ����Ӧ����
A. �̷�-FeSO4��7H2OB. â��-Na2SO4��10H2O
C. ����- Al2(SO4)3��12H2OD. ����- CuSO4��5H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����¸�����Һ��Cl-�����ʵ���Ũ����300 mL 1 mol/L NaCl��Һ��Cl-�����ʵ���Ũ����ͬ����
A. 100 mL 1 mol/L AlCl3��Һ B. 200 mL 1 mol/L MgCl2��Һ
C. 100 mL 0.5 mol/L CaCl2��Һ D. 100 mL 2 mol/L KCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������;��������������ʵ���� ( )
A. �����ƿ�����ľ�ķ���Ϳ��
B. Fe2O3��������ǽͿ��
C. �������ƿ�����DZͧ������
D. ����������������ϡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ���;������� ( )
A. ˮ������觶����Ƴɸ�����Ʒ������Ҫ�ɷ־�Ϊ�赥��
B. ��ClO2������ˮ����ɱ������
C. С�մ������θ�����
D. �����¿�����������װ��Ũ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���շ���͡��һ�ֵ���Ѫ֬��ҩ���ṹ��ͼ�����й�ϵ�շ���͡��������������ȷ����
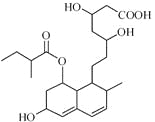
A. ����FeCl3��Һ������ɫ��Ӧ
B. ��ʹ����KMnO4��Һ��ɫ
C. �ܷ����ӳɡ�ȡ������ȥ��Ӧ
D. 1mol����������Һ��������2molNaOH��Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com