
【题目】已知25 ℃时,Ka(HF)=3.6×10-4,Ksp(CaF2)=1.46×10-10,现向1 L 0.2 mol·L-1HF溶液中加入1 L 0.2 mol·L-1 CaCl2溶液,则下列说法中,正确的是
A. 25 ℃时,0.1 mol·L-1 HF溶液中pH=1
B. Ksp(CaF2)随温度和浓度的变化而变化
C. 该体系中没有沉淀产生
D. 该体系中HF与CaCl2反应产生沉淀
科目:高中化学 来源: 题型:
【题目】现有反应的化学方程式为:aFeCl2+bKNO3+cHCl=dFeCl3+eKCl+fX+gH2O,若b=1,d=3,X为生成物,其分子式应为
A. NH4Cl B. NO C. N2 D. NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 W、X、Y 和 Z 的原子序数依次增大。金属元素 W 是制备一种高效电池的重要材料,X 原子的最外层电子数是内层电子数的 2 倍,元素 Y 是地壳中含量最丰富的金属元素,Z 原子的最外层电子 数是其电子层数的 2 倍。
(1)W 元素的原子核外共有_____种不同运动状态的电子、_____种不同能量的电子。
(2)元素 Z 与元素 X 形成共价化合物 XZ2是____(选填“极性”或“非极性”)分子,其电子式为_____。
(3)Y 原子的最外层电子排布式为_____
(4)两种非金属元素中,非金属性较强的元素是_____(写元素符号),试写出一个能说明这一事实的 化学方程式______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室采用HCl气体“置换”除水,升华相结合的方法从市售的氯化锌制备高纯度无水氯化锌,装置如图所示[市售氯化锌含Zn(OH)Cl]。下列说法不正确的是

A. 恒压漏斗的作用是平衡气体压强
B. 管式炉Ⅰ采取的升温方式是阶段式升温
C. 实验时,应先撒去管式炉Ⅰ,再撤去管式炉Ⅱ
D. 在尾气吸收装置前应增加一个干燥装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于相同质量的SO2和SO3,下列说法中正确的是( )
A.硫元素的质量比为4∶5B.分子数之比为1∶1
C.原子总数之比为15∶16D.氧元素的质量之比为5∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O。
(1)为了加快正反应速率,可以采取的措施有________(填序号,下同)。
A.使用催化剂 B.适当提高氧气的浓度
C.适当提高反应的温度 D.适当降低反应的温度
(2)下图能正确表示该反应中能量变化的是________。
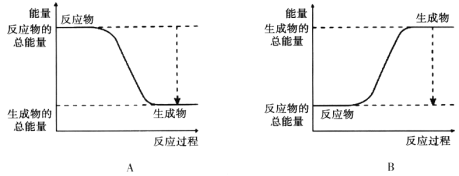
(3)从断键和成键的角度分析上述反应中能量的变化。
化学键 | H—H | O=O | H—O |
键能kJ/mol | 436 | 496 | 463 |
请填写下表:
化学键 | 填“吸收热量”或“放出热量” | 能量变化(kJ) | |
拆开化学键 | 2molH2化学键 | ________ | ________ |
1molO2化学键 | |||
形成化学键 | 4molH-O键 | ________ | ________ |
总能量变化 | ________ | ________ | |
(4)氢氧燃料电池的总反应方程式为2H2 +O2=2H2O。其中,氢气在______极发生_______反应。电路中每转移0.2mol电子,标准状况下消耗H2的体积是______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电-Fenton法是用于水体中有机污染物降解的高级氧化技术,其反应原理如图所示。其中电解产生的H2O2与Fe2+发生Fenton反应生成的羟基自由基(·OH) 能氧化降解有机污染物。下列说法正确的是

A. 电源的X极为正极
B. 与电源Y相连电极的电极反应式为H2O+e-=H++·OH
C. Fenton反应: H2O2+Fe2+=Fe(OH)2++·OH
D. 每消耗22.4L O2 (标准状况),整个电解池中理论上可产生2mol·OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将钠投入到滴有无色酚酞溶液的水中,下列有关叙述中错误的是( )
A.Na浮在水面上
B.有气体产生
C.水溶液变为蓝色
D.Na熔化成小球并在水面上四处游动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4气态分子。N4分子结构如图所示,已知断裂1molN-N吸收l67KJ的热量,生成lmol N![]() N放出942KJ热量。
N放出942KJ热量。
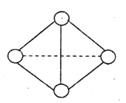
(1)试写出由N4气态分子变成N2气态分子的热化学方程式:_____________________。
(2)某盐N2H6Cl2的性质与NH4Cl类似,是离子化合物,其水溶液因分步水解而呈弱酸性。
①N2H6Cl2显酸性原因(用离子方程式表示)__________________________。
②写出足量金属镁加入盐N2H6Cl2的溶液中产生H2的化学方程式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com