
【题目】央视《每周质量报告》曾报道,某些保鲜膜样品中检出国家明令禁止使用的增塑剂,有机物E和F可用作塑料增塑剂或涂料中的溶剂,它们的相对分子质量相等,可用如图所示方法合成:

(1)X反应类型是_____________,X反应的条件是_________________ 。
(2)A的结构简式____________________ 。
(3)写出反应B+C→F的化学方程式______________________。
(4)物质F有多种同分异构体,满足下列条件的共有____________种(包括F);
①与F具有相同的官能团,能发生水解反应;
②分子中含有一个苯环;
③苯环上有两个取代基,且取代基相同。
写出符合上述条件,且水解产物遇FeC13溶液显紫色的一种物质的结构简式_________________。
【答案】 取代反应 光照 ![]()
![]() 18
18 ![]()
【解析】试题分析:![]() 发生取代反应后生成
发生取代反应后生成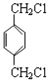 ,
, 在氢氧化钠的水溶液中发生水解反应生成A,A的结构简式为
在氢氧化钠的水溶液中发生水解反应生成A,A的结构简式为![]() ;乙醛经氧化后生成D,D为乙酸;A与D在硫酸作催化剂条件下发生酯化反应生成二乙酸对苯二甲酯;乙烯与水发生加成反应后生成C,则C为乙醇;
;乙醛经氧化后生成D,D为乙酸;A与D在硫酸作催化剂条件下发生酯化反应生成二乙酸对苯二甲酯;乙烯与水发生加成反应后生成C,则C为乙醇;![]() 经氧化后生成B,B与C也可以发生酯化反应生成与E相对分子质量相同的F,则B为对苯二甲酸、F为对苯二甲酸二乙酯。
经氧化后生成B,B与C也可以发生酯化反应生成与E相对分子质量相同的F,则B为对苯二甲酸、F为对苯二甲酸二乙酯。
(1)![]() 发生X反应后生成
发生X反应后生成 ,所以该反应是取代反应,该反应的条件是光照。
,所以该反应是取代反应,该反应的条件是光照。
(2)  在氢氧化钠的水溶液中发生水解反应生成A,A的结构简式为
在氢氧化钠的水溶液中发生水解反应生成A,A的结构简式为![]() 。
。
(3)反应B+C→F的化学方程式![]() 。
。
(4)物质F有多种同分异构体,①与F具有相同的官能团,能发生水解反应,说明分子中有2个酯基;②分子中含有一个苯环;③苯环上有两个取代基,且取代基相同。苯环上的这两个取代基有邻、间、对3种排列方式,这个取代基有-COOC2H5、-CH2COOCH3、CH3CH2COO-、CH3COOCH2-、HCOOCH2CH2-、HCOOCH(CH3)-等6种情况,所以满足这些条件的共有18种(包括F);其中水解产物遇FeC13溶液显紫色的结构简式为![]() 。
。


科目:高中化学 来源: 题型:
【题目】已知某溶液中存在较多的H+、SO42+ 、NO3-,则溶液中还可能大量存在的离子组成( )
A. Al3+、CH3COO-、Cl- B. Na+、NH4+、Cl-
C. Mg2+、Cl-、Fe2+ D. Mg2+、Ba2+、Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中各微粒的浓度关系正确的是
A. 0.2 mol·L-1的Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
B. pH相等的NaF与CH3COOK溶液:[c(Na+)-c(F-)]>[c(K+)-c(CH3COO-)]
C. pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液,NH4+大小顺序为①=②>③
D. 0.2 mol·L-1HCl与0.1 mol·L-1NaAlO2溶液等体积混合:c(Cl-)>c(Na+)>c(H+)>c(Al3+)>c(OH-)
【答案】C
【解析】根据质子守恒,0.2 mol·L-1的Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3),故A错误;根据电荷守恒,NaF溶液中[c(Na+)-c(F-)]= [c(OH-)-c(H+)],CH3COOK溶液[c(K+)-c(CH3COO-)]= [c(OH-)-c(H+)],PH相等,所以[c(Na+)-c(F-)]=[c(K+)-c(CH3COO-)],故B错误; NH4Cl、(NH4)2SO4由于NH4+水解溶液呈酸性,pH相等,所以NH4+浓度相等,NH4HSO4溶液主要由于NH4HSO4电离呈酸性,所以NH4HSO4溶液中NH4+浓度最小,故C正确;0.2 mol·L-1HCl与0.1 mol·L-1NaAlO2溶液等体积混,完全反应生成氯化钠、氯化铝、氢氧化铝,所以c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-),故D错误。
【题型】单选题
【结束】
8
【题目】直接排放含SO2的烟气会形成酸雨,危害环境。某化学兴趣小组进行如下有关SO2性质和含量测定的探究活动。

(1)装置A中仪器a的名称为________。写出A中发生反应的离子方程式_________________________。若利用装置A中产生的气体证明+4价的硫元素具有氧化性,试用化学方程式表示该实验方案的反应原理_______________________________________。
(2)选用图中的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按A→C→F→尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是__________________________________。
②丙同学设计的合理实验方案为:按照A→C→______→F→尾气处理(填字母)顺序连接装置。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是____________________________。
③其中裝置C的作用是____________________________。
(3)为了测定装置A残液中SO2的含量,量取10.00mL残液于圆底烧瓶中,加热使SO2全部蒸出,用20.00mL0.0500mol·L-1的KMnO4溶液吸收。充分反应后,再用0.2000 mol·L-1的KI标准溶液滴定过量的KMnO4,消耗KI溶液20.00mL。
已知:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+ 10I-+2MnO4-+16H+=2Mn2++5I2+8H2O
①残液中SO2的含量为____g·L-1。
②若滴定前读数时平视,滴定终点读数时俯视则测定结果________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于胶体和溶液的本质区别,下列叙述中正确的( )
A. 溶液呈电中性,胶体带电荷
B. 溶液中通过一束光线出现明显光路,胶体中通过一束光线没有特殊现象
C. 溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸
D. 溶液与胶体的本质区别在于分散质微粒直径大小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一固定容积的容器中进行反应:SO3(g)+NO(g)![]() NO2 (g)+SO2(g),下列情况一定能说明已经达到化学反应限度的是
NO2 (g)+SO2(g),下列情况一定能说明已经达到化学反应限度的是
A.体系总压强不再随时间而改变 B.体系总质量不再随时间而改变
C.NO(g)和 NO2(g)的生成速率相同 D.SO3 (g)和 NO(g)的浓度比为 1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。

下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)海洋资源的利用具有广阔前景。
(1)下图是从海水中提取镁的简单流程:

①从悬浊液中将Mg(OH)2分离出来的操作名称为_____________。
②Mg(OH)2转化为MgCl2的离子方程式是_____________。
③由无水MgCl2制取Mg的化学方程式是_____________。
(2)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧所用仪器是下列中的哪一种_____________(填字母序号)。
a. 蒸发皿 b. 坩埚 c. 烧杯
②向酸化的滤液中加入过氧化氢溶液,可将I-氧化为I2,请写出该反应的离子方程式:__________________________。
③上述反应结束后,可加入萃取剂,采用萃取一分液的方法从碘水中提取碘。下列试剂中可以用于萃取碘单质的是_____________(填字母序号)。
a. 乙酸 b. 四氯化碳 c. 硝酸 d. 苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是

A. 加入Na2SO4可使溶液由a点变到b点
B. 通过蒸发可以使溶液由d点变到c点
C. d点无BaSO4沉淀生成
D. a点对应的Ksp大于c点对应的Ksp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属氧化物的说法不正确的是( )
A.Fe3O4是具有磁性的黑色晶体
B.Al2O3能溶于酸和强碱,是两性氧化物
C.Na2O是碱性氧化物,可与H2O、CO2反应
D.FeO不稳定,在空气中受热迅速被氧化为Fe2O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com