
����Ŀ����֪��A(g) �� 2B(g) ![]() 2C(g) ��H= Q kJ��mol-1��Q��0�����ں��ݵ��ܱ������г���1 mol A��2 mol B��һ�������·�����Ӧ�������й�˵����ȷ���ǣ� ��
2C(g) ��H= Q kJ��mol-1��Q��0�����ں��ݵ��ܱ������г���1 mol A��2 mol B��һ�������·�����Ӧ�������й�˵����ȷ���ǣ� ��
A. ƽ��ǰ�����ŷ�Ӧ���У������������ܶ���С
B. ƽ��ʱ���÷�Ӧ�ų�������ΪQ kJ
C. ƽ�������������ͨ��1 mol������A��ת��������
D. ƽ�����С�����ݻ��ﵽ��ƽ�⣬A��Ũ������
���𰸡�D
�����������������A����Ϊ�÷�Ӧ�ں��ݵ��ܱ������н��У���������������Ϊ��ֵ������ƽ��ǰ�����ŷ�Ӧ�Ľ��У������������ܶȲ��䣬��A����B���÷�ӦΪ���淴Ӧ������ƽ��ʱ���÷�Ӧ�ų�������С��QkJ����B����C����Ϊ�÷�Ӧ�ں��ݵ��ܱ������н��У�ƽ�������������ͨ��1mol������ԭ��ϵ�еĸ����ʵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ�������A��ת���ʲ��䣬��C����D��ƽ�����С��������������ʵ�Ũ�ȶ�����D��ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��W��X��Y��Z��Q��ԭ��������������c��d��e��f��h������ЩԪ����ɵĶ�Ԫ�������Ȼ����Ӳ�����ĵ��ʺ�a����X��ɣ�b��W��Y��Q����Ԫ�����0.05mol/Lb��Һ��pHΪ1��d��ʹƷ����Һ��ɫ��e��Һ�壬f����ɫ��ӦΪ��ɫ���������ʵ�ת����ϵ��ͼ��ʾ(���������ȥ)������˵��������ǣ� ��
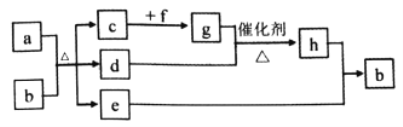
A. ��Ԫ������е㣺e>d>c B. �⻯����ȶ��ԣ�Q>Y>X
C. Ԫ�صķǽ����ԣ�Y>X>W D. ԭ�Ӱ뾶�Ĵ�С��Z>Q>Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������֤�����������̼������Ӧ����ȷ��������װ����ͼ��ʾ(��֪��PdC12��Һ��CO�ܲ�����ɫ��Pd)������˵���������

A. װ�âٵ�������������ȡH2��NH3������
B. װ�â���ʯ��ˮ����Ǻ��ٵ�ȼ�ƾ���
C. װ�âڢ��зֱ�ʢװ����Na2CO3��Һ��ŨH2SO4
D. װ�â����к�ɫ�����������ķ�Ӧ��PdC12+CO+H2O=Pd��+CO2+2HC1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ũ������H3AsO3��SnCl2��Ӧ��SnCl2+H3AsO3+HCl��Ũ����As+SnCl4+M������ȷ�������( )
��H3AsO3����ԭ���ڻ�ԭ�ԣ�Cl->As����MΪ����ʣ���SnCl4�����������ÿ����7.5gAs����ԭ��ʧȥ�ĵ���Ϊ0.3mol
A. �٢ۢܢ� B. �٢ܢ� C. �٢ڢۢ� D. �٢ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼����(MnCO3)�Ǹ����ܴ��Բ��ϣ�����������Ҫ��ս�����ʡ��ɺ��ٿ�(��Ҫ�ɷ�ΪFeWO4��MnWO4������SiO2)��ȡ̼���̺ͽ����ٵ��������£�

��֪��������(H2WO4)���Ժ�����������ˮ��������������ˮ����SiO32-��WO42-��ȫ������pH�ֱ�Ϊ8��5���۲���(H2C2O4)�������Ժͻ�ԭ�ԣ��ֽܷ⡣
�ش��������⣺
(1)����ʯ�����Ŀ����_____________________��
(2)����(X)�Ļ�ѧʽ��____________________________��
(3)д�����±��չ����У�MnWO4������Ӧ�Ļ�ѧ����ʽ________________��
(4)MnO2�����ᡢ���ᷴӦ�����ӷ���ʽ��__________________________�����һ����MnO2��ȫ�ܽ��ʱ�����¶ȵĹ�ϵ��ͼ��ʾ���������¼���75��ʱMnO2�ܽ�����ʱ�����ٵ�ԭ��__________________��

(5)��Һ�����pHӦѡ����Լ�Ϊ_________________��
A��WO3 B����ˮ C��ϡ���� D��NaHCO3
(6)��Na2CO3��Һ����Mn2+ʱ��Ӧ����MnSO4��Һ��pH������8����ֹ����Mn(OH)2����Na2CO3��Һ���̲�ȡ�IJ���������________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��NaHCO3��KHCO3��ɵĹ����������ʵ�飬���ʵ�����ݣ���������ʵ���Ũ����ȣ������ʾ������˵������ȷ���� ( )
����/mL | 50 | 50 | 50 |
������������/g | 9.2 | 15.7 | 27.6 |
��״����CO2���/L | 2.24 | 3.36 | 3.36 |
A. ��������ʵ���Ũ��Ϊ3.0 mol��L-1 B. ���ݱ��������ܼ�����������NaHCO3����������
C. ����9.2g��������ʱ������� D. 15.7g��������ǡ����������ȫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����373 Kʱ����0.5 mol N2O4ͨ�����Ϊ5 L�ĺ�������ܱ������У��������ֺ���ɫ���塣��Ӧ���е�2 sʱ��NO2��Ũ��Ϊ0.02 mol��L-1����60 sʱ����ϵ�ﵽƽ��״̬����ʱ�����ڵ�ѹǿΪ��ʼʱ��1.6��������˵��������ǣ� ��
A. ǰ2 s��N2O4��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ0.005 mol��L-1��s-1
B. ��2 sʱ��ϵ�ڵ�ѹǿΪ��ʼʱ��1.1��
C. ƽ��ʱ��ϵ�ں�N2O4 0.2 mol
D. ƽ��ʱ��N2O4��ת����Ϊ40%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������м��㣺
��1��ij���������õ�Ӫ��Һ��Ҫ��KCl��K2SO4��NH4Cl���ֹ���ԭ�ϵ����ʵ���֮��Ϊ1��4��8�������Ƹ�Ӫ��Һ��ȡ428gNH4Cl������KCl������Ϊ________g��
��2����K2SO4��Al2(SO4)3�Ļ����Һ�У����Al3+��Ũ��Ϊ0.2molL��1����������0.6molL��1��BaCl2��Һǡ��ʹSO42-��ȫ������������Һ��K+��Ũ��Ϊ_____molL��1��
��3��ij��̬������X���ȷֽ�ķ�ӦΪ��X=A��+B��+C������һ�����¶Ⱥ�ѹǿ�²�÷�Ӧ���ɵĻ�����������������ܶ�Ϊ15����X��Ħ��������___________��
��4����״���£���V L A���壨Ħ������ΪM molL��1������0.1Lˮ���ܶ�1g/cm3���У�������Һ���ܶ�Ϊdg/mL�������Һ�����ʵ���Ũ��Ϊ____________molL��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������谷���类���ϣ��1834��ϳɣ����ж�����������ʳƷ�ӹ���ʳƷ���Ӽ��������ϣ��������֪�������谷�����У���Ԫ�صĺ����ߴ�66.67%����Ԫ�ص���������Ϊ4.76%������Ϊ̼Ԫ�ء�������Է�����������100����С��150���Իش��������⣺
��1������ʽ��ԭ�Ӹ�����N(C)��N (H)��N(N)=________________________��
��2�����˴Ź���������ʾֻ��1�����շ壬������ױ�����1����̼������Ԫ����ɵ���Ԫ�ӻ����������谷�Ľṹ��ʽΪ________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com