
����Ŀ����100��ʱ����0.5molN2O4ͨ�����Ϊ5L������ܱ������У��������ֺ���ɫ����Ӧ���е�2sʱ��NO2��Ũ��Ϊ0.02mol��L-1����60sʱ����ϵ�Ѵ�ƽ�⣬��ʱ������ѹǿΪ��ʼʱ��1.6 ��������˵����ȷ����( )
A.ǰ2s��N2O4��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ0.01mol��L-1��s-1
B.��2sʱ��ϵ�ڵ�ѹǿΪ��ʼʱ��1.2��
C.��ƽ��ʱ��ϵ��N2O4�����ʵ���Ϊ0.2mol
D.ƽ��ʱ��N2O4��ת����Ϊ40%
���𰸡�C
��������
2��ʱ��NO2��Ũ��Ϊ0.02mol/L����ת����N2O4��Ũ��Ϊ0.01mol/L����Ӧ���е�60sʱ����ϵ�Ѵ�ƽ�⣬��ʱ������ѹǿΪ��ʼʱ��1.6����������N2O4�����ʵ���Ϊx����
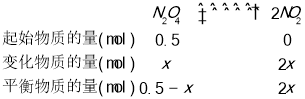
0.5-x+2x=0.5��1.6��x=0.3mol��
A��2��ʱ��NO2��Ũ��Ϊ0.02mol/L����ת����N2O4��Ũ��Ϊ0.01mol/L����ǰ2�룬��N2O4��ʾ��ƽ����Ӧ����Ϊ![]() =0.005mol/(Ls)����A����
=0.005mol/(Ls)����A����
B��

ѹǿ��ϵ��2sʱ��ϵ�ڵ�ѹǿ����ʼѹǿ=0.55��0.5=1.1��1����2sʱ��ϵ�ڵ�ѹǿΪ��ʼʱ��1.1������B����
C����ƽ��ʱ����ϵ�ں�N2O4=0.5mol-0.3mol=0.2mol����C��ȷ��
D��ƽ��ʱ��N2O4��ת����=![]() ��100%=60%����D����
��100%=60%����D����
�ʴ�ΪC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������н������·�Ӧ�� X2(g)+Y 2(g) ![]() 2Z(g) ����֪ X 2��Y2��Z ����ʼŨ�ȷֱ�Ϊ0.1mol/L ��0.3mol/L ��0.2mol/L ����һ�������£�����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п����� ( )
2Z(g) ����֪ X 2��Y2��Z ����ʼŨ�ȷֱ�Ϊ0.1mol/L ��0.3mol/L ��0.2mol/L ����һ�������£�����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п����� ( )
A.Z Ϊ 0.3mol/LB.Y2 Ϊ 0.4mol/LC.X2 Ϊ 0.2mol/LD.Z Ϊ 0.4mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��̼��������Ԫ�ص���������24��5��G����Ũ������ζ������֮���ת����ϵ���£�������ͬ�����ŵ��л���ͨ���������ƵĻ�ѧ���ʣ���
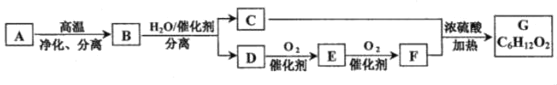
��ش�
��1��������B�����Ĺ����ŵ�������___��
��2��D�Ľṹ��ʽ��___��
��3��C+F��G�Ļ�ѧ����ʽ��___��
��4������˵����ȷ����___��
A���ڹ�ҵ�ϣ�A��B�Ĺ��̿��Ի�����͵�������
B���л���C��D����������Ʒ�Ӧ��C������Ҳ�ɵõ�F
C��������̼������Һ����E��F��G
D����������E��G���������Ժα�����ϣ���ȫȼ�պ�������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ȼ�ϵ��ԭ���о������°��ĺϳɣ���ع���ʱMV2+/MV+�ڵ缫��ø֮�䴫�ݵ��ӣ�ʾ��ͼ������ʾ������˵���������

A. ������й�ҵ�ϳɰ����÷��������ºͣ�ͬʱ�����ṩ����
B. �����������⻯ø�����·�����ӦH2+2MV2+![]() 2H++2MV+
2H++2MV+
C. ���������̵�øΪ������N2������ԭ��Ӧ����NH3
D. ��ع���ʱ����ͨ������Ĥ�ɸ��������������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ۺͻ���̿�Ļ������NaCl��Һʪ���������ͼ��ʾװ���У��������ĵ绯ѧ��ʴʵ�顣�����йظ�ʵ���˵����ȷ����

A. ���������ĵ缫��ӦʽΪFe3e![]() Fe3+
Fe3+
B. ����ʴ�����л�ѧ��ȫ��ת��Ϊ����
C. ����̿�Ĵ��ڻ�������ĸ�ʴ
D. ��ˮ����NaCl��Һ�������ܷ���������ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��װ�ã�C��D��E��F��X��Y���Ƕ��Ե缫������Դ��ͨ����(��)�е����̪��Һ����F�������Ժ�ɫ��������˵����ȷ����(����)

A.��ԴB��������
B.(��)(��)װ�õ�C��D��E��F�缫���е������ɣ������ʵ���֮��Ϊ1��2��2��1
C.����(��)װ�ø�ͭ������HӦ����Ag�����Һ��AgNO3��Һ
D.װ��(��)��Y���������ɫ���˵���������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������װ��˵����ȷ����

A. װ�����У������е�Cl������ZnSO4��Һ
B. װ��������һ��ʱ���b��������Һ��pH����
C. ��װ��������ͭʱ��c��Ϊ��ͭ
D. װ�����е�����Zn����Fe��װ������Fe2������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�з�Ӧ�����Ʊ�SiH4��һ�ַ������丱����MgCl2��6NH3�����ʵ�þ��Դ���ش��������⣺

��1��MgCl2��6NH3����Ԫ�صļ����Ӱ뾶��С�����˳��H-���⣩��_________________________��Mg��Ԫ�����ڱ��е�λ�ã�_____________________��Mg(OH)2�ĵ���ʽ��____________________��
��2��A2B�Ļ�ѧʽΪ_______________����Ӧ�ڵıر�������_______________����ͼ�п���ѭ��ʹ�õ�������_______________��
��3����һ�������£���SiH4��CH4��Ӧ����H2��һ�ֹ�����ĥ����_______________��д��ѧʽ����
��4��Ϊʵ��ȼú������ú�м��뽬״Mg(OH)2��ʹȼ�ղ�����SO2ת��Ϊ�ȶ���Mg�����д���÷�Ӧ�Ļ�ѧ����ʽ��_______________��
��5����Mg�Ƴɵĸ����Լ���RMgBr���������л��ϳɣ������Ʊ��������ĺϳ�·�����£�
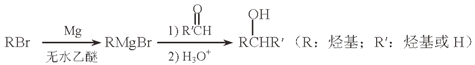
����������Ϣ��д���Ʊ�![]() ����ȩ�Ŀ��ܽṹ��ʽ��_______________��
����ȩ�Ŀ��ܽṹ��ʽ��_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����20 mL 0.1 mol��L��1 NaOH��Һ����μ���0.2 mol��L��1������Һ��������ͼ��ʾ���й�����Ũ�ȹ�ϵ�ıȽ��У���������
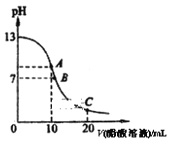
A.��A�㣺c(Na��)>c(OH��)>c(CH3COO��)>c(H��)
B.��B�㣺c(OH��)=c(H��)<c(Na��)=c(CH3COO��)
C.��C�㣺c(CH3COO��)��c(CH3COOH)=2c(Na��)
D.��A��B��C�㣺c(Na��)��c(H��)=c(OH��)��c(CH3COO��)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com