
【题目】某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如图所示的实验装置。
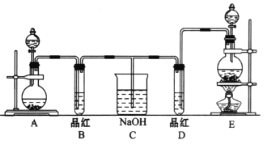
(1)实验室常选用制CO2的发生装置制SO2;实验室在用MnO2跟浓盐酸反应制备Cl2时,应选用图中A、E两发生装置中___装置(填装置序号)制Cl2。在制Cl2的反应中浓盐酸所表现出的性质是___。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B:___D:___。
(3)装置C的作用是____。
(4)甲乙两名同学分别利用如图所示装置探究两种气体按不同比例混合后的漂白性,试
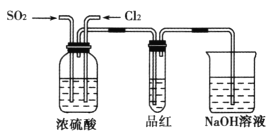
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是___。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色写出其相应的离子方程式:___。
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅。其原因是__。
【答案】E 还原性和酸性 溶液由无色变成红色 溶液没有明显变化 保证安全,吸收多余的氯气和二氧化硫 使两种气体充分混合,通过观察气泡的速度控制气体流量,使二者按一定比例混合 SO2+Cl2+2H2O=4H++SO42-+2Cl- SO2和Cl2的进气速度不相等,混合发生反应后其中一种气体有剩余,仍具有漂白性
【解析】
(1)根据反应物的状态和反应条件选择反应装置,根据氯元素的化合价判断其表现的性质;
(2)次氯酸的漂白性是利用次氯酸的强氧化性,二氧化硫的漂白性是利用二氧化硫和有色物质生成无色物质,注意次氯酸的漂白性是永久性的,二氧化硫的漂白性是暂时的;
(3)根据氢氧化钠及二氧化硫和氯气的性质分析;
(4)①浓硫酸和二氧化硫、氯气不反应,但氯气和二氧化硫在该装置中能充分混合,且通过观察气泡的速度控制气体流量,使二者按一定比列混合;
②氯气有强氧化性,二氧化硫有还原性,二者能按1:1发生氧化还原反应而使气体失去漂白性;
③如果SO2和Cl2的进气速度不相等,混合发生反应后其中一种气体有剩余,仍具有漂白性。
(1)实验室制取氯气所用药品是固体和液体,反应条件是加热,所以应选用固液加热型装置,答案选E;
实验室制取氯气的反应方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,由HCl生成MnCl2,氯元素化合价不变,由HCl生成Cl2,氯元素化合价升高,所以浓盐酸所表现出的性质是酸性和还原性;
MnCl2+Cl2↑+2H2O,由HCl生成MnCl2,氯元素化合价不变,由HCl生成Cl2,氯元素化合价升高,所以浓盐酸所表现出的性质是酸性和还原性;
(2)次氯酸的漂白性是利用次氯酸的强氧化性,二氧化硫的漂白性是利用二氧化硫和有色物质生成无色物质,次氯酸的漂白性是永久性的,二氧化硫的漂白性是暂时的;
加热时,次氯酸漂白过的溶液无变化,二氧化硫和有色物质生成的无色物质不稳定,加热时能重新变成红色;
(3)氯气和二氧化硫有毒,不能排放到空气中,但氯气和二氧化硫都和碱反应,所以装置C的作用是保证安全,吸收多余的氯气和二氧化硫;
(4)①浓硫酸和二氧化硫、氯气不反应,但氯气和二氧化硫在该装置中能充分混合,且通过观察气泡的速度控制气体流量,使二者按一定比列混合;
②氯气有强氧化性,二氧化硫有还原性,二者能按1:1发生氧化还原反应而使气体失去漂白性,离子反应方程式为SO2+Cl2+2H2O=4H++SO42-+2Cl-;
③通气一段时间后,品红溶液颜色随时间推移变得越来越浅,说明有漂白性;如果SO2和Cl2的进气速度不相等,混合发生反应后其中一种气体有剩余,仍具有漂白性。


科目:高中化学 来源: 题型:
【题目】某课外活动小组拟用下列装置做炼铁原理的实验,同时检测氧化铁的纯度(假设矿石中不含其他与CO反应的成分),并除去尾气。CO气体用H2C2O4![]() CO2↑+CO↑+H2O来制取,与Fe2O3反应的CO需纯净、干燥。
CO2↑+CO↑+H2O来制取,与Fe2O3反应的CO需纯净、干燥。
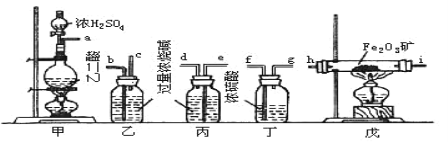
(1)若所制气体从左向右流向时,上述仪器组装连接的顺序是(用a、b…表示) 接 , 接 , 接 , 接 。___________________
(2)装置乙的作用是___________________;装置丙的目的是____________________。
(3)实验结束后,先熄灭戊处的酒精灯,再熄灭甲处的酒精灯,其主要原因是____________________。
(4)实验前氧化铁矿粉末为xg,实验后测得乙、丙质量分别增加yg和zg,则氧化铁的质量分数为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新版人民币的发行,引发了人们对有关人民币中化学知识的关注。下列表述不正确的是( )
A. 制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B. 用于人民币票面文字等处的油墨中所含有的![]() 是一种磁性物质
是一种磁性物质
C. 某种化学验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是淀粉
D. 防伪荧光油墨由颜料与树脂连接料等制成,树脂与油脂一样,属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl晶体呈白色,见光易分解,在潮湿空气中易被氧化,难溶于水、稀盐酸和乙醇。实验室用如图所示装置制取CuCl。以下说法正确的是( )

A.装置A中发生的反应是氧化还原反应
B.装置B中的搅拌子是由铁直接铸造
C.装置B中反生反应的离子方程式是SO2+2Cu2++2Cl-+2H2O=2CuCl↓+4H++SO42-
D.装置C中用干燥管替代导管的主要目的是使剩余的SO2能被充分吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯为基本原料可制备X、Y、Z、W等物质,下列有关说法中正确的是( )
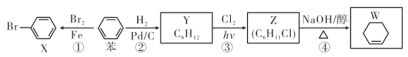
A. 反应①是苯与溴水的取代反应 B. 可用AgN03溶液检测W中是否混有Z
C. X、苯、Y分子中六个碳原子均共平面 D. 反应④中产物除W外还有H2O和NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图A~J分别代表相关反应中的一种物质,已知A分解得到等物质的量的B、C、D,常温下B、D为气态化合物,C为液态化合物,图中有部分生成物未标出。已知﹕2Mg+CO2![]() 2MgO+C。
2MgO+C。
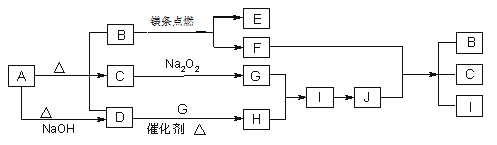
请回答下列问题:
(1)写出A的化学式:___。
(2)写出下列反应的化学方程式:
D+G→H___。
F+J→B+C+I___。
(3)写出A+NaOH→D的离子方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验发现,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中逐滴加入5mol/L NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列说法不正确的是( )
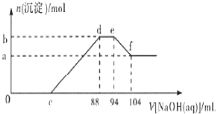
A.稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵
B.c点对应NaOH溶液的体积为48 mL
C.b点与a点的差值为0.05 mol
D.样品中铝粉和铁粉的物质的量之比为5:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.热的纯碱液去油污效果好,因为加热可使CO32-的水解程度增大,溶液碱性增强,去污力增强
B.铁在潮湿的环境下生锈以及Mg与NH4Cl溶液反应生成H2都与盐类水解有关
C.将Al2(SO4)3溶液加热、蒸干、灼烧,可得到固体Al2(SO4)3
D.将饱和FeCl3溶液滴入沸水中制胶体,离子方程式:Fe3++3H2O![]() Fe(OH)3(胶体) +3H+
Fe(OH)3(胶体) +3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.髙锰酸钾在实验室和工农业生产中有广泛的用途,实验室以二氧化锰为主要原料制备高锰酸钾,其部分流程如下:

(1)第①步加热熔融应在铁坩埚中进行,而不用瓷坩埚的原因是_______________________________(用化学方程式表示)。
(2)第④步通人适量CO2,发生反应生成MnO4-、MnO2和碳酸盐,则发生反应的离子方程式为_______________________________。
(3)第⑥步加热浓缩至液面有细小晶体析出时,停止加热,冷却结晶、过滤、洗涤、干燥,干燥过程中,温度不宜过高,其原因是_________________(用化学方程式表)。
(4)H2O2和KMnO4都是常用的强氧化剂,若向H2O2溶液中滴加酸性髙锰酸钾溶液,则酸性髙锰酸钾溶液会褪色,写出该反应的离子方程式: ________________________________。
II.某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和C12的性质。

(5)若从左端分别通入SO2和C12,装置A中观察到的现象是否相同______(填“相同”或“不相同”)。
(6)若装置B中装有5.0 mL 1.0 mol L-1的碘水,当通入足量Cl2完全反应后,共转移了5. 0×10-2 mol电子,则该反应的化学方程式为____________________________。
(7)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4 : 3;当Cl2与含有X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加人氯化钡溶液,有白色沉淀产生。 写出Cl2与含有X的溶液反应的离子方程式: __________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com