
【题目】类推法在化学学习过程中广泛使用,如下四项推测,其中正确的是( )
A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大
B.根据结构和组成相似的物质,沸点随相对分子质量增大而升高,推出NH3的沸点低于PH3
C.CO2中的C采用sp杂化轨道成键,CS2中的C也是采用sp杂化轨道成键
D.CH4的空间结构为正四面体,键角为109°28′,P4的空间结构也为正四面体,键角为109°28′
【答案】C
【解析】
A.同周期元素第一电离能的变化趋势为:从左到右逐渐增大。但镁和铝例外,因为镁的价电子排布是3s2,s轨道全满,较稳定。而铝是3s23p1,不是全满、半满、全空中任意一种情况,稳定性较差,故铝的第一电离能比镁小,A错误;
B.氨分子间存在氢键,导致沸点升高,而PH3分子间没有氢键,所以NH3的沸点高于PH3, B错误;
C.CO2中C和O形成双键,结构式为O=C=O,空间构型为直线型;CS2中S和O也形成双键,结构式为S=C=S,空间构型为直线型,所以C和S均为sp杂化,C正确;
D.CH4的空间结构为正四面体,空间构型为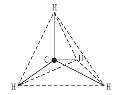 ,键角为109°28′;白磷的空间结构也为正四面体,空间构型为
,键角为109°28′;白磷的空间结构也为正四面体,空间构型为![]() ,键角为60°,D错误;
,键角为60°,D错误;
故选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图是氢氧燃料电池构造示意图。下列说法不正确的是( )
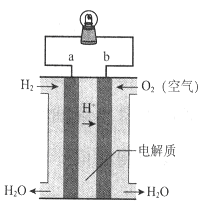
A. a极是负极
B. 电流由b通过灯泡流向a
C. 该电池总反应是2H2+ O2=2H2O
D. b极的电极反应为:O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有室温下四种溶液,①pH=11的氨水;②pH=11的NaOH溶液;③pH=3的醋酸;④pH=3的硫酸,下列有关说法不正确的是
A.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B.分别加水稀释10倍,四种溶液的pH①>②>④>③
C.①、④两溶液混合后,若溶液呈中性,则所得溶液中2c(NH4+)=c(SO42-)
D.V1L④与V2L②溶液混合后,若混合后溶液pH=4,则V1:V2=11:9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向![]() 时,体积均为20mL、浓度均为
时,体积均为20mL、浓度均为![]() 的两种酸HX、HY溶液中分別滴加
的两种酸HX、HY溶液中分別滴加![]() 的NaOH溶液,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是
的NaOH溶液,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是![]()
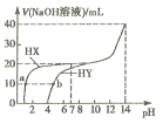
A.HX与NaOH溶液反应的离子方程式为:![]()
B.![]() 的数量级约为
的数量级约为![]()
C.b点时:![]()
D.![]() 时,两种反应后的溶液中
时,两种反应后的溶液中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】顺铂[Pt(NH3)2Cl2]是1969年发现的第一种具有抗癌活性的金属配合物;碳铂是1,1-环丁二羧酸二氨合铂(Ⅱ)的简称,属于第二代铂族抗癌药物,结构简式如图所示,其毒副作用低于顺铂。下列说法正确的是( )

A. 碳铂中所有碳原子在同一个平面中
B. 顺铂分子中氮原子的杂化方式是sp2
C. 碳铂分子中sp3杂化的碳原子与sp2杂化的碳原子之比为2∶1
D. 1 mol 1,1-环丁二羧酸含有σ键的数目为12NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)F2通入稀NaOH溶液中可生成OF2,OF2立体构型为___,其中氧原子的杂化方式为___。
(2)X、Y、Z、R为前四周期元素且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。XY2-的立体构型是___;X与Z形成化合物中含有的化学键是___、R2+的水合离子中,提供孤电子对的原子是___。
(3)ClO3-的立体构型为___(用文字描述,下同);CO32-的立体构型是__。
(4)在BF3分子中:F—B—F的键角是___,B原子的杂化轨道类型为__,BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为___。
(5)用价层电子对互斥理论推断,SnBr2分子中Sn—Br键的键角___(填“>”“<”或“=”)120°。其原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钠![]() 化合物中钠元素是
化合物中钠元素是![]() 价,NaH跟水反应放出
价,NaH跟水反应放出![]() ,下列叙述正确的是( )
,下列叙述正确的是( )
A.在NaH中的氢离子半径比锂离子半径大
B.在NaH中的氢离子的电子层排布与![]() 不相同
不相同
C.NaH跟水反应后溶液呈酸性
D.NaH中的氢离子被还原成氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学中常用图像直观的描述化学反应的进程或结果。下列图像描述正确的是:
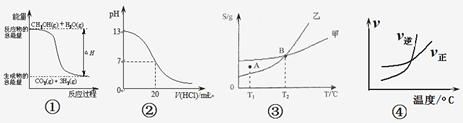
A.根据图①可判断反应CH3OH(g)+H2O(g)=CO2(g)+3H2(g)的ΔH<0
B.图②表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液的pH随加入酸体积的变化
C.根据图③(S表示溶解度),A点表示T1℃时甲为饱和溶液,乙溶液未饱和。
D.根据图④可判断可逆反应A2(g)+3B2(g)![]() 2AB3(g)的ΔH>0
2AB3(g)的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA代表阿伏加德罗常数的值。下列说法正确的是
A.1 L0.5 mol/L Na2SO3溶液中含氧原子数为1.5NA
B.1 mol Na2O2中阴阳离子总数为3NA
C.4.6 g NO2和N2O4混合气体中含氧原子数为0.3NA
D.11.2 L NH3所含的分子数为0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com