
【题目】标准状况下1mol某烃完全燃烧时,生成89.6LCO2,又知0.1mol此烃能与标准状况下4.48LH2加成,则此烃的结构简式是
A.CH3CH=CHCH3B.CH3C≡CCH3
C.CH3CH2CH=CH2D.CH2=CHCH=CHCH3
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:
【题目】用AG表示溶液的酸度,其表达式为AG=lg[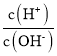 ],298K时,向10mL0.1 molL-1 HX溶液中滴加 0.1molL-1NaOH 溶液。溶液的AG与NaOH溶液体积的关系如图所示。下列说法错误的是 ( )
],298K时,向10mL0.1 molL-1 HX溶液中滴加 0.1molL-1NaOH 溶液。溶液的AG与NaOH溶液体积的关系如图所示。下列说法错误的是 ( )
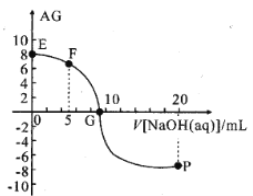
A.溶液pH和AG的关系式为AG=14-2pH
B.对G点溶液,c(Na+) = c(X-)
C.298K时HX的电离常数Ka≈1.0×10-5
D.溶液中水电离的c(OH-) F点<P点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质在食品、化妆品等行业有广泛用途。
(1)C8H8O3的某一同分异构体尼泊金酯的结构简式如图。
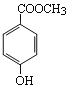
①下列对尼泊金酯的判断不正确的是______。
a.能发生水解反应
b.能与FeCl3溶液发生显色反应
c.分子中所有原子都在同一平面上
d.与浓溴水反应时,1 mol尼泊金酯消耗1 mol Br2
②尼泊金酯与NaOH溶液在一定条件下反应的化学方程式是________________________,其中包含的反应类型有________________、_______________。
(2)C8H8O3的另一种同分异构体甲满足以下条件:
①与足量的NaOH溶液完全反应时,1 mol甲消耗3 molNaOH
②遇FeCl3溶液显色③ 苯环上的一氯取代物只有一种,甲可能的结构简式是_______、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的结构简式为![]() ,它可通过不同化学反应分别制得B、C、D和E四种物质。
,它可通过不同化学反应分别制得B、C、D和E四种物质。
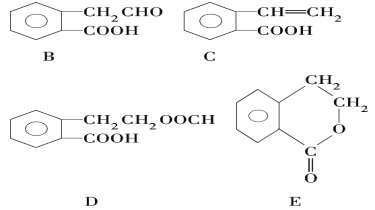
请回答下列问题:
(1)在A~E五种物质中,互为同分异构体的是____________ (填序号)。
(2)C能形成高聚物,该高聚物的结构简式为 _______________________。
(3)指出反应的类型:A→C:_________,E中含有的官能团的名称:_______
(4)写出由A生成B的化学方程式_______________________。
(5)已知HCHO分子中所有原子都在同一平面内,则在上述分子中所有的原子有可能都在同一平面的物质是__________________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用甲酸和浓硫酸反应制备CO,用于还原氧化铜,实验装置图和实验步骤如下:

①按上图连接好装置,检查装置气密性。
②点燃Ⅰ处酒精灯,缓慢滴入甲酸。
③在完成某项操作后,点燃另外两处酒精灯。
④反应结束后熄灭酒精灯,待产物冷却至室温后,收集产物。
请回答下列问题:
Ⅰ.(1)甲酸在浓硫酸条件下能分解生成CO和H2O,体现浓硫酸具有_____________。
A.氧化性 B.脱水性 C.吸水性
(2)NaOH溶液的作用是_________。实验步骤③某项操作是指___________;
(3)若干燥管中的固体颗粒堵塞干燥管的出口,则装置Ⅱ中出现的现象为:_____________;
(4)该实验能证明HCOOH受热产物中有CO的现象为:___________________;
(5)实验步骤④中酒精灯I、III和Ⅳ的熄灭顺序为_______________。
Ⅱ.学习小组查阅资料知:
①Cu的颜色为红色或紫红色,而Cu2O的颜色也为红色或砖红色。
②4CuO![]() 2Cu2O + O2↑ ③Cu2O +2H+=Cu +Cu2+ + H2O
2Cu2O + O2↑ ③Cu2O +2H+=Cu +Cu2+ + H2O
因此对CO充分还原CuO后所得红色固体是否含有Cu2O进行了认真的研究,提出下列设计方案:取该红色固体溶于足量稀硫酸中,观察溶液颜色的变化。
(6)请你评价该方案的合理性,并简述理由:
方案:_______________,理由:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是
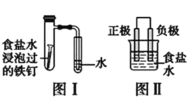
A.按图Ⅰ装置实验,加热具支试管可更快更清晰地得到实验证据—观察到液柱上升
B.图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
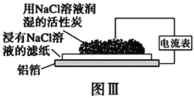
C.铝制品表面白斑可用图Ⅲ装置进行探究,Cl-在铝箔表面区发生电极反应:2Cl- -2e-=Cl2↑
D.图Ⅲ装置的总反应为4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3脱水形成白斑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将其与浓盐酸混合加热,产生了黄绿色气体。
(1)该反应的化学方程式为____________________。
(2)反应中氧化剂是_______(填化学式),锰元素的化合价________(填“升高”或“降低”)。若消耗了17.4 g MnO2,则生成标准状况下Cl2的体积是_______L,转移电子的物质的量是______mol。
(3)用此反应制得的氯气中常混有_______,要收集到干燥纯净的氯气,应使气体依次通过装有_______、_______的洗气瓶后再收集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,后者刚好是前者两倍的是
A.51 g氧化铝中氧原子数和67.2 L一氧化碳中氧原子数
B.1molCO2的摩尔质量和2 molCO2的摩尔质量
C.50 mL 2 mol·L-1氯化钠溶液中c(Cl-)和50 mL 2 mol·L-1氯化镁溶液中c(Cl-)
D.1molNa2O2固体中阳离子与阴离子比值和1molNa2O固体中阳离子与阴离子比值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某地海水中主要离子的含量如下表,现利用“电渗析法”进行淡化,技术原理如图所示(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过)。下列有关说法错误的是
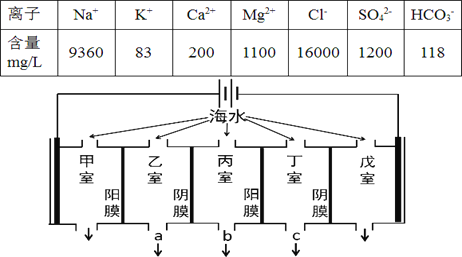
A. 甲室的电极反应式为:2Cl--2e-= Cl2↑
B. 淡化过程中易在戊室形成水垢
C. 乙室和丁室中部分离子的浓度增大,淡水的出口为 b
D. 当戊室收集到22.4L(标准状况)气体时,通过甲室阳膜的离子的物质的量一定为2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com