
【题目】下列各组数据中,后者刚好是前者两倍的是
A.51 g氧化铝中氧原子数和67.2 L一氧化碳中氧原子数
B.1molCO2的摩尔质量和2 molCO2的摩尔质量
C.50 mL 2 mol·L-1氯化钠溶液中c(Cl-)和50 mL 2 mol·L-1氯化镁溶液中c(Cl-)
D.1molNa2O2固体中阳离子与阴离子比值和1molNa2O固体中阳离子与阴离子比值
【答案】C
【解析】
A.51g氧化铝物质的量为![]() =0.5mol,含有氧原子物质的量为1.5mol,标况下67.2LCO物质的量为3mol,含有O原子物质的量为3mol,后者是前者的2倍,但题干中温度和压强未知,气体摩尔体积未知,所以无法计算一氧化碳中n(O),故A不符合题意;
=0.5mol,含有氧原子物质的量为1.5mol,标况下67.2LCO物质的量为3mol,含有O原子物质的量为3mol,后者是前者的2倍,但题干中温度和压强未知,气体摩尔体积未知,所以无法计算一氧化碳中n(O),故A不符合题意;
B.2molCO2的质量是1molCO2的质量的2倍,但CO2的摩尔质量为定值是44g/mol,故B不符合题意;
C.电解质离子浓度=电解质浓度×电解质电离出的该离子数目,与溶液的体积无关,2mol/L氯化钠溶液中c(Cl-)=2mol/L,2molL-1氯化镁溶液中c(Cl-)=4mol/L,氯离子浓度后者是前者的2倍,故C正确;
D.1mol Na2O2晶体物质的量为1mol,阳离子Na+为2mol,阴离子O22-物质的量为1mol,阳离子与阴离子比值2:1,1mol Na2O晶体物质的量为1mol,阳离子Na+为2mol,阴离子O2-物质的量为1mol,阳离子与阴离子比值2:1,故D错误;
故选:C。


科目:高中化学 来源: 题型:
【题目】用下列装置不能达到有关实验目的的是( )
A.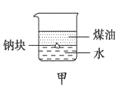 用甲图装置证明ρ(煤油)<ρ(钠)<ρ(水)
用甲图装置证明ρ(煤油)<ρ(钠)<ρ(水)
B.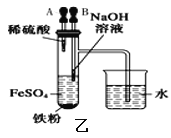 用乙图装置制备Fe(OH)2
用乙图装置制备Fe(OH)2
C.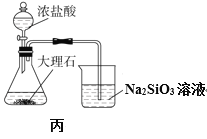 用丙图装置验证酸性:盐酸>碳酸>硅酸
用丙图装置验证酸性:盐酸>碳酸>硅酸
D.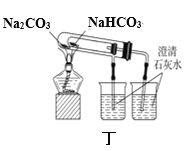 用丁图装置比较NaHCO3和Na2CO3的热稳定性
用丁图装置比较NaHCO3和Na2CO3的热稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下1mol某烃完全燃烧时,生成89.6LCO2,又知0.1mol此烃能与标准状况下4.48LH2加成,则此烃的结构简式是
A.CH3CH=CHCH3B.CH3C≡CCH3
C.CH3CH2CH=CH2D.CH2=CHCH=CHCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组欲制取氨气设计了如下图所示装置(另有橡胶管若干可选用)。
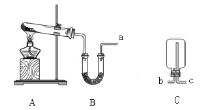
(1)A中制氨气的化学方程式是____________________________________。
(2)B中应装___________,作用是____________。
(3)收集氨气时,B装置的a口应连接C装置的___________(填“b”或“c”)口;证明氨气已集满的操作和现象是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在水溶液中1 mol ClOx-(x=0,1,2,3,4)的能量(kJ)相对大小如图所示,下列有关说法正确的是( )
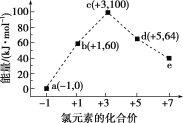
A.e是ClO3-
B.b→a+c反应的活化能为60 kJ·mol-1
C.a、b、c、d、e中c最稳定
D.b→a+d反应的热化学方程式为3ClO-(aq)=2Cl-(aq)+ClO3-(aq) ΔH=-116 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把2V L含有Na2SO4和MgSO4的混合溶液分成两等份,一份加入含溶质a mol的KOH溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含溶质b mol的BaCl2溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钠离子的浓度为
A.![]() mol·L-1B.
mol·L-1B.![]() mol·L-1C.
mol·L-1C.![]() mol·L-1D.
mol·L-1D.![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F可用于某抗凝血药的制备,工业生成F的一种路线图如下(其中H与FcCl3溶液能发生显色反应):
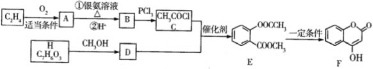
回答下列问题:
(1) A的名称是_____,E中的官能团名称是_______。
(2) B→C的反应类型是___, F的分子式为_______。
(3) H的结构简式为__.
(4) E与NaOH溶液反应的化学方程式为___。
(5)同时满足下列条件的D的同分异构体共有_____种,写出核磁共振氢谱有5组峰的物质的结构简式___。
①是芳香族化合物
②能与NaHCO3溶液反应但不能与FeCl3溶液发生显色反应
③l mol该物质与钠反应时最多可得到1molH2
(6)以2-氯丙酸、苯酚为原料制备聚丙烯酸苯酚酯(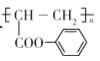 ),写出合成路线图(无机试剂自选)___。
),写出合成路线图(无机试剂自选)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)
图1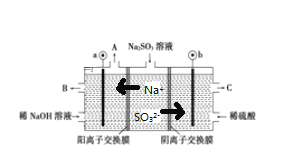 图2
图2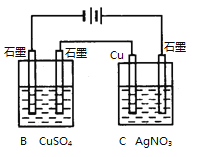
(1)图1中a极要连接电源的__________(填“正”或“负”)极,SO32-放电的电极反应__________
(2)在图2所示的装置中,若通入直流电5 min时,铜电极质量增加2.16g,试回答:
①溶液pH变化:B__________,C__________(填“增大”“减小”或“不变”)。
②通电5 min时,B中共收集224mL气体(标准状况),溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为__________(设电解前后溶液体积无变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,向20mL0.1mol/L的醋酸溶液中不断滴入0.1mol/L的NaOH溶液,溶液的pH变化曲线如图所示.下列说法中正确的是
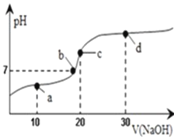
A.a点时:c(CH3COO-)c(Na+)c(H+)c(OH-)
B.用甲基橙试液作指示剂时终点颜色变化是由红色变为橙色
C.c点时:c(H+)=c(OH-)+c(CH3COOH)
D.d点时:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com