
ЎҫМвДҝЎҝіЈјыөДОеЦЦСОXЎўYЎўZЎўMЎўNЈ¬ЛьГЗөДТхАлЧУҝЙДЬКЗSO42ЈӯЎўClЈӯЎўNO3ЈӯЎўCO32ЈӯЈ¬СфАлЧУҝЙДЬКЗAg+ЎўNH4+ЎўNa+ЎўAl3+ЎўCu2+ЎўBa2+ЎўFe3+Ј¬ТСЦӘЈә
ўЩMөДСжЙ«·ҙУҰіК»ЖЙ«ЎЈ
ўЪОеЦЦСОҫщИЬУЪЛ®Ј¬Л®ИЬТәҫщОӘОЮЙ«ЎЈ
ўЫXөДИЬТәіКЦРРФЈ¬YЎўZЎўNөДИЬТәіКЛбРФЈ¬MөДИЬТәіКјоРФЎЈ
ўЬИфФЪХвОеЦЦСОөДИЬТәЦР·ЦұрјУИлBaЈЁNO3Ј©2ИЬТәЈ¬Ц»УРXЎўZөДИЬТәІ»ІъЙъіБөнЎЈ
ўЭИфФЪХвОеЦЦСОөДИЬТәЦРЈ¬·ЦұрјУИл°ұЛ®Ј¬NәНZөДИЬТәЦРЙъіЙіБөнЈ¬јМРшјУ°ұЛ®Ј¬ZЦРіБөнПыК§ЎЈ
ўЮ°СXөДИЬТә·ЦұрјУИлөҪYЎўZЎўNөДИЬТәЦРЈ¬ҫщДЬЙъіЙІ»ИЬУЪПЎПхЛбөДіБөнЎЈ
Зл»ШҙрПВБРОКМвЈә
ЈЁ1Ј©ОеЦЦСОЦРЈ¬Лщә¬ТхАлЧУПаН¬өДБҪЦЦСОөД»ҜС§КҪКЗ__________________
ЈЁ2Ј©MИЬТәПФјоРФөДФӯТтКЗЈЁУГАлЧУ·ҪіМКҪұнКҫЈ©______________________
ЈЁ3Ј©XәНZөДИЬТә·ҙУҰөДАлЧУ·ҪіМКҪКЗ_______________________
ЈЁ4Ј©NәН°ұЛ®·ҙУҰөДАлЧУ·ҪіМКҪКЗ_____________________________________
ЈЁ5Ј©ИфТӘјмСйYЦРЛщә¬өДСфАлЧУЈ¬ХэИ·өДКөСй·Ҫ·ЁКЗ______________________
Ўҫҙр°ёЎҝЈЁ1Ј©ЈЁNH4Ј©2SO4ЎўAl2ЈЁSO4Ј©3
ЈЁ2Ј©CO32-Ј«H2O ![]() HCO3ЈӯЈ«OHЈӯ
HCO3ЈӯЈ«OHЈӯ
ЈЁ3Ј©AgЈ«Ј«ClЈӯ===AgClЎэ
ЈЁ4Ј©Al3Ј«Ј«3NH3ЎӨH2O===AlЈЁOHЈ©3ЎэЈ«3NH4+
ЈЁ5Ј©ИЎЙЩБҝBУЪКФ№ЬЦРЈ¬јУИлЕЁNaOHИЬТәІўјУИИЈ¬УГКӘИуөДәмЙ«КҜИпКФЦҪ·ЕФЪКФ№ЬҝЪЈ¬№ЫІмКЗ·сұдА¶Й«
ЎҫҪвОцЎҝ
КФМв·ЦОцЈәўЩMөДСжЙ«·ҙУҰіК»ЖЙ«Ј¬ФтMИЬТәә¬УРNa+;ўЪОеЦЦСОҫщИЬУЪЛ®Ј¬Л®ИЬТәҫщОӘОЮЙ«ЛөГчІ»ә¬УРА¶Й«өДCu2+Ўў»ЖЙ«өДFe3+;ўЫXөДИЬТәіКЦРРФЈ¬YЎўZЎўNөДИЬТәіКЛбРФЈ¬MөДИЬТәіКјоРФЈ¬ФтMә¬УРИхјоТхАлЧУCO32-Ј¬ЛщТФMКЗNa2CO3ЎЈYЎўZЎўNКЗЗҝЛбИхјоСО;ўЬИфФЪХвОеЦЦСОөДИЬТәЦР·ЦұрјУИлBaЈЁNO3Ј©2ИЬТәЈ¬Ц»УРXЎўZөДИЬТәІ»ІъЙъіБөнЈ¬ЛөГчXЎўZЦРГ»УРSO42-Ј¬ўЭИфФЪХвОеЦЦСОөДИЬТәЦРЈ¬·ЦұрјУИл°ұЛ®Ј¬NәНZөДИЬТәЦРЙъіЙіБөнЈ¬јМРшјУ°ұЛ®Ј¬ZЦРіБөнПыК§Ј¬ФтZКЗAgNO3Ј¬NЦРУРAl3+ЎЈўЮ°СXөДИЬТә·ЦұрјУИлөҪYЎўZЎўNөДИЬТәЦРЈ¬ҫщДЬЙъіЙІ»ИЬУЪПЎПхЛбөДіБөнЈ¬ФтXКЗBaCl2ИЬТәЈ¬YКЗЈЁNH4Ј©2SO4Ј¬NКЗAl2ЈЁSO4Ј©3ЎЈ
ЈЁ1Ј©ОеЦЦСОЦРЈ¬Т»¶ЁІ»ә¬УРөДСфАлЧУКЗCu2+ЎўFe3+;Лщә¬ТхАлЧУПаН¬өДБҪЦЦСОөД»ҜС§КҪКЗЈЁNH4Ј©2SO4ЎўAl2ЈЁSO4Ј©3ЎЈ
ЈЁ2Ј©MөД»ҜС§КҪОӘNa2CO3Ј¬MИЬТәПФјоРФөДФӯТтКЗCO32-·ўЙъЛ®Ҫв·ҙУҰЈ¬ПыәДЛ®өзАлІъЙъөДH+Ј¬ҙЩҪшБЛЛ®өДөзАлЈ¬өұҙпөҪЖҪәвКұЈ¬cЈЁOH-Ј©>cЈЁH+Ј©Ј¬УГАлЧУ·ҪіМКҪұнКҫКЗ: CO32-Ј«H2O ![]() HCO3ЈӯЈ«OHЈӯЎЈ
HCO3ЈӯЈ«OHЈӯЎЈ
ЈЁ3Ј©XәНZөДИЬТә·ҙУҰөДАлЧУ·ҪіМКҪКЗAg++Cl-===AgClЎэ;ЈЁ4Ј©NәН°ұЛ®·ҙУҰөДАлЧУ·ҪіМКҪКЗAl3++3NH3ЎӨH2O===AlЈЁOHЈ©3Ўэ+3NH4+ЎЈ
ЈЁ4Ј©ИфТӘјмСйYЦРЛщә¬өДСфАлЧУЈ¬ХэИ·өДКөСй·Ҫ·ЁКЗИЎЙЩБҝBУЪКФ№ЬЦРЈ¬јУИлЕЁNaOHИЬТәІўјУИИЈ¬УГКӘИуөДәмЙ«КҜИпКФЦҪ·ЕФЪКФ№ЬҝЪЈ¬№ЫІмКЗ·сұдА¶Й«ЎЈ


 ФД¶БҝміөПөБРҙр°ё
ФД¶БҝміөПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБР№ШУЪІ»РвёЦәНЖХНЁёЦөДРрКцЦРХэИ·өДКЗЈЁ Ј©
A. ЧйіЙФӘЛШПаН¬
B. ДНёҜКҙРФДЬІ»Н¬
C. ¶јКфУЪёЦЈ¬ТтҙЛОпАнРФЦКПаН¬
D. №№іЙөДЦчТӘФӘЛШ¶јКЗМъЈ¬ТтҙЛ»ҜС§РФЦКНкИ«ПаН¬
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ[»ҜѧѡРЮ5УР»ъ»ҜС§»щҙЎ]УР»ъОпFКЗТ»ЦЦЦШТӘөДТҪТ©ЦРјдМеЈ¬ТФ»ҜәПОпAЈЁПа¶Ф·ЦЧУЦКБҝОӘ126.5Ј©ОӘФӯБПәПіЙFөД№ӨТХБчіМИзПВЈә

ТСЦӘЈә
ЈЁ1Ј©AөДҪб№№јтКҪОӘ Ј¬D·ЦЧУЦРә¬Сх№ЩДЬНЕөДГыіЖОӘ_______Ј¬·ҙУҰBЎъCөД·ҙУҰАаРНОӘ ЎЈ
ЈЁ2Ј©1molCФЪТ»¶ЁМхјюПВЧо¶аДЬУл______mol NaOH·ҙУҰЎЈ
ЈЁ3Ј©ТСЦӘDУлSOCl2·ҙУҰіэЙъіЙEНв»№УРБҪЦЦТЧИЬУЪЛ®өДЖшМеЙъіЙЈ¬·ҙУҰөД»ҜС§·ҪіМКҪОӘ ЎЈ
ЈЁ4Ј©ВъЧгПВБРМхјюөДУР»ъОпDөДН¬·ЦТм№№МеУР______ЦЦЎЈ
ўЩКфУЪ1Ј¬3Ј¬5ЎӘИэИЎҙъұҪЈ» ўЪДЬ·ўЙъТшҫө·ҙУҰЈ» ўЫДЬУлВИ»ҜМъИЬТәПФЧПЙ«
ЈЁ5Ј©BФЪЙъіЙD·ҙУҰ№эіМ»№ҝЙөГөҪБнТ»ЦЦёұІъОпGЈЁ Ј©Ј¬ПВБРУР№ШGөДРрКцХэИ·өДКЗ ЎЈЈЁМоСЎПоЈ©
Ј©Ј¬ПВБРУР№ШGөДРрКцХэИ·өДКЗ ЎЈЈЁМоСЎПоЈ©
AЈ®ДЬУлТТ¶юҙјНЁ№эјУҫЫ·ҙУҰөГөҪёЯ·ЦЧУІДБП
BЈ®ДЬ·ўЙъИЎҙъ·ҙУҰәНјУіЙ·ҙУҰ
CЈ®ёГ·ЦЧУЦРЧо¶аУР8ёцМјФӯЧУ№ІЖҪГж
DЈ®ёГ·ЦЧУЦРЧо¶аУР1ёцКЦРФМјФӯЧУ
ЈЁ6Ј©ёщҫЭТСУРЦӘК¶ІўҪбәППа№ШРЕПўЈ¬РҙіцТФ»ҜәПОпCH2ЈЁCOOC2H5Ј©2ОӘУР»ъ·ҙУҰФӯБПЦЖұёCH3OCOCH2CH2CH2CH2COOCH3өДәПіЙВ·ПЯБчіМНјЈЁЧўГч·ҙУҰМхјюЈ¬ОЮ»ъКФјБИОСЎЈ©ЎЈәПіЙВ·ПЯБчіМНјКҫАэИзПВЈә

Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝОӘБЛМбҙҝПВБРОпЦК(АЁәЕЦРОӘФУЦК),ЛщСЎіэФУКФјБәН·ЦАл·Ҫ·Ё¶јХэИ·өДКЗ( )
СЎПо | ұ»МбҙҝөДОпЦК(ФУЦК) | іэФУКФјБ | ·ЦАл·Ҫ·Ё |
AЈ® | H2O(Br2) | CCl4 | ЭНИЎ·ЦТә |
BЈ® | MgCl2ИЬТә(AlCl3) | ЕЁ°ұЛ® | №эВЛ |
CЈ® | CO2(HCl) | ұҘәНNa2CO3ИЬТә | ПҙЖш |
DЈ® | Si(Al) | NaOHИЬТә | №эВЛ |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝAЎўBЎўCЎўDОӘН¬Т»ЦЬЖЪөД4ЦЦФӘЛШЈ¬ТСЦӘ0.2 mol AУлЧгБҝЛбід·Ц·ҙУҰәуЙъіЙ2.24 L H2ЈЁұкЧјЧҙҝцПВЈ©ЎЈBөДСх»ҜОпјИҝЙИЬУЪЛбУЦҝЙИЬУЪЗҝјоИЬТәЎЈCЎўDАлЧУөДөзЧУІгҪб№№УллІФӯЧУПаН¬Ј¬CөгИјКұУлСхЖш·ҙУҰЙъіЙөДСх»ҜОпҝЙУлCөДЖшМ¬Зв»ҜОп·ҙУҰөГөҪCөДөҘЦКЈ¬DөҘЦКіЈОВПВОӘЖшМ¬ЎЈ
ЈЁ1Ј©AЎўBЎўCЎўDөДФӘЛШГыіЖ·ЦұрОӘЈәA Ј¬B Ј¬C Ј¬D ЎЈ
ЈЁ2Ј©»ӯіцBөДФӯЧУҪб№№КҫТвНј ЎЈ
ЈЁ3Ј©CФЪЦЬЖЪұнЦРО»УЪөЪ ЦЬЖЪ ЧеЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ»·ҫіОЫИҫТСіЙОӘИЛАаЙз»бГжБЩөДЦШҙуНюРІЈ¬ЛбУкКЗТ»ЦЦЦШТӘөД»·ҫіОЫИҫЈ¬ЛбУкөДРОіЙЦчТӘКЗУЙУЪЈЁ Ј©
AЈ®ЙӯБЦУцөҪВТҝіВТ·ҘЈ¬ЖЖ»өБЛЙъМ¬ЖҪәв
BЈ®ҙуБҝИј·ЕСМ»Ёұ¬Цс
CЈ®ҙуЖшЦР¶юСх»ҜМјөДә¬БҝФцјУ
DЈ®ҙуБҝИјЙХә¬БтИјБП
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝјшұрөн·ЫЎўө°°ЧЦКЎўЖПМСМЗЛ®ИЬТәЈ¬ТАҙОҝЙ·ЦұрК№УГөДКФјБәН¶ФУҰөДПЦПуХэИ·өДКЗ
A. өвЛ®Ј¬ұдА¶Й«Ј»ЕЁПхЛбЈ¬ұд»ЖЙ«Ј»РВЦЖCu(OH)2Ј¬Ч©әмЙ«іБөн
B. ЕЁПхЛбЈ¬ұд»ЖЙ«Ј»РВЦЖCu(OH)2Ј¬Ч©әмЙ«іБөнЈ»өвЛ®Ј¬ұдА¶Й«
C. РВЦЖCu(OH)2Ј¬Ч©әмЙ«іБөнЈ»өвЛ®Ј¬ұдА¶Й«Ј»ЕЁПхЛбЈ¬ұд»ЖЙ«
D. өвЛ®Ј¬ұдА¶Й«Ј»РВЦЖCu(OH)2Ј¬Ч©әмЙ«іБөнЈ»ЕЁПхЛбЈ¬ұд»ЖЙ«
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВұнОӘФӘЛШЦЬЖЪұнөДТ»Іҝ·ЦЈә
Че | ||||||||
1 | ўЩ | |||||||
2 | ўЪ | |||||||
3 | ўЫ | ўЬ | ўЭ | ўЮ | ||||
I. ЗлІОХХФӘЛШўЩЈӯўЮФЪұнЦРөДО»ЦГЈ¬УГ»ҜС§УГУп»ШҙрПВБРОКМвЈә
ЈЁ1Ј©»ӯіцФӘЛШўЪөДАлЧУҪб№№КҫТвНј______________ЎЈ
ЈЁ2
ЈЁ3Ј©ФӘЛШўЬәНўЮРОіЙөД»ҜәПОпөДөзЧУКҪЈә____________________ЎЈ
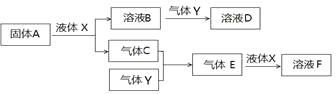
II. УЙЙПКцІҝ·ЦФӘЛШЧйіЙөДОпЦКјдЈ¬ФЪТ»¶ЁМхјюПВЈ¬ҝЙТФ·ўЙъПВНјЛщКҫөДұд»ҜЈ¬ЖдЦРAКЗТ»ЦЦөӯ»ЖЙ«№ММеЎЈЗл»ШҙрЈә
ЈЁ4Ј©Рҙіц№ММеAУлТәМеX·ҙУҰөДАлЧУ·ҪіМКҪ ЎЈ
ЈЁ5Ј©ЖшМеYКЗТ»ЦЦҙуЖшОЫИҫОпЈ¬ЦұҪУЕЕ·Е»бРОіЙЛбУкЎЈҝЙУГИЬТәBОьКХЈ¬Рҙіц№эБҝөДYУлB
ИЬТә·ҙУҰөДАлЧУ·ҪіМКҪ__________________________________________________
ЈЁ6Ј©ИфЖшМеCУлYФЪәгИЭҫшИИөДМхјюПВ·ҙУҰЈ¬ПВБРДДР©Лө·ЁЛөГчёГ·ҙУҰҙпөҪЖҪәвЧҙМ¬Јә_______
A. ОВ¶ИІ»ұд
B. 2vХэЈЁCЈ©=vДжЈЁYЈ©
C.»мәПЖшМеөДГЬ¶ИІ»ұд
D.»мәПЖшМеөДЖҪҫщПа¶Ф·ЦЧУЦКБҝІ»ұд
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРУР№ШОпЦКөДРФЦК»тУҰУГөДЛө·ЁХэИ·өДКЗ
AЈ®ҫ§Ме№иҫЯУР°лөјМеРФЦКЈ¬ҝЙУГУЪЙъіЙ№вөјПЛО¬
BЈ®УГNa2O2ЖҜ°Ч№эөДЦҜОпЎўВуёСИХҫГУЦҪҘҪҘұдіЙ»ЖЙ«
CЈ®K2FeO4ҫЯУРЗҝСх»ҜРФЈ¬ҝЙУГУЪЧФАҙЛ®өДЙұҫъПы¶ҫЎў
DЈ®ЕЁБтЛбҫЯУРҪПЗҝЛбРФЈ¬іЈУГЧчөн·ЫЛ®ҪвөДҙЯ»ҜјБ
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com