
【题目】下表为元素周期表的一部分:
族 | ||||||||
1 | ① | |||||||
2 | ② | |||||||
3 | ③ | ④ | ⑤ | ⑥ | ||||
I. 请参照元素①-⑥在表中的位置,用化学用语回答下列问题:
(1)画出元素②的离子结构示意图______________。
(2
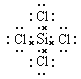
(3)元素④和⑥形成的化合物的电子式:____________________。
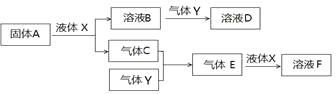
II. 由上述部分元素组成的物质间,在一定条件下,可以发生下图所示的变化,其中A是一种淡黄色固体。请回答:
(4)写出固体A与液体X反应的离子方程式 。
(5)气体Y是一种大气污染物,直接排放会形成酸雨。可用溶液B吸收,写出过量的Y与B
溶液反应的离子方程式__________________________________________________
(6)若气体C与Y在恒容绝热的条件下反应,下列哪些说法说明该反应达到平衡状态:_______
A. 温度不变
B. 2v正(C)=v逆(Y)
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
【答案】Ⅰ.(1) (1分) (2)S2->O2-> Na+(1分)
(1分) (2)S2->O2-> Na+(1分)
(3) (1分)
(1分)
Ⅱ.(4)2Na2O2+2H2O=4Na++ 4OH―+ O2↑(2分)
(5)SO2 + OH-= HSO3-(2分)(6)ABD(2分)(6分)
【解析】试题分析:Ⅰ.由元素在周期表中的位置可知,①为H、②为O、③为Na、④为Si、⑤为S、⑥为Cl.
(1)元素②的离子为O2-,原子核外有10个电子,离子结构示意图为![]() ;
;
(2)电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,所以离子半径大小顺序是S2->O2->Na+;
(3)元素④与⑥形成化合物为SiCl4,属于共价化合物,硅原子和每个Cl原子之间都存在共价键,其电子式为![]() ;
;
Ⅱ.由上述部分元素组成的物质,A是一种淡黄色固体,则A为Na2O2,能与液态X反应生成气体C与B的溶液,可推知X为H2O、B为NaOH、C为O2;
(4)过氧化钠和水反应生成NaOH和氧气,离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑;
(5)气体Y是一种大气污染物,直接排放会形成酸雨,Y为SO2,过量的二氧化硫与NaOH反应生成NaHSO3,反应离子方为:SO2+OH-=HSO3-;
(6)A.绝热条件下,随反应进行温度升高,温度不变时说明到达平衡,故A正确;B.由方程式可知2v正(C)=v正(Y),而2v正(C)=v逆(Y),说明二氧化硫的生成速率与消耗速率相等,反应到达平衡,故B正确;C.混合气体总质量不变,容器容积不变,混合气体的密度始终不变,故C错误;D.混合气体总质量不变,随反应进行混合气体物质的量减小,混合气体相对分子质量增大,当混合气体的平均分子量不变,说明反应到达平衡,故D正确;故选ABD。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】常见的五种盐X、Y、Z、M、N,它们的阴离子可能是SO42-、Cl-、NO3-、CO32-,阳离子可能是Ag+、NH4+、Na+、Al3+、Cu2+、Ba2+、Fe3+,已知:
①M的焰色反应呈黄色。
②五种盐均溶于水,水溶液均为无色。
③X的溶液呈中性,Y、Z、N的溶液呈酸性,M的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有X、Z的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,N和Z的溶液中生成沉淀,继续加氨水,Z中沉淀消失。
⑥把X的溶液分别加入到Y、Z、N的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,所含阴离子相同的两种盐的化学式是__________________
(2)M溶液显碱性的原因是(用离子方程式表示)______________________
(3)X和Z的溶液反应的离子方程式是_______________________
(4)N和氨水反应的离子方程式是_____________________________________
(5)若要检验Y中所含的阳离子,正确的实验方法是______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下左图所示实验装置可以测定常温常压下气体的摩尔体积。
 c
c
甲同学利用如上左图装置,根据下列步骤完成实验:
① 装配好装置,作气密性检查。
②用砂纸擦去镁带表面的氧化物,然后取0.108g的镁带。
③取下A瓶加料口的橡皮塞,用小烧杯加入20mL水,再把已称量的镁带加到A瓶的底部,用橡皮塞塞紧加料口。
④用注射器从A瓶加料口处抽气,使B瓶导管内外液面持平。
⑤用注射器吸取10mL3mol·L-1硫酸溶液,用针头扎进A瓶加料口橡皮塞,将硫酸注入A瓶,注入后迅速拔出针头。
⑥当镁带完全反应后,读取C瓶中液体的体积,记录数据。⑦用注射器从A瓶加料口处抽出8.0mL气体,使B瓶中导管内外液面持平。⑧读出C瓶中液体体积是115.0mL。
完成下列填空:
(1) 在常温常压下气体摩尔体积理论值约为24.5L/mol,甲同学测出此条件下lmol气体的体积为______,计算此次实验的相对误差为________%〈保留2位有效数字)。引起该误差的可能原因是______。
a.镁带中含铝; b.没有除去镁带表面的氧化物; c.反应放热; d.所用硫酸的量不足
(2) 丙同学提出可用如上右图装置完成该实验。该装置气密性的检查方法是:_____________。
(3) 与原方案装置相比,丙同学使用的装置实验精度更高。请说明理由(回答两条)____________________________________,_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga_____________As,第一电离能Ga____________As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGa g·mol-1 和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质既能因发生化学反应使溴水褪色,又能使酸性KMnO4溶液褪色的是( )
①SO2 ②![]() ③
③![]()
④![]() ⑤CH
⑤CH![]() C CH3⑥CH3(CH2)4CH3
C CH3⑥CH3(CH2)4CH3
A. ①②③④ B. ③④⑤ C. ①②④⑥ D. ①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g)+2N2(g)+6H2(g)![]() Si3N4(s)+12HCl(g) ΔH <0
Si3N4(s)+12HCl(g) ΔH <0
完成下列填空:
(1)试写出SiCl4的电子式_____________________________。
(2)在一定温度下进行上述反应,若反应容器的容积为2 L,3 min后达到平衡,测得固体的物质的量增加了0.02mol,则H2的平均反应速率为____________________。
(3)上述反应达到平衡后,下列说法正确的是__________。
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si3N4的物质的量平衡向左移动
d.其他条件不变,增大HCl的浓度平衡向左移动
(4)一定条件下,在恒容密闭的容器中,能表示上述反应达到化学平衡状态的是_____。
a.3v逆(N2)= v正(H2)
b.v正(HCl)=4v正(SiCl4)
c.混合气体密度保持不变
d.c(N2):c(H2):c(HCl)=1:3:6
e.单位时间内有n molN2消耗的同时有6 molHCl生成
(5)若平衡时H2和HCl的物质的量之比为m:n,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比_______m:n(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用正确的序号填空: ①12C、13C、14C; ②红磷和白磷; ③H2O和D2O;④CH3CH2OH与CH3OCH3; ⑤CH4和CH3CH3;
互为同位素的是 ; 互为同素异形体的是 ;
互为同分异构体的是 ; 互为同系物的是
(2)由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 金属A不 | C的质 | A上有气 |
根据实验现象回答下列问题:
①装置甲中作正极的是________ (填“A”或“B”) 。
②装置乙溶液中Cu2+向_______极移动(填“B”或“C”)。
③装置丙中金属A上电极反应属于______(填“氧化反应”或“还原反应”)。
④四种金属活动性由强到弱的顺序是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修2:化学与技术】高锰酸钾(KMnO4)是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:

回答下列问题:
(1)原料软锰矿与氢氧化钾按1∶1的比例在“烘炒锅”中混配,混配前应将软锰矿粉碎,其作用是 。
(2)“平炉”中发生的化学方程式为 。
(3)“平炉”中需要加压,其目的是 。
(4)将K2MnO4转化为KMnO4的生产有两种工艺。
①“![]() 歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应,反应中生成K2MnO4,MnO2和 (写化学式)。
歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应,反应中生成K2MnO4,MnO2和 (写化学式)。
②“电解法”为现代工艺,即电解K2MnO4水溶液,电解槽中阳极发生的电极反应为 ,阴极逸出的气体是 。
③“电解法”和“![]() 歧化法”中,K2MnO4的理论利用率之比为 。
歧化法”中,K2MnO4的理论利用率之比为 。
(5)高锰酸钾纯度的测定:称取1.0800 g样品,溶解后定容于100 mL容量瓶中,摇匀。取浓度为0.2000 mol·L1的H2C2O4标准溶液20.00 mL,加入稀硫酸酸化,用KMnO4溶液平行滴定三次,平均消耗的体积为24.48 mL,该样品的纯度为
(列出计算式即可,已知2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com