
【题目】[化学——选修3:物质结构与性质]砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga_____________As,第一电离能Ga____________As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGa g·mol-1 和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。

【答案】(1)1s22s22p63s23p63d104s24p3;(2) 大于,小于;(3)三角锥形,sp3;(4)GaF3是离子晶体,GaCl3是分子晶体,离子晶体GaF3的熔沸点高;(5)原子晶体;共价键;![]() 。
。
【解析】
试题分析:(1)As的原子序数是33,则基态As原子的核外电子排布式为1s22s22p63s23p63d104s24p3。
(2)同周期自左向右原子半径逐渐减下,则原子半径Ga大于As,由于As的4p轨道电子处于半充满状态,稳定性强,所以第一电离能Ga小于As。
(3)AsCl3分子的价层电子对数=3+![]() =4,即含有一对孤对电子,所以立体构型为三角锥形,其中As的杂化轨道类型为sp3。
=4,即含有一对孤对电子,所以立体构型为三角锥形,其中As的杂化轨道类型为sp3。
(4)由于GaF3是离子晶体,GaCl3是分子晶体,所以离子晶体GaF3的熔沸点高;
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示,熔点很高,所以晶体的类型为原子晶体,其中Ga与As以共价键键合。根据晶胞晶胞可知晶胞中Ca和As的个数均是4个,所以晶胞的体积是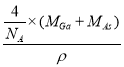 。二者的原子半径分别为rGa pm和rAs pm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为
。二者的原子半径分别为rGa pm和rAs pm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为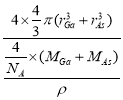 ×100%=
×100%=![]() 。
。


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
【题目】恒温恒容下,将2 mol A气体和2 mol B气体通入体积为2 L的密闭容器中发生如下反应:2A(g)+B(g)![]() xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol·L-1。
xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol·L-1。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为________。
(2)x=________。
(3)A的转化率与B的转化率之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为同一周期的4种元素,已知0.2 mol A与足量酸充分反应后生成2.24 L H2(标准状况下)。B的氧化物既可溶于酸又可溶于强碱溶液。C、D离子的电子层结构与氩原子相同,C点燃时与氧气反应生成的氧化物可与C的气态氢化物反应得到C的单质,D单质常温下为气态。
(1)A、B、C、D的元素名称分别为:A ,B ,C ,D 。
(2)画出B的原子结构示意图 。
(3)C在周期表中位于第 周期 族。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鉴别淀粉、蛋白质、葡萄糖水溶液,依次可分别使用的试剂和对应的现象正确的是
A. 碘水,变蓝色;浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀
B. 浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀;碘水,变蓝色
C. 新制Cu(OH)2,砖红色沉淀;碘水,变蓝色;浓硝酸,变黄色
D. 碘水,变蓝色;新制Cu(OH)2,砖红色沉淀;浓硝酸,变黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的叙述中不正确的是
A.丙烷跟甲烷一样能与氯气发生取代反应
B.1 mol乙酸与乙醇在一定条件下发生酯化反应,可生成1 mol乙酸乙酯
C.CH2Cl2是纯净物说明甲烷是四面体结构而不是正方形结构
D.溴水既可鉴别乙烷与乙烯,又可除去乙烷中的乙烯而得到纯净的乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分:
族 | ||||||||
1 | ① | |||||||
2 | ② | |||||||
3 | ③ | ④ | ⑤ | ⑥ | ||||
I. 请参照元素①-⑥在表中的位置,用化学用语回答下列问题:
(1)画出元素②的离子结构示意图______________。
(2
(3)元素④和⑥形成的化合物的电子式:____________________。
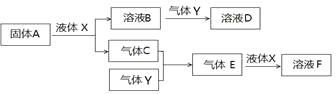
II. 由上述部分元素组成的物质间,在一定条件下,可以发生下图所示的变化,其中A是一种淡黄色固体。请回答:
(4)写出固体A与液体X反应的离子方程式 。
(5)气体Y是一种大气污染物,直接排放会形成酸雨。可用溶液B吸收,写出过量的Y与B
溶液反应的离子方程式__________________________________________________
(6)若气体C与Y在恒容绝热的条件下反应,下列哪些说法说明该反应达到平衡状态:_______
A. 温度不变
B. 2v正(C)=v逆(Y)
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[物质结构与性质]
[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2-+4H++4H2O===[Zn(H2O)4]2++4HOCH2CN

(1)Zn2+基态核外电子排布式为____________________。
(2)1 mol HCHO分子中含有σ键的数目为____________mol。
(3)HOCH2CN分子中碳原子轨道的杂化类型是______________。
(4)与H2O分子互为等电子体的阴离子为________________。
(5)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3月调研)[化学——选修3:物质结构与性质]氮化硼( BN)是一种重要的功能陶瓷材料。以天然硼砂(主要成分Na2B4O7)为起始物,经过一系列反应可以得到BN和火箭高能燃料及有机合成催化剂BF3的过程如下:

(1)写出由B203制备BF3的化学方程式 ,BF3中B原子的杂化轨道类型为____,BF3分子空间构型为____。
(2)在硼、氧、氟、氮中第一电离能由大到小的顺序是(用元素符号表示)____。
(3)已知:硼酸的电离方程式为H3B03 +H20 ![]() [B(OH)4] - +H+,试依据上述反应写出[ Al( OH)4] -的结构式____,并推测1mol NH4BF4(氟硼酸铵)中含有____个配位键。
[B(OH)4] - +H+,试依据上述反应写出[ Al( OH)4] -的结构式____,并推测1mol NH4BF4(氟硼酸铵)中含有____个配位键。
(4)由12个硼原子构成如图1的结构单元,硼晶体的熔点为1873℃,则硼晶体的1个结构单元中含有____ 个B-B键。

(5)氮化硼(BN)晶体有多种相结构。六方相氮化硼(晶体结构如图2)是通常存在的稳定相可作高温润滑剂。立方相氮化硼(晶体结构如图3)是超硬材料,有优异的耐磨性。
①关于这两种晶体的说法,不正确的是____(填字母)。
a.两种晶体均为分子晶体
b.两种晶体中的B-N键均为共价键
c.六方相氮化硼层间作用力小,所以质地软
d.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体内B-N键数与硼原子数之比为__ __,其结构与石墨相似却不导电,原因是____。
③立方相氮化硼晶体中,每个硼原子连接____个六元环。该晶体的天然矿物在青藏高原地下约300 km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯和液溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑。填写下列空白:

(1)写出A中反应的化学方程式__________________________________________。
(2)试管C中苯的作用是:________________。反应开始后,观察D和E两试管,看到的现象为:D________________;E________________。
(3)B中的NaOH溶液的作用是_____________________________________________,可观察到的现象是________________。
(4)在上述整套装置中,具有防倒吸的装置有________(填字母序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com