
【题目】下列有关说法正确的是( )
A. 若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀
B. 2NO(g)+2CO(g)===N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0
C. 加热0.1 mol·L-1Na2CO3溶液,CO![]() 的水解程度和溶液的pH均增大
的水解程度和溶液的pH均增大
D. 对于乙酸与乙醇的酯化反应(ΔH<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e为元素周期表前3周期中的部分元素,它们在元素周期表中的相对位置如图所示.下列叙述正确的是( ) 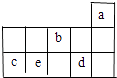
A.b元素除0价外,只有一种化合价
B.五种元素中,c元素的性质最稳定
C.d气态氢化物溶于水,溶液显碱性
D.e元素最高价氧化物对应的水化物和不同量的氢氧化钠反应,可能生成三种盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图所示,甲池的总反应式为:N2H4+O2=N2+2H2O,下列关于该电池工作时的说法正确的是
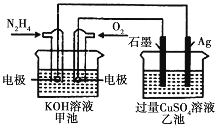
A. 该装置工作时,Ag电极上有气体生成
B. 甲池和乙池中的溶液的pH均减小
C. 甲池中负极反应为N2H4-4e-=N2+4H+
D. 当甲池中消耗0.1molN2H4时,乙池中理沦上最多产生6.4g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃是一种比水轻的油状液体,相对分子质量为78,碳元素与氢元素的质量比为12:1,不能使溴水和酸性高锰酸钾溶液褪色.写出此烃发生取代反应的化学方程式(任意写一个即可) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型,NiMH中的M表示储氢金属或合金,该电池在充电过程中的总反应方程式是Ni(OH)2+M===NiOOH+MH。已知:6NiOOH+NH3+H2O+OH-===6Ni(OH)2+NO![]()
下列说法正确的是( )
A. NiMH电池放电过程中,正极的电极反应式为NiOOH+H2O+e-===Ni(OH)2+OH-
B. 充电过程中OH-从阳极向阴极迁移
C. 充电过程中阴极的电极反应式:H2O+M+e-===MH+OH-,H2O中的H被M还原
D. NiMH电池中可以用KOH溶液、氨水等作为电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如下图所示,其中阴极和阳极均为惰性气体电极。测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法正确的是
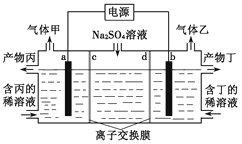
A. a极与电源的负极相连
B. 产物丁为硫酸溶液
C. 离子交换膜d为阴离子交换膜(允许阴离子通过)
D. b电极反立式为2H2O+2e-=2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列两个热化学方程式:
H2(g)+ ![]() O2(g)═H2O(l)△H=﹣285kJ/mol
O2(g)═H2O(l)△H=﹣285kJ/mol
C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=﹣2220.0kJ/mol
(1)实验测得H2和C3H8的混合气体共3mol完全燃烧生成液态水时放热2790kJ,则混合气体中H2和C3H8的体积比为 .
(2)已知:H2O(l)═H2O(g)△H=+44.0kJ/mol,写出丙烷燃烧生成CO2和气态水的热化学方程式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com