
����Ŀ������ͼ��ʾ��һ�ܱ���������Ħ�����ɻ�����������a��b�ֳɼס������ң���״���£��������г���NH30.4mol�������г���HCl��N2�Ļ�����壬��ֹʱ����λ����ͼ��ʾ����֪�ס������������������֮��Ϊ17.3g��
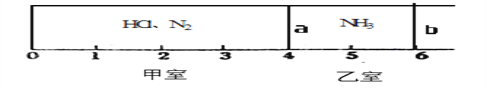
��1��������HCl��N2������֮��Ϊ__________________��
��2��������aȥ����һ��ʱ�����b���ȶ�λ�ڿ̶ȡ�________�����������֣������ǹ������ʲ�����ѹǿ������ʱ��ϵ��ƽ����Է�������Ϊ________��
����֪���ᡢ��ˮ���ܶ�������ˮ�����Ĺ�ϵ��ͼ��ʾ�����������백ˮ��һ�ݣ�����ݱ�����Ϣ���ش��������⣺
���ʵ����ʵ���Ũ��/molL-1 | ��Һ���ܶ�/gcm-3 | |
���� | c1 | ��1 |
��ˮ | c2 | ��2 |
��1�������������������Ϊ________����д��λ���ú�c1����1�Ĵ���ʽ��ʾ����
��2�����ʵ���Ũ��Ϊc1molL-1��������ˮ�������ϣ���Ϻ���Һ������仯���Բ��ƣ���������Һ�����ʵ���Ũ��Ϊ________molL-1��
��3�������ʵ���Ũ�ȷֱ�Ϊc2molL-1��0.2c2molL-1�İ�ˮ��������ϣ�������Һ�����ʵ���Ũ��__________0.6c2molL-1������ڡ�����С�ڡ����ڡ��������Ϻ���Һ������仯���Բ��ƣ���
���𰸡� 73��168 4 25.25 ![]() C1/2 ����
C1/2 ����
��������������Ҫ�����й����ʵ����ļ��㡣
��1��������0.4molNH3������Ϊ6.8g��������HCl��N2�����������ʵ����ǰ�������Ϊ0.8mol������Ϊ(6.8+17.3)g=24.1g��n(HCl)+n(N2)=0.8mol��36.5g/mol��n(HCl)+28g/mol��n(N2)=24.1g�����n(HCl)=0.2mol��n(N2)=0.6mol��������HCl��N2������֮��Ϊ(36.5��0.2):(28��0.6)=73:168��
��2��������aȥ����һ��ʱ���NH3+HCl![]() NH4Cl���÷�Ӧʣ��0.2mol��������b���ȶ�λ�ڿ̶ȡ�4��������ʱ��ϵ��ƽ����Է�������Ϊ(0.2��17+0.6��28)/(0.2+0.6)=25.25��
NH4Cl���÷�Ӧʣ��0.2mol��������b���ȶ�λ�ڿ̶ȡ�4��������ʱ��ϵ��ƽ����Է�������Ϊ(0.2��17+0.6��28)/(0.2+0.6)=25.25��
��1�������������������Ϊ98c1/(1000��1)=![]() ��
��
��2�����ʵ���Ũ��Ϊc1molL-1��������ˮ�������ϣ���Ϻ���Һ������仯���Բ��ƣ���������Һ�����ʵ���Ũ��ΪC1/2molL-1��
��3��������������ˮ�������ϣ�������Һ�����ʵ���Ũ��Ϊ0.6mol��L��1��������������Һ��������ϣ������ܶ�ǰ��<���ߣ���c2molL-1��ˮ������ϴ�����������Һ�����ʵ���Ũ�ȴ���0.6c2molL-1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڣ�NH4��2SO4��Һ������˵����ȷ���ǣ� ��
A.��Һ�д��ڵ���ƽ�⣺��NH4��2SO4?2NH ![]() +SO
+SO ![]()
B.����Һ�еμ�����Ũ���ᣬc��NH ![]() ����c��SO
����c��SO ![]() ��������
��������
C.��ˮϡ�ͣ���Һ���������ӵ�Ũ�Ⱦ���С
D.��Һ�У�c��SO ![]() ��=2c��NH
��=2c��NH ![]() ��+2c��NH3?H2O��
��+2c��NH3?H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ƽ�����̣�����������ȵ�A��B���ձ�������ƽ�⣬Ȼ��ֱ���������ȵ��������ᣬ�̶���AB���ձ��з��������������ʣ������ƽ�Ա���ƽ����ǣ� ��
A. ��������Na��Mg B. 0.1molZn��0.1molAl
C. 8.4gMgCO3��8.4gNaHCO3 D. 10gCaCO3��10gMgCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ��(����)
A. ����ķ�ɢ������ֱ����10-9 ~10-7m֮��
B. �����ö����ЧӦ������Һ�ͽ���
C. �����������ᴿ����
D. ������ȶ���ԭ���ǽ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ȩ������NaOH��Һ�����¿��Է����ӳɷ�Ӧ������һ���ǻ�ȩ�� 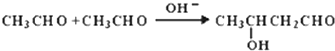
���ȩF������ʽΪC9H8O������Ȼ������ڹ����У���һ�ֳ��õ�ֲ���ζ�ͣ���ҵ����Ҫ�ǰ�����·�ߺϳɵģ�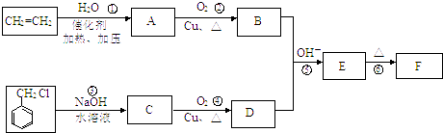
��֪����Ӧ��Ϊ��ȩ���Ϸ�Ӧ����ش�
��1�����ȩF�Ľṹ��ʽΪ�� �� E�к��������ŵ�����Ϊ ��
��2����Ӧ�١����з���ԭ�Ӿ����Ե��� ��
��3��д������ת���Ļ�ѧ����ʽ�� ��
��
д���йط�Ӧ�����ͣ�
��
��
��4����������Ҫ���E���ʵ�ͬ���칹�����֣�������������ȡ������������һ�����ڶ�λ���������ࣩ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ǧ���ص��ܷ�ӦʽΪ��PbO2+Pb+2H2SO4 ![]() 2PbSO4+2H2O�ݴ��ж�����������ȷ���ǣ� ��
2PbSO4+2H2O�ݴ��ж�����������ȷ���ǣ� ��
A.�ŵ�ʱ��H2SO4Ũ������
B.�ŵ�ʱ�������ĵ缫��ӦʽΪ��Pb+SO42����2e���TPbSO4
C.�ڳ��ʱ�������ÿת��1 mol���ӣ�����������2 mol����
D.�ڳ��ʱ�����������ķ�Ӧ��PbSO4��2e��+2H2O�TPbO2+SO42��+4H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����______���______���ܹ�����Ļ������������ʡ��������Һ֮�����ܹ����磬��������������Һ�з�����______��������______������ʱ���ɵ�______����ȫ����______�Ļ������������ɵ�______����ȫ����______�Ļ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�϶������Ե��ǣ� ��
A.��H+����Һ
B.��ʹ��̪����ɫ����Һ
C.pH��7����Һ
D.c��OH������c��H+������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯��Ҫ���뻹ԭ������ʵ�ֵ��ǣ���
A. CO32-��CO2 B. Cl-��Cl2 C. Cr2O72-��Cr3�� D. NH3��NO
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com