
【题目】由SO2和O2制备SO3(熔点16.8 ℃,沸点44.8 ℃)的模拟装置如图所示(加热和夹持装置省略):

下列说法正确的是( )
A.装置①中的试剂为饱和Na2SO3溶液
B.实验室可用铜与稀硫酸在加热条件下制取SO2
C.装置③反应管中的铂石棉用作反应的催化剂
D.从装置⑤逸出的气体有过量的SO2和O2
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在 5 L 的容器中,X、Y、Z 三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题。
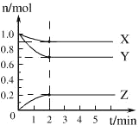
(1)反应进行至_________min 时达到平衡状态,此时 Y 的平均反应速率是________mol/ (L·min)。
(2)分析有关数据,写出 X、Y、Z 的反应方程式_________________;
(3)对于一个未知反应,影响反应速率的因素很多,请写出可能影响化学反应速率的三个因素:______________,____________,__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应CH4(g)+H2O(g) ![]() CO(g)+3H2(g) △H>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是( )
CO(g)+3H2(g) △H>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是( )
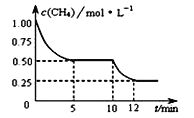
A. 10 min时,改变的外界条件可能是升高温度
B. 反应进行到12min时,CH4的转化率为25%
C. 0∽5 min内,v(H2)=0.1 mol·(L·min)-1
D. 恒温下,缩小容器体积,平衡后H2浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验方案能达到实验目的的是
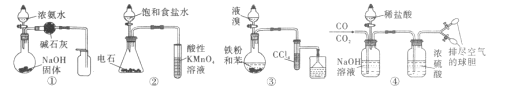
A.用图①的装置制取并收集干燥的NH3B.用图②的装置验证乙炔的还原性
C.用图③的装置制取溴苯D.用图④的装置分离CO和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图能量关系示意图,下列说法正确的是

A. 1 mol C(s)与1 mol O2(g)的能量之和为393.5 kJ
B. 反应2CO(g)+O2(g)= 2CO2(g)中,生成物的总能量大于反应物的总能量
C. 由C(s)→CO(g)的热化学方程式为:2C(s)+O2(g)= 2CO(g) ΔH=-221.2 kJ·mol-1
D. 热值指一定条件下单位质量的物质完全燃烧所放出热量,则CO热值ΔH=-10.1 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要的化工原料,其有关制备途径如图所示。下列说法正确的是

A. 途径①所用混酸中H2SO4与HNO3物质的量之比最好为2∶3
B. 利用途径③制备16g硫酸铜,消耗硫酸的物质的量为0.1mol
C. 生成等量的硫酸铜,三个途径中参加反应的硫酸的物质的量:①=②=③
D. 与途径①、③相比,途径②更好地体现了绿色化学思想
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向盛有100mLHNO3溶液的烧杯中加入一定量的Cu、Al合金(还原产物为NO ),充分反应后向溶液中加入lmol/L的NaOH溶液,产生沉淀的质量与所加溶液的体积的关系如下图所示。则原HNO3溶液的物质的最浓度是

A. 0.4mol/L B. 0.45mol/L C. 0.525mol/L D. 0.625mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性HSO3—>I-,氧化性IO3—>I2。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是( )

A.0~a间发生反应3HSO3—+IO3—===3SO42—+I-+3H+
B.a~b间共消耗NaHSO3的物质的量为1.2 mol
C.b~c间发生的反应中I2既是氧化产物又是还原产物
D.当溶液中I-与I2的物质的量之比为5∶2时,加入的KIO3为1.08 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】洁净安全的生存环境:2012年3月,新《环境空气质量标准》的颁布表明国家对环境问题的进一步重视。
(1)煤燃烧产生的SO2所形成的酸雨中,SO2最终转化成的酸是___(填化学式)。在煤中加入适量___,可以大大减少煤燃烧时SO2的排放,该反应的化学方程式为:___。
(2)A、B、C三个城市全年雨水的月平均pH变化如图所示。
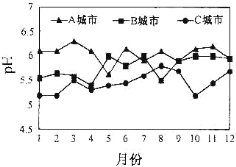
①受酸雨危害最严重的是___城市。
②汽车尾气中含有NO2、NO、CO等有害气体。汽车安装尾气净化装置可将NO、CO转化为无害气体。写出该反应的化学方程式:___。
③自来水生产过程中要经过:去除固体杂质和悬浮物、消毒、去除异味等一系净化工序。天然水中杂质较多,常需加入明矾,ClO2等物质处理后才能饮用:加入ClO2的作用是___;加入明矾后,Al3+水解生成的___(填化学式)胶体能吸附水中的悬浮颗粒,并使之沉降。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com